На примере карбоксипептидазы А
Рассмотрим механизм действия гидролаз на примере такой гидролазы, как карбоксипептидаза А.
Карбоксипептидаза А (КПА) – пищеварительный фермент, вырабатывается в поджелудочной железе в виде неактивного предшественника – прокарбоксипептидазы А, которая превращается в активный фермент под действием трипсина. Фермент действует как на низкомолекулярные субстраты, так и на белки. Типичные низкомолекулярные субстраты – карбобензоксиглицил-L-фенилаланин и карбобензоксиглицил-L-триптофан. В полипептидах карбоксипептидаза А гидролизует С-концевую пептидную связь. Особенно легко гидролизуются пептиды, в которых С-концевой остаток имеет ароматическую или большую алифатическую боковую цепь (рис. 3.2.1). Фермент не действует на концевые аминокислотные остатки, если они представлены основными аминокислотами или пролином.

Рис. 3.2.1. Реакция, катализируемая карбоксипептидазой А
Этот фермент интересен в том отношении, что по механизму катализа он принципиально отличается от лизоцима. Прежде чем перейти к подробному обсуждению механизма действия карбоксипептидазы А, отметим два основных аспекта.
1. Индуцированное соответствие. Связывание субстрата сопровождается значительными изменениями структуры фермента.
2. Смещение электронов. В активном центре фермента содержатся атом цинка и другие группы, которые индуцируют перераспределение электронов в субстрате, облегчая тем самым процесс гидролиза.
Трехмерную структуру карбоксипептидазы А (рис. 3.2.2) при разрешении в 0,2 нм получил в 1967 г. Уилльям Липском (W. Lipscomb).
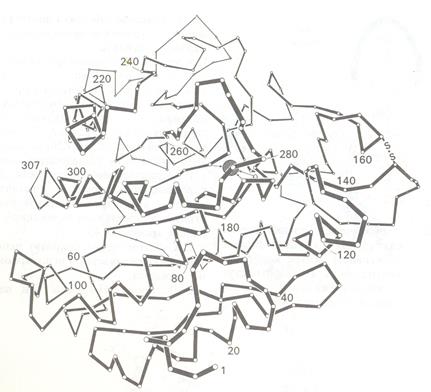
Рис3.2.2 Трехмерная структура карбоксипептидазы А. Показаны только α-углеродные атомы и ион цинка (заштрихованный кружок в центре)
Фермент содержит одну полипептидную цепь из 307 аминокислот, имеет компактную форму, которую можно приближенно описать как эллипсоидную с размерами 5х4,2х3,8 нм. В ферменте имеются области α-спиралей (38%) и β-складчатых слоев (17%). С белком прочно связан ион цинка, наличие которого необходимо для проявления ферментативной активности. Ион цинка расположен в углублении близко к поверхности молекулы, причем он образует координационные связи (в виде тетраэдра) с боковыми цепями двух гистидинов, боковой цепью глутамата и молекулой воды (рис. 3.2.3).
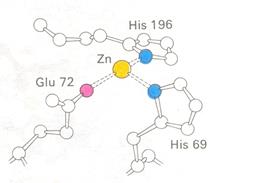
Рис. 3.2.3. Ион цинка, расположенный в активном центре карбоксипептидазы А, образует координационные связи с боковыми цепями двух гистидинов и глутамата. Занимающая 4-ю координационную связь молекула воды здесь не показана
Рядом с ионом цинка на ферменте имеется большого размера «карман», в который попадает боковая цепь концевого остатка пептидного субстрата.
Дата добавления: 2020-10-01; просмотров: 690;











