Правила определения степени окисления
1. Атомы кислорода имеют степень окисления «-2», за исключением окиси фтора О+2F2 и пероксидов 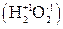 .
.
2. Атомы водорода во всех соединениях имеют степень окисления «+1» за исключением гидридов металла (Li+H-).
3. Степень окисления элемента в простом веществе (О2, Н2, Na, C) равна нулю.
4. Степень окисления атомов в ионных соединениях для данного иона равна по знаку и величине его электрическому заряду  .
.
5. В соединениях с ковалентной полярной связью, атомы элементов с большей величиной электроотрицательности имеют «–» степень окисления, а с меньшей электроотрицательностью «+» степень окисления.
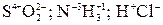 .
.
6. Степень окисления атомов в органических соединениях, определяется также, как и в ковалентно-полярных соединениях.
7. Алгебраическая сумма степеней окисления элементов в нейтральной молекуле равна нулю, в сложном ионе – заряду иона.
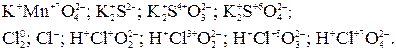
Различают 3 типа окислительно-восстановительных реакций:
1. Межмолекулярные – к ним относятся реакции, в которых окислитель и восстановитель находятся в разных веществах (например, рассмотренная выше реакция);
2. Внутримолекулярные – реакции, в которых окислитель и восстановитель находятся в одном и том же веществе, например в реакциях термического разложения:
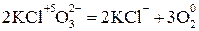
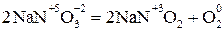
4. Диспропорционирования – реакции, в которых участвуют молекулы, атомы, ионы, проявляющие и окислительные, и восстановительные свойства:
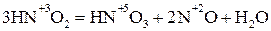 .
.
Дата добавления: 2020-03-21; просмотров: 623;











