Механизм реакции диазотирования
В реакцию диазотирования вступает свободный ароматический первичный амин, образующийся в результате гидролиза его солей. При взаимодействии нитритов металлов с минеральными кислотами устанавливается сложное равновесие, зависящее от кислотности среды и природы применяемых кислот.
Это равновесие ионов, расположенные в указанном ряду по убывающей активности, представляющие собой диазотирующие агенты:
1) ион нитрозония или нитрозоний-ион (N+ = O),
2) нитрозацидий-ион (H2O+ – N = O),
3) оксид азота (O2N – N = O),
4) азотистая кислота (HO – N = O).
Во всех случаях взаимодействие первичного ароматического амина с диазотирующей частицей приводит по синхронному механизму к первичному ароматическому нитрозоамину (Б.А.Порай-Кошиц, 1964 г.). Последний в кислой среде перегруппировывается в диазогидрат, находящийся в равновесии с диазокатионом:
 NaNO2 + HCl HO – N = O + NaCl
NaNO2 + HCl HO – N = O + NaCl
 H HCl
H HCl



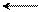

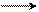
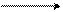

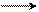

 Ar – N׃ + N+ = O Ar – NH – N = O Ar – N = N –OH ArN2+Cl–
Ar – N׃ + N+ = O Ar – NH – N = O Ar – N = N –OH ArN2+Cl–
H OH
 ариламин арилнитрозоамин арилдиазогидрат арилдиазонийхлорид
ариламин арилнитрозоамин арилдиазогидрат арилдиазонийхлорид
(катион диазония)
Успех реакции диазотирования зависит как от концентрации наиболее энергичного диазотирующего агента, так и от основности амина. Иногда условия, оптимальные для диазотирующих частиц, не слишком благоприятные для достижения макимальных концентраций свободного амина.
Дата добавления: 2017-01-16; просмотров: 2025;











