Функциональные производные карбоновых кислоты
О О О О
|| || || ||
R−C−OМ R−C−OR´ R−C−OS´ R−C−NH2
соли сложные эфиры сложные тиоэфиры амиды
О О О О О
|| || || || ||
R−C−NHR´ R−C−NR´2 R−C−Hal R−C−O−C−R O=C=O
замещенные амиды галогенангидриды ангидриды диоксид углерода
Взаимные превращения производных карбоновых кислот. Рассмотренные производные карбоновых кислот склонны к взаимопревращениям за счет реакций нуклеофильного замещения у карбонильного углеродного атома. Это отражено на рис. 9. На схеме указаны типовые реагенты, при помощи которых из карбоновой кислоты могут быть получены ее производные. Реагенты, отмеченные кружком, позволяют получить соответствующие им ацилпроизводные из любых других, расположенных на схеме правее. Наиболее реакционноспособны галогенангидриды карбоновых кислот (ацилгалогениды), которые можно превратить в ангидриды, сложные эфиры или амиды обработкой их или солью кислоты, или спиртом, или аммиаком соответственно. Ангидриды кислот легко превращаются в сложные эфиры или амиды. В организме галогенангидриды или ангидриды карбоновых кислот не встречаются.
Ацилкоферменты А по ацилирующей способности близки к ангидридам кислот. В организме они легко превращаются в сложные эфиры или амиды. Сложные эфиры действием аммиака или амина превращаются в амиды.
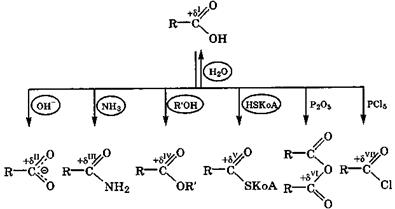
———————————————————————→
Возрастание реакционной способности в процессах гидролиза и ацилирования
+δII << +δIII < +δI < +δIV < +δV< +δVI < +δVII
Рис. 9. Схема получения производных карбоновых кислот и их превращений
Сложные эфиры и тиоэфиры.Эфиры имеют общую формулу 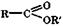 , а тиоэфиры
, а тиоэфиры 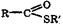 , где R и R' - углеводородные радикалы. Названия сложных эфиров строятся из названий исходных кислоты и спирта. По систематической номенклатуре общее название сложных эфиров - алкилалканоаты.
, где R и R' - углеводородные радикалы. Названия сложных эфиров строятся из названий исходных кислоты и спирта. По систематической номенклатуре общее название сложных эфиров - алкилалканоаты.
Алкил алкан оат
 |  |  |
название алкильного название фрагмента суффикс, указывающий на
фрагмента исходного карбоновой кислоты принадлежность вещества
спирта к классу сложных эфиров
Сложные эфиры широко распространены в живой природе. Многие из них входят в состав цветов, ягод и фруктов, определяя их аромат (табл. 13), и используются в пищевой и парфюмерной промышленности. Тиоэфиры также отличает резкий запах, но очень неприятный, который обнаруживается уже в ничтожных концентрациях.
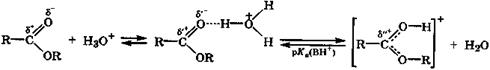
Сложные эфиры, подобно карбоновым кислотам, образуют ассоциат с ионом гидроксония, который в очень кислой среде (> 50 % H2SO4) превращается в катион эфира (рК 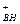 = -5 ÷ -7):
= -5 ÷ -7):
|
δ''+ > δ'+ > δ+ ассоциат эфира катион эфира
с Н3О+
В результате этих процессов происходит активация электрофильного центра на углеродном атоме карбонильной группы сложного эфира, по которому протекают реакции нуклеофильного замещения: гидролиз и ацилирование.
Таблица 13
Дата добавления: 2019-09-30; просмотров: 663;











