Кислоты и щелочи. Органические соединения
Все вещества - либо кислотные, либо щелочные, либо нейтральные. Точную степень этого можно измерить с использованием шкалы pH. Нейтральные вещества имеют pH, равный 7, pH кислот ниже 7, а у щелочей - выше 7.
Кислоты. Кислота растворяется в воде с образованием ионов водорода. Атомы водорода в молекуле соединения отделяются от других атомов в виде положительно заряженных ионов (Н+).
Когда газообразный хлорид водорода (НСІ) растворяется в воде, атомы водорода и хлора разделяются, образуя положительно заряженные ионы водорода (Н+) и отрицательно заряженные ионы хлора (СГ), содержащиеся в растворе соляной кислоты.
Доля молекул кислоты, диссоциирующих подобным образом, определяет ее силу. Сильной кислотой, например, является азотная (HN03), используемая в производстве удобрений и взрывчатых веществ. Слабые кислоты включают уксусную кислоту (СН3С02Н), содержащуюся в уксусе, и лимонную кислоту (C6H607), которая придает характерный вкус лимонам, грейпфрутам и другим цитрусовым.
Основания. Основания можно рассматривать как противоположность кислотам. Это группа соединений, которые реагируют с ионами водорода, даваемыми кислотами, и нейтрализуют их. Если основание растворимо в воде, оно называется щелочью.
Когда основание нейтрализует кислоту, продуктом реакции являются соль и вода. Например, при смешении хлористоводородной кислоты (HCI) с гидроксидом калия (КОН) получаются хлорид калия плюс вода:
![]()
Щелочи. Щелочи - это основания, которые, растворяясь в воде, дают гидроксильные ионы (ОН-). Пример - каустическая сода (NaOH), ее используют в производстве мыла и бумаги. При растворении в воде молекула диссоциирует с образованием положительно заряженного иона натрия (Na+) и отрицательно заряженного гидроксильного иона (ОН-). Сила щелочи определяется тем, сколько ее молекул диссоциирует подобным образом с образованием гидроксильных ионов.
Одно из свойств щелочей - способность превращать масла и жиры в растворимые мыла, которые легко отмываются. Поэтому их применяют в различных очистителях.
Органические соединения. Углерод является уникальным элементом, поскольку его атомы могут соединяться друг с другом в длинные цепи и кольца. Многие из этих соединений были впервые открыты в живых организмах, поэтому их изучением занимается органическая химия. Топливо, пластмассы и искусственные волокна тоже относят к органическим, поскольку молекулы включают кольца и цепи углеродных атомов.
Углеводороды содержат только атомы углерода и водорода. Их используют главным образом как топливо или сырье для производства пластмасс, волокон, резины.
Алифатические соединения. В них атомы углерода соединены в цепи. Они группируются в классы на основании структур молекул.
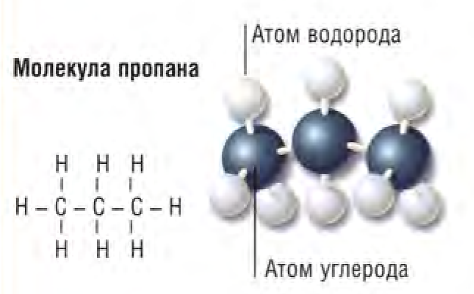
Алканы имеют одинарные связи между атомами углерода. Простейший алкан - метан (СН4); природный газ на 99% состоит из него. Другие алканы также служат топливом: этан (С2Н6), пропан (С3Н8) и бутан (С4Н10).
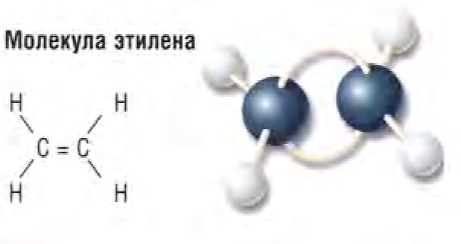
Алкены имеют не менее одной двойной связи между атомами углерода: этилен (С2Н4), пропилен (С3Н6) и бутен (С4Н8). В процессе полимеризации двойные связи молекул алкенов могут разрываться, что позволяет многим молекулам соединиться с образованием одной очень большой молекулы. Подобным образом получают многие пластмассы, например полиэтилен.
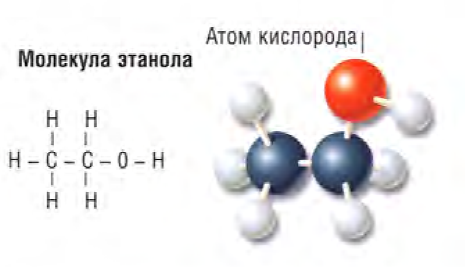
Спирты содержат одну или более гидроксильных групп (-ОН). К ним относится этанол (С2Н5ОН), содержащийся в алкогольных напитках. Он получается при ферментации (сбраживании) дрожжей. Этанол применяется также как растворитель.
Ароматические соединения. Органические соединения, молекулы которых содержат фрагмент из шести углеродных атомов, соединенных в кольцо, называемое ароматическим. Это название обусловлено тем, что группа подобных соединений, выделенная из каменноугольной смолы, обладала характерным сильным запахом.
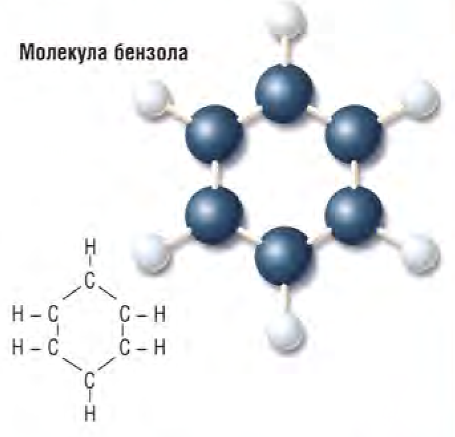
Простейший ароматический углеводород - бензол (С6Н6). В некоторых ароматических соединениях атомы водорода в бензольном кольце замещены другими атомами или химическими группами, например карболовая кислота.
Крекинг. Длинноцепочечные углеводородные молекулы превращаются в более короткие в химическом процессе, называемом крекингом. Например, сырая нефть содержит много непригодных для прямого использования углеводородов. Они расщепляются при нагревании.
Дата добавления: 2022-12-02; просмотров: 6587;











