Реакции нуклеофилъного замещения у тетрагонального атома
углерода (SN)
Субстраты: спирты и галогенопроизводные Условия: водные растворы
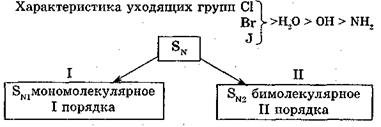
I. Механизм SN1 —замещение нуклеофильное, мономолекулярное I порядка.
Субстраты: третичные галогенопроизводные, у которых прямая атака нуклеофильными реагентами затруднена из-за наличия стерического эффекта заместителей.— пространственные затруднения.
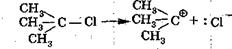
|
1-я стадия - образование карбокатиона в результате медленной диссоциации субстрата:
|
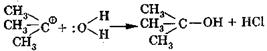
2-я стадия: атака нуклеофильной частицей (НОН) протекает мгновенно:
карбокатион третичный спирт
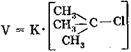 , поэтому реакция I порядка , поэтому реакция I порядка
|
Скорость реакции:
II. Механизм SN2- бимолекулярное нуклеофильное замещение II порядка.
Субстраты: первичные галогенопроизводные и первичные спирты, атака нуклеофильными реагентами субстрата не затруднена.
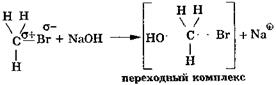
|
1-я стадия — нуклеофильный реагент атакует положительную часть молекулы с тыла (т. е. со стороны, противоположной галогену) с образованием промежуточного, переходного комплекса, в котором старые связи еще полностью не разорвались, а новые еще полностью не образовались:
2-я стадия:согласованно протекает разрыв старых (ковалентных) связей и образованиеновых:
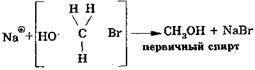
|
Скорость в SN2 определяется по формуле: V=K-[CH3Br]·[NaOH], поэтому это реакция II порядка. Если изменить условия протекания этих реакций: вместоводных растворов взять безводные спиртовые растворы сильных щелочей, то с этими же субстратами пойдут конкурирующие реакции — реакции отщепления (элиминирования) —Е1 и Е2.
Реакции нуклеофильного замещения происходят только в том случае, если уходящая группа стабильнее вступающей.
Хорошоуходящие группы — это такие группы, протонированные формы которых соответствуют сильным кислотам, например:  (протонированные формы: галогеноводородные кислоты HHal, ионы: гидроксония
(протонированные формы: галогеноводородные кислоты HHal, ионы: гидроксония 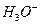 , алкилоксония
, алкилоксония 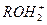 , аммония
, аммония 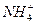 — сильные кислоты).
— сильные кислоты).
Плохоуходящие группы — это такие группы, протонированные формы которых соответствуют слабым кислотам, например:
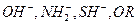 и др. В этом случае для протекания реакции необходимо протонирование, т.е. кислотный катализ, что позволит перевести плохоуходящую группу в хорошоуходящую:
и др. В этом случае для протекания реакции необходимо протонирование, т.е. кислотный катализ, что позволит перевести плохоуходящую группу в хорошоуходящую:
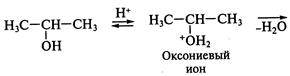

На последней (быстрой) стадии реакции происходит конкуренция за карбкатион между двумя частицами: галогенид-ионом (если в качестве кислоты использовали галогеноводородную кислоту) и молекулой воды, выступающей в роли акцептора протона. В первом случае происходит нуклеофильное замещение ( 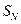 ) гидроксила на галоген, а во втором — элиминирование (Е) — отщепление протона.
) гидроксила на галоген, а во втором — элиминирование (Е) — отщепление протона.
§ 3.3.3. Реакции элиминирования(Е1 и Е2).
(Самостоятельная работа студентов)
Механизм E1 (отщепление молекулярное, I порядка).
Субстраты: третичные спирты, третичные галогенопроизводные.
Условия:
Катализатор - конц. H2SO4
1-я стадия — протонирование субстрата, преследует 2 цели:
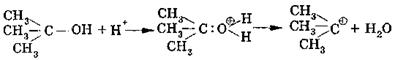
|
(1) образование карбокатиона и (2) образование хорошей уходящей группы (НОН >ОН):
третичный спирт карбокатион
2-я стадия — образовавшийся карбокатион не стабилен, поэтому стабилизацияегопроисходит за счет выброса протона (H+):
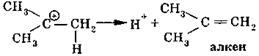
|
В результате реакции третичные спирты, отщепляя воду [Е], превращаются в непредельные углеводороды — алкены.
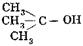
|
Скорость реакции:
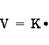
|
поэтому это отщепление I порядка (Е1) (реакции I порядка)
Б) Механизм Е2 (отщепление бимолекулярное, второго порядка)
Субстраты: первичные спирты, галогенопроизводные Условия — безводные, спиртовые растворы сильной щелочи.
1-я стадия — атака ОН-группой водорода, стоящего в β-положении с образованием переходного комплекса:
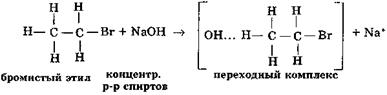
|
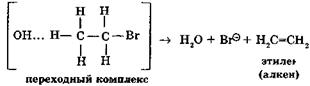
|
2-я стадия — далее реакция смещается в сторону образования молекулы Н2О, так как в окружающей среде нет Н2О (безводные, спиртовые растворы NaOH) (это кинетический контроль реакции), а с другой стороны идет образование Н2О как более термодинамически устойчивой частицы (термодинамический контроль реакции):
а)
б) Na+ + Br- → Na Br
Атаку ОН– группой водорода в β-положении (β-элиминирование) легко объяснить смещением реакции в сторону образования более термодинамически устойчивого кар-бокатиона, чем это имело бы место при α-элиминировании.
Дата добавления: 2019-09-30; просмотров: 787;











