III. Окислительно-восстановительные реакции
1) Окисление фенолов протекает очень легко даже под действием кислорода воздуха при комнатной температуре (этим объясняется появление окраски). Различными окислителями фенолы окисляются до разных состояний.
| 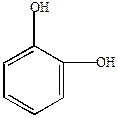
|
O
 H2O + H2O +
| 
| ||
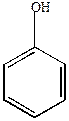
| + O | 
| пирокатехин | о-бензохинон | |

| 
|
O
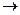 H2O + H2O +
| 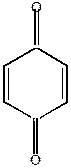
|
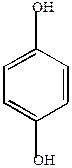
гидрохинон п-бензохинон
Гидрохинон и пирокатехин восстанавливают Ag из его соединений – применяются в фотографии как проявители.
а) окисление пространственно затрудненных (экранированных) фенолов приводит к образованию устойчивых свободных радикалов – ароксилов,
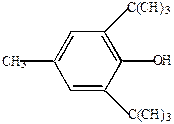
|
+ HO-OH 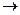 2 H2O + 2 H2O +
| 
|
| 4-метил-2,6-дитретбутилфенол (ионол) |
в которых электронное облако неспаренного электрона вступает в сопряжение с 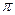 -электронами ароматического кольца, чему способствует наличие 3-х электронодонорных алкильных групп и
-электронами ароматического кольца, чему способствует наличие 3-х электронодонорных алкильных групп и 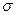 -р сопряжение ядра с метильной группой. Радикал приобретает стабильность и в отсутствие воздуха может существовать в свободном состоянии.
-р сопряжение ядра с метильной группой. Радикал приобретает стабильность и в отсутствие воздуха может существовать в свободном состоянии.
Этим свойством обусловлено использование экранированных фенолов в качестве ингибиторов окислительных процессов (антиоксидантов).
При добавлении небольших количеств экранированных фенолов в массу полимера они предупреждают развитие цепной реакции окисления, связывая образующиеся свободные радикалы полимера.
| RO . + | 
|
 ROH + ROH +
| 
|
| перекисный радикал полимера | ароксил |
Ароксил не способен продолжать цепной реакции, но может связать еще один радикал, превращаясь при этом в соединения хиноидного типа.

|
+ R. 
| 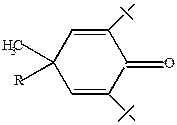
|
2) Восстановление фенолов.
Протекает трудно.
а) При перегонке в присутствии Zn-пыли фенол восстанавливается до углеводорода.
C6H5OH + Zn  ZnO + C6H6
ZnO + C6H6
б) действие водорода в присутствии катализатора группу ОН не затрагивает (гидрируется ядро), т.е.
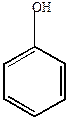
| Ni
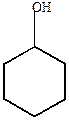
+ 3 H2 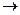
| 
|
| циклогексанол |
Дата добавления: 2020-10-14; просмотров: 897;











