Обратимые (двусторонние) реакции
Обратимыесостоят из прямой и обратной реакций, протекающих с разными скоростями.
Для реакций первого порядка они имеют вид:
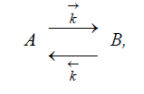
где 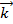 и
и 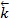 - константы скоростей соответственно прямой и обратной элементарных реакций. Понятие обратимые реакции в кинетике и термодинамике отличаются. В термодинамике в обратимой реакции скорости прямой обратной реакций должны быть равны. Кинетически обратимые – это реакции, протекающие в прямом и обратном направлениях с соизмеримыми, но разными скоростями, в связи с чем в химической кинетике вместо обратимые часто применяют термин двухсторонние реакции. Скорость обратимой реакции w равна разности скоростей прямой
- константы скоростей соответственно прямой и обратной элементарных реакций. Понятие обратимые реакции в кинетике и термодинамике отличаются. В термодинамике в обратимой реакции скорости прямой обратной реакций должны быть равны. Кинетически обратимые – это реакции, протекающие в прямом и обратном направлениях с соизмеримыми, но разными скоростями, в связи с чем в химической кинетике вместо обратимые часто применяют термин двухсторонние реакции. Скорость обратимой реакции w равна разности скоростей прямой 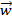 и обратной
и обратной 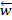 элементарных реакций:
элементарных реакций:
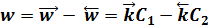 -
-
где С1 и С2 - концентрации соответственно веществ А и В в текущий момент времени τ.
Кинетические кривые для обратимых реакций первого порядка приведены на рис.:
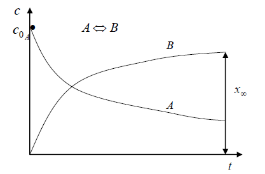
Рис. Зависимость концентрации реагента и продукта от времени для обратимой реакции первого порядка при k >1
Дата добавления: 2021-02-19; просмотров: 518;











