РАСТВОРИМОСТЬ ГАЗОВ И ТВЁРДЫХ ВЕЩЕСТВ В ЖИДКОСТЯХ
Рассмотрим растворимость газов и твердых веществ в жидкостях в случае образования идеальных растворов.
1). Растворимость твердых веществ (например, солей) в жидкостях. Растворение при постоянной температуре происходит до тех пор, пока не образуется насыщенный раствор (когда кристаллы твердого вещества присутствуют в растворе, однако количество растворившегося вещества и перешедшего в твердую фазу за единицу времени одинаково). Устанавливается равновесие “твердый компонент – насыщенный раствор”, при котором
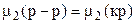 , (20)
, (20)
где m2 — химический потенциал вещества в растворе и в кристаллической фазе.
Можно показать, что при образовании идеального раствора
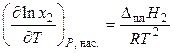 , (21)
, (21)
где x2 — мольная доля растворенного вещества в насыщенном растворе, DплН2 — энтальпия плавления этого вещества. Уравнение (5.21) было впервые выведено русским физико-химиком И.Ф. Шредером и с тех пор носит его имя как уравнение Шредера.
Уравнение (5.21) можно преобразовать:
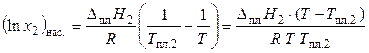 , (22)
, (22)
где Тпл.2 — температура плавления чистого кристаллического вещества.
Из уравнений (21) и (22) следует, что
— чем выше температура, тем больше растворимость твердых веществ в жидкостях, так как DплН2 > 0;
— чем выше температура плавления и теплота плавления твердых веществ, тем меньше их растворимость в жидкостях.
Растворимость твердых тел в жидкостях зависит также от давления и эту зависимость надо учитывать, особенно в геологии, где имеют дело с сотнями и тысячами атмосфер. Для идеальных растворов эта зависимость определяется уравнением Планка-Ван-Лаара:
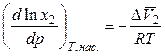 , (23)
, (23)
где 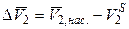 — разность парциальных мольных объёмов растворенного вещества в растворе и твердой фазе.
— разность парциальных мольных объёмов растворенного вещества в растворе и твердой фазе.
2. Растворение газов в жидкостях. Рассмотрим случай, когда растворитель нелетуч или малолетуч. При образовании насыщенного раствора устанавливается равновесие «газ – насыщенный раствор». Тогда
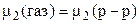 . (24)
. (24)
Можно показать, что
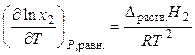 , (25)
, (25)
где Dраств.H2 < 0 — энтальпия растворения газа (или энтальпия конденсации газа). Следовательно, повышение температуры приводит к уменьшению растворимости газов. При растворении газов не в чистых растворителях, а в растворах, увеличение концентрации солей также уменьшает растворимость газа, так как при этом уменьшается значение Dраств.H2.
На растворимость газа в жидкости оказывает влияние и давление газа:
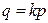 , (26)
, (26)
где q — растворимость газа, р — давление газа. Коэффициент пропорциональности 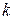 получил название коэффициента Генри, впервые систематически исследовавшего растворимость газов в жидкостях.
получил название коэффициента Генри, впервые систематически исследовавшего растворимость газов в жидкостях.
В гидрогеохимии часто используют другое уравнение, связывающее приведенный объём растворенного газа с (парциальным) давлением этого газа над раствором:
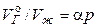 , (27)
, (27)
где 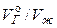 – приведенный к нормальным условиям (00С и 1атм) объём газа, растворенного в единице объёма (1л) жидкости. Коэффициент пропорциональности a получил название коэффициента абсорбции газа в жидкости или коэффициента Бунзена.
– приведенный к нормальным условиям (00С и 1атм) объём газа, растворенного в единице объёма (1л) жидкости. Коэффициент пропорциональности a получил название коэффициента абсорбции газа в жидкости или коэффициента Бунзена.
Дата добавления: 2016-06-18; просмотров: 2725;











