Растворы классифицируют
1). по степени дисперсности на
— истинные (молекулярные или атомные смеси компонентов);
— коллоидные (микрогетерогенные);
— тонкие механические взвеси (суспензии и эмульсии).
2). по агрегатному состоянию на
— газовые;
— жидкие;
— твёрдые.
3. с термодинамических позиций на
— идеальные;
— предельно разбавленые (С2 → 0);
— реальные.
Физическая химия изучает термодинамические и другие свойства растворов. Коллоидные растворы и тонкие механические взвеси являются предметом исследования коллоидной химии. Свойства растворителя обычно обозначаются индексом (1), а свойства растворенных веществ – индексами (2), (3) и т. д.
Способы выражения состава растворов.
Так как количество каждого компонента может быть представлено в различных единицах измерения, то и состав раствора можно выразить несколькими способами.
1). Через мольные (молярные) доли xi:
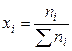 ,
, 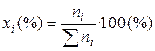 , (1)
, (1)
где ni – число молей i-го компонента в растворе.
2). Через объёмные доли ji:
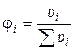 ,
,  , (2)
, (2)
где ui ‑ объём i-ого компонента в объёме раствора u.
3). Через массовые доли 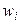 :
:
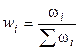 ,
, 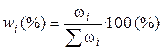 , (3)
, (3)
где ωi – масса i-ого компонента в растворе.
4). Через молярные концентрации (молярности) Сi:
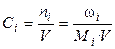 (моль/л), (4)
(моль/л), (4)
где ωi – масса i-го компонента (г), Мi – молярная масса i-ого компонента (г/моль), V – объём раствора (л), ni – число молей.
5). Через моляльные концентрации (моляльности) mi:
 (моль/кг). (5)
(моль/кг). (5)
Моляльность выражает число молей i-ого компонента (растворенного вещества) в расчете на 1 кг растворителя.
6) Через молярные концентрации эквивалента (эквивалентные концентрации, нормальности) – Сi или Ni:
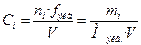 (моль·г-экв/л), (6)
(моль·г-экв/л), (6)
где фактор эквивалентности fэкв показывает, какая доля молярной массы данного вещества эквивалентна одному иону водорода в данной окислительно – восстановительной реакции.
Дата добавления: 2016-06-18; просмотров: 2147;











