I.2.2 ТЕПЛОЁМКОСТЬ ВЕЩЕСТВА
Теплоёмкостью 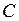 тела называется физическая величина, численно равная отношению количества теплоты
тела называется физическая величина, численно равная отношению количества теплоты  , сообщаемого телу, к изменению
, сообщаемого телу, к изменению 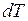 температуры тела в рассматриваемом термодинамическом процессе:
температуры тела в рассматриваемом термодинамическом процессе:
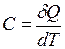 . (I.54)
. (I.54)
Значение теплоёмкости тела зависит от массы тела, его химического состава, термодинамического состояния и процесса, в котором сообщается теплота  .
.
Из определения теплоёмкости следует, что при адиабатном процессе, когда 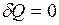 , теплоёмкость равна нулю.
, теплоёмкость равна нулю.
При изотермическом процессе 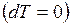 понятие теплоёмкости не имеет смысла (
понятие теплоёмкости не имеет смысла (  ).
).
Удельной теплоёмкостью вещества сназывается физическая величина, равная количеству теплоты, необходимому для нагревания 1 кг вещества на 1 К
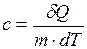 . (I.55)
. (I.55)
Или другое определение удельной теплоёмкости.
Удельной теплоёмкостью вещества называется теплоёмкость единицы массы вещества. Для однородного тела
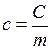 , (I.56)
, (I.56)
где 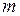 – масса вещества.
– масса вещества.
Молярной теплоёмкостью вещества 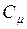 называется физическая величина, равная количеству теплоты, необходимому для нагревания 1 моля вещества на 1 К
называется физическая величина, равная количеству теплоты, необходимому для нагревания 1 моля вещества на 1 К
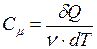 , (I.57)
, (I.57)
где 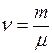 – количество вещества, выражающее число молей.
– количество вещества, выражающее число молей.
Или молярной (мольной) теплоёмкостью называется теплоёмкость одного моля вещества
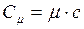 , (I.58)
, (I.58)
где 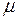 – молярная масса вещества.
– молярная масса вещества.
Различают теплоёмкости при постоянном объёме и постоянном давлении, если в процессе нагревания вещества его объём или давление поддерживаются постоянным.
Молярная теплоёмкость газа при постоянном объёме 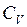
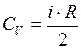 , (I.59)
, (I.59)
где 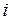 – число степеней свободы молекулы;
– число степеней свободы молекулы;
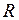 – универсальная (молярная) газовая постоянная.
– универсальная (молярная) газовая постоянная.
Молярная теплоёмкость газа при постоянном давлении 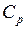
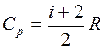 . (I.60)
. (I.60)
Молярные теплоёмкости газа 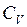 и
и 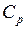 связаны уравнением Майера
связаны уравнением Майера
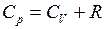 . (I.61)
. (I.61)
Уравнение (I.61), показывает, что 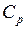 всегда больше
всегда больше 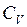 на величину молярной газовой постоянной. Это объясняется тем, что при нагревании газа при постоянном давлении требуется ещё дополнительное количество теплоты на совершение работы расширения газа, так как постоянство давления обеспечивается увеличением объёма газа.
на величину молярной газовой постоянной. Это объясняется тем, что при нагревании газа при постоянном давлении требуется ещё дополнительное количество теплоты на совершение работы расширения газа, так как постоянство давления обеспечивается увеличением объёма газа.
При рассмотрении термодинамических процессов важно знать характерное для каждого газа отношение 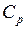 к
к 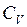
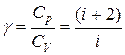 , (I.62)
, (I.62)
где 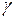 – безразмерная величина, называемая коэффициентом Пуассона (показатель адиабаты).
– безразмерная величина, называемая коэффициентом Пуассона (показатель адиабаты).
Из формул (I.59) и (I.60) следует, что молярные теплоёмкости определяются лишь числом степеней свободы и не зависят от температуры.
Дата добавления: 2016-09-06; просмотров: 5145;











