Синаптическая интеграция: механизмы пространственной и временной суммации возбуждающих и тормозных постсинаптических потенциалов
В большинстве нейронов одного возбуждающего синаптического события недостаточно для достижения порога генерации потенциала действия в постсинаптическом нейроне. Например, один возбуждающий постсинаптический потенциал (ВПСП, EPSP) может составлять всего 0,5 мВ, тогда как для деполяризации мембраны до порогового значения требуется изменение примерно на 15 мВ. Следовательно, потенциал действия может быть инициирован только при совместном воздействии многих одновременно активных возбуждающих синапсов. Это фундаментальное свойство нейронных сетей обеспечивает пороговый характер передачи сигнала и предотвращает случайное срабатывание клеток.
Из тысяч синапсов, присутствующих в типичном нейроне, сотни могут быть активны одновременно или в течение достаточно короткого интервала времени, чтобы их эффекты суммировались. Таким образом, мембранный потенциал постсинаптического нейрона в любой момент времени представляет собой интегральный результат всей текущей синаптической активности. Когда преобладает возбуждающий сигнал, мембрана деполяризуется до порогового уровня; когда доминирует тормозной сигнал, происходит либо гиперполяризация, либо стабилизация мембранного потенциала, что снижает вероятность генерации ответа. Этот динамический баланс лежит в основе всех вычислительных процессов в центральной нервной системе.
Экспериментальная демонстрация взаимодействия ВПСП и ТПСП. Простой эксперимент (рис. 6.31) наглядно демонстрирует, как взаимодействуют EPSP и тормозные постсинаптические потенциалы (ТПСП, IPSP). Предположим, что постсинаптическая клетка имеет три синаптических входа: аксоны A и B образуют возбуждающие синапсы, а аксон C — тормозной синапс. Стимуляторы на аксонах A, B и C обеспечивают их индивидуальную активацию, а внутриклеточный электрод в теле клетки регистрирует изменения мембранного потенциала. В части 1 эксперимента при двух последовательных стимуляциях аксона A взаимодействия между двумя EPSP не наблюдается, поскольку постсинаптический потенциал является кратковременным (как и все градуированные потенциалы): в течение нескольких миллисекунд клетка возвращается в состояние покоя.
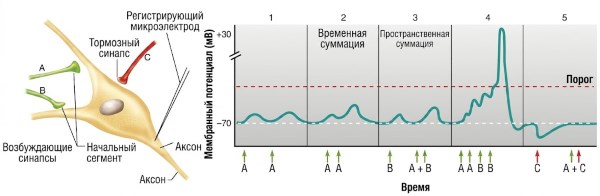
Рисунок 6.31. Взаимодействие EPSP и IPSP в постсинаптическом нейроне. Пресинаптические нейроны (А–С) стимулировались в моменты, указанные стрелками, а результирующий мембранный потенциал регистрировался в постсинаптической клетке с помощью микроэлектрода.
В части 2 эксперимента вторая стимуляция аксона A происходит до того, как первый EPSP затухает, в результате чего второй синаптический потенциал добавляется к предыдущему, вызывая бóльшую деполяризацию. Это явление называется временной суммацией (темпоральной суммацией), поскольку входные сигналы поступают от одной и той же пресинаптической клетки, но в разные моменты времени. Суммирование происходит благодаря дополнительному притоку положительных ионов до того, как ионы, выходящие через мембрану, восстановят потенциал покоя. Временная суммация особенно эффективна при высокой частоте разряда пресинаптического нейрона.
Часть 3 на рис. 6.31 сначала демонстрирует стимуляцию одиночного аксона B для определения его изолированного ответа, а затем — одновременную стимуляцию аксонов A и B. EPSP от двух разных нейронов также объединяются в постсинаптическом нейроне, что приводит к более выраженной деполяризации. Хотя для суммирования две стимуляции должны происходить в близкие временные интервалы, этот феномен называется пространственной суммацией (пространственной суммацией), поскольку входные сигналы поступают из разных участков клетки. Благодаря пространственной и временной суммации множественные EPSP могут увеличить суммарный приток положительных ионов и довести постсинаптическую мембрану до порогового значения, тем самым инициируя потенциалы действия (см. часть 4 рисунка 6.31). В реальных нейронных сетях оба типа суммации действуют одновременно.
Взаимодействие возбуждающих и тормозных сигналов. До сих пор были рассмотрены только паттерны взаимодействия возбуждающих синапсов. Поскольку EPSP и IPSP возникают за счет противоположно направленных локальных токов, они, как правило, нейтрализуют друг друга, практически не вызывая изменения мембранного потенциала при одновременной стимуляции A и C (рис. 6.31, часть 5). Тормозные потенциалы также способны к временной и пространственной суммации, что позволяет им эффективно подавлять деполяризацию. Этот механизм шунтирующего торможения играет критическую роль в регуляции возбудимости нейронов и предотвращении избыточной активности в нейронных цепях.
В зависимости от сопротивления постсинаптической мембраны и величины заряда, проходящего через лиганд-управляемые ионные каналы, синаптический потенциал распространяется по плазматической мембране в большей или меньшей степени. Во время активации возбуждающего синапса обширная область мембраны становится слабо деполяризованной; при активации тормозного синапса она становится слабо гиперполяризованной или стабилизированной, хотя эти градуированные потенциалы затухают по мере удаления от синаптического контакта (рис. 6.32). Сигналы от нескольких синапсов могут суммироваться, потенциально вызывая потенциал действия в аксонном холмике или начальном сегменте.
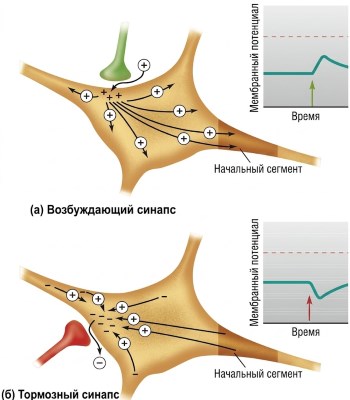
Рисунок 6.32. Сравнение возбуждающих и тормозных синапсов, показывающее направление тока через постсинаптическую клетку после синаптической активации. (а) Ток, проходящий через постсинаптическую клетку, направлен от возбуждающего синапса и может деполяризовать начальный сегмент. (б) Ток, проходящий через постсинаптическую клетку, направлен к тормозному синапсу и может вызвать гиперполяризацию начального сегмента. Стрелка на графике указывает момент возникновения стимула.
Роль начального сегмента и пространственного расположения синапсов. В предыдущих примерах порог постсинаптического нейрона описывался как единый для всей клетки, но разные компартменты имеют различные пороговые значения. В целом, начальный сегмент аксона (или аксонный холмик) обладает более отрицательным порогом (то есть расположен гораздо ближе к потенциалу покоя), чем мембрана тела клетки и дендритов. Этот более низкий порог обусловлен более высокой плотностью потенциал-зависимых Na⁺-каналов в данной области. Следовательно, начальный сегмент наиболее чувствителен к небольшим изменениям мембранного потенциала, возникающим вследствие синаптического влияния на тело клетки и дендриты. Когда накапливается достаточное количество EPSP, начальный сегмент достигает порога, и результирующий потенциал действия распространяется от этой точки вниз по аксону.
Тот факт, что начальный сегмент обычно имеет самый низкий порог, объясняет, почему расположение отдельных синапсов на постсинаптической клетке имеет решающее значение. Синапс, находящийся вблизи начального сегмента, вызывает там большее изменение напряжения, чем синапс на самой дистальной ветви дендрита, поскольку он обеспечивает больший локальный ток в начальном сегменте. Однако в некоторых нейронах сигналы от дендритов, удаленных от начального сегмента, могут усиливаться благодаря наличию в этих дендритных областях потенциал-зависимых Na⁺-каналов, которые генерируют дендритные потенциалы действия и усиливают дистальные входы. Такая компартментализация обеспечивает сложную вычислительную мощность отдельных нейронов.
Генерация серий потенциалов действия. Постсинаптические потенциалы сохраняются намного дольше, чем потенциалы действия (миллисекунды против микросекунд). Если накопленные EPSP удерживают начальный сегмент деполяризованным выше порога после завершения предыдущего потенциала действия и окончания периода рефрактерности, возникает второй потенциал действия. Более того, пока мембрана остается деполяризованной до порогового уровня, потенциалы действия продолжают генерироваться с частотой, пропорциональной степени надпороговой деполяризации. Таким образом, нейронные реакции почти всегда проявляются в виде залпов (пачек) потенциалов действия, а не в виде единичных изолированных событий. Эта тоническая активность лежит в основе кодирования интенсивности стимула и передачи информации в нейронных сетях. Понимание механизмов синаптической суммации и интеграции имеет фундаментальное значение для нейробиологии, клинической неврологии и разработки нейропротезов.
Сведения об авторах и источниках:
Авторы: Эрик П. Видмайер, Бостонский университет, Хершел Рафф, Медицинский колледж Висконсина, Медицинский центр Авроры Сент-Люк, Кевин Т. Странг, Университет Висконсин-Мэдисон
Источник: Физиология человека: механизмы функционирования организма
Данные публикации будут полезны студентам биологических и медицинских специальностей, начинающим специалистам в области клеточной биологии, биофизики и физиологии, а также всем, кто интересуется основами мембранного транспорта и регуляции клеточного гомеостаза.
Дата добавления: 2026-04-29; просмотров: 94;











