Механизмы высвобождения нейромедиаторов и синаптической передачи: возбуждающие и тормозные постсинаптические потенциалы
Как показано на рисунке 6.27, а, нейромедиаторы (нейротрансмиттеры) хранятся в небольших синаптических везикулах — пузырьках, окруженных липидным бислоем. До активации нейрона часть везикул закрепляется в специализированных участках пресинаптической мембраны, называемых активными зонами, тогда как другие остаются распределенными в терминале. Высвобождение нейромедиатора инициируется при достижении потенциала действия пресинаптической терминальной мембраны. Ключевой особенностью химических синаптических окончаний является наличие потенциал-зависимых Ca²⁺-каналов наряду с Na⁺- и K⁺-каналами, характерными для других участков нейрона. Деполяризация во время потенциала действия открывает эти Ca²⁺-каналы, и благодаря электрохимическому градиенту ионы кальция устремляются в окончание аксона.
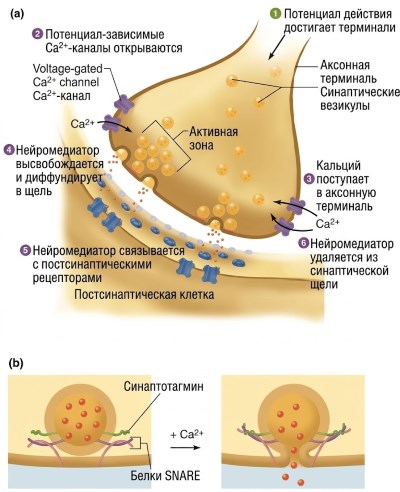
Рисунок 6.27. (а) Механизмы передачи сигналов в химическом синапсе. (б) Увеличенное изображение, показывающее детали высвобождения нейромедиаторов. Ионы кальция активируют синаптотагмин и белки SNARE, вызывая слияние мембран и высвобождение нейромедиаторов. (SNARE — растворимый N-этилмалеимид-чувствительный фактор прикрепления, рецепторный белок).
Ионы кальция активируют процессы, приводящие к слиянию пристыкованных везикул с синаптической терминальной мембраной (рис. 6.27, б). До прихода потенциала действия везикулы слабо закреплены в активных зонах благодаря взаимодействиям между SNARE-белками (растворимыми белковыми рецепторами, чувствительными к N-этилмалеимид-фактору прикрепления), часть которых встроена в мембрану везикулы, а другая часть — в терминальную мембрану. Поступающие при деполяризации ионы Ca²⁺ связываются с синаптотагминами — семейством белков, ассоциированных с везикулами, что вызывает конформационные изменения в комплексе SNARE, инициирует слияние мембран и высвобождение нейромедиатора. После слияния везикулы могут претерпевать две возможные судьбы: в одних синапсах они полностью сливаются и позже рециркулируют путем эндоцитоза из участков мембраны за пределами активной зоны (см. рис. 4.21). В других синапсах, особенно при высокой частоте потенциалов действия, везикулы способны на короткое время сливаться, высвобождать содержимое, закрывать пору и возвращаться в окончание аксона с помощью механизма, называемого «слиянием по принципу "целуй и убегай"» (kiss-and-run).
После высвобождения из пресинаптического окончания нейромедиаторы диффундируют через синаптическую щель и взаимодействуют с постсинаптической клеткой. Часть молекул нейромедиатора связывается с рецепторами на постсинаптической плазматической мембране. Активированные рецепторы могут быть ионотропными (непосредственно функционирующими как ионные каналы, как показано на рис. 6.15) или метаботропными (опосредованно влияющими на ионные каналы через G-белки и/или вторичные мессенджеры). В любом случае связывание нейромедиатора приводит к открытию или закрытию специфических лиганд-управляемых ионных каналов в постсинаптической мембране, что в итоге изменяет мембранный потенциал. Вследствие последовательности событий между приходом потенциала действия на пресинаптическое окончание и результирующим изменением постсинаптического потенциала возникает кратковременная синаптическая задержка, составляющая приблизительно 0,2 миллисекунды.
Связывание нейромедиатора с рецепторами является временным и обратимым процессом, существующим в равновесии между связанной и несвязанной формами. По мере снижения концентрации свободного нейромедиатора в синаптической щели количество занятых рецепторов пропорционально уменьшается. Когда нейромедиаторы перестают связываться, ионные каналы в постсинаптической мембране возвращаются в состояние покоя. Эта обратимость обеспечивает точный временной контроль синаптической передачи сигналов, что критически важно для нормальной работы нейронных сетей.
Удаление нейромедиатора из синапса. Пресинаптические клетки обычно выделяют большое количество нейромедиатора, чтобы увеличить вероятность его связывания с постсинаптическими рецепторами. Однако несвязанные нейромедиаторы должны быть удалены для прекращения сигнала и предотвращения его распространения на соседние клетки, где они могут вызвать нежелательные эффекты. Несвязанные нейромедиаторы выводятся из синаптической щели с помощью четырех основных механизмов: (1) активный перенос обратно в пресинаптическое окончание аксона для повторного использования (обратный захват); (2) перенос в близлежащие глиальные клетки для деградации; (3) диффузия из рецепторной области; (4) ферментативное превращение в неактивные вещества, некоторые из которых транспортируются обратно в пресинаптическое окончание для повторного использования. Ферменты, участвующие в ферментативной трансформации, могут располагаться на постсинаптической мембране, пресинаптической мембране или внутри синаптической щели.
Возбуждающие химические синапсы. Два типа химических синапсов — возбуждающие и тормозные — различаются по их воздействию на постсинаптическую клетку, которое зависит от ионных каналов, активируемых связыванием нейромедиатора. В возбуждающем химическом синапсе постсинаптический ответ представляет собой деполяризацию, приближающую мембранный потенциал к пороговому значению. Обычный эффект активированных рецепторов в таких синапсах заключается в открытии неселективных каналов, проницаемых как для Na⁺, так и для K⁺. Электрический градиент и градиент концентрации приводят к поступлению Na⁺ в клетку, тогда как для K⁺ электрический градиент противостоит градиенту концентрации (см. рис. 6.12).
Открытие каналов, проницаемых для обоих ионов, приводит к одновременному перемещению относительно небольшого количества ионов калия из клетки и большего количества ионов натрия внутрь клетки. Суммарное перемещение положительных ионов в постсинаптическую клетку вызывает небольшую деполяризацию, известную как возбуждающий постсинаптический потенциал (ВПСП, EPSP) (рис. 6.28). EPSP представляет собой деполяризующий градуированный потенциал, величина которого уменьшается по мере удаления от синапса благодаря локальному току. Его единственная функция заключается в приближении мембранного потенциала постсинаптического нейрона к порогу, что способствует генерации потенциала действия.
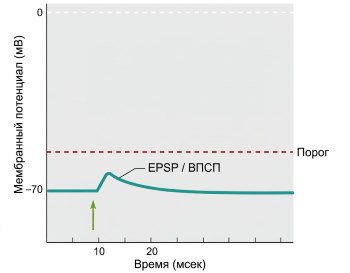
Рисунок 6.28. Возбуждающий постсинаптический потенциал (EPSP). Стимуляция пресинаптического нейрона отмечена зеленой стрелкой. (На рисунке показано увеличение масштаба: типичный EPSP составляет около 0,5 мВ).
Тормозные химические синапсы. В тормозных химических синапсах изменение постсинаптического потенциала обычно представляет собой гиперполяризующий градуированный потенциал, называемый тормозным постсинаптическим потенциалом (ТПСП, IPSP) (рис. 6.29). Как альтернатива, IPSP может быть неизмеримым, а скорее стабилизировать мембранный потенциал на существующем уровне. В любом случае активация тормозного синапса снижает вероятность того, что постсинаптическая клетка деполяризуется до порогового значения и сгенерирует потенциал действия. Таким образом, IPSP выполняют критическую роль в поддержании баланса возбуждения и торможения в ЦНС.
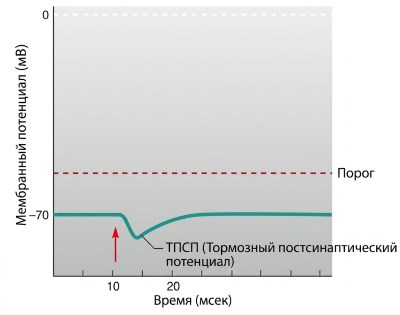
Рисунок 6.29. Тормозной постсинаптический потенциал (IPSP). Стимуляция пресинаптического нейрона отмечена красной стрелкой. (Эта гиперполяризация изображена крупнее, чем типичный IPSP).
В тормозном синапсе активированные рецепторы на постсинаптической мембране открывают Cl⁻- или K⁺-каналы, не влияя на проницаемость для Na⁺. В клетках, которые активно регулируют внутриклеточную концентрацию Cl⁻ посредством активного вывода хлорида из клетки, равновесный потенциал Cl⁻ более отрицательный, чем потенциал покоя. Следовательно, когда Cl⁻-каналы открываются, хлорид поступает в клетку, вызывая гиперполяризацию — IPSP. В клетках, которые не транспортируют Cl⁻ активно, равновесный потенциал хлорида равен потенциалу мембраны покоя; повышенная Cl⁻-проницаемость не изменяет мембранный потенциал, но усиливает стабилизирующее влияние хлорида, затрудняя изменение потенциала возбуждающими сигналами от других синапсов, когда хлоридные каналы одновременно открыты (рис. 6.30).
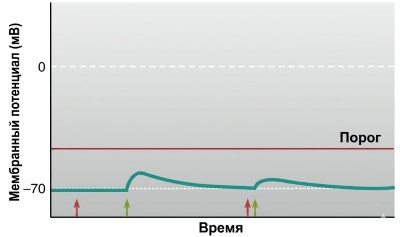
Рисунок 6.30. Синаптическое торможение постсинаптической клетки, при котором ECl равен мембранному потенциалу покоя. Стимуляция пресинаптического нейрона, высвобождающего нейромедиатор, который открывает Cl⁻-каналы (красные стрелки), не оказывает прямого влияния на потенциал постсинаптической мембраны. Однако, когда одновременно активируется возбуждающий синапс (зеленые стрелки), перемещение Cl⁻ в клетку уменьшает EPSP.
Повышенная проницаемость для K⁺ в постсинаптической клетке также вызывает IPSP. Если бы клеточная мембрана была проницаема только для K⁺, мембранный потенциал покоя равнялся бы равновесному потенциалу K⁺ (приблизительно -90 мВ вместо типичных -70 мВ). Таким образом, при повышении проницаемости для K⁺ больше ионов калия покидает клетку, приближая мембранный потенциал к равновесному потенциалу K⁺ и вызывая гиперполяризацию. Это еще больше снижает возбудимость нейрона, эффективно подавляя генерацию потенциала действия. В совокупности механизмы возбуждающих и тормозных синапсов обеспечивают тонкую регуляцию нейронной активности, лежащую в основе всех когнитивных и поведенческих процессов.
Сведения об авторах и источниках:
Авторы: Эрик П. Видмайер, Бостонский университет, Хершел Рафф, Медицинский колледж Висконсина, Медицинский центр Авроры Сент-Люк, Кевин Т. Странг, Университет Висконсин-Мэдисон
Источник: Физиология человека: механизмы функционирования организма
Данные публикации будут полезны студентам биологических и медицинских специальностей, начинающим специалистам в области клеточной биологии, биофизики и физиологии, а также всем, кто интересуется основами мембранного транспорта и регуляции клеточного гомеостаза.
Дата добавления: 2026-04-29; просмотров: 135;











