Нейромедиаторы и нейромодуляторы: классификация, механизмы действия и роль в регуляции нервной системы
Исследователи традиционно акцентируют внимание на роли нейротрансмиттеров в генерации возбуждающих постсинаптических потенциалов (ВПСП) и тормозных постсинаптических потенциалов (ТПСП). Однако определённые химические посредники инициируют сложные ответные реакции, которые невозможно однозначно классифицировать как ВПСП или ТПСП. Для описания таких интегративных эффектов используется термин «модуляция», а сигнальные молекулы, ответственные за эти процессы, получили название нейромодуляторов. Границы между нейромодуляторами и классическими нейротрансмиттерами зачастую размыты, поскольку многие нейромодуляторы синтезируются в пресинаптической клетке и высвобождаются совместно с традиционными медиаторами. Дополнительную сложность вносит тот факт, что многочисленные гормоны, паракринные факторы и компоненты иммунной системы также способны функционировать в качестве нейромодуляторов.
Нейромодуляторы преимущественно изменяют чувствительность постсинаптических клеток к определённым нейромедиаторам, тем самым усиливая или ослабляя эффективность текущей синаптической активности. Альтернативным механизмом является их влияние на синтез, высвобождение, обратный захват или ферментативный распад трансмиттера в пресинаптическом окончании. Таким образом, нейромодуляторы не вызывают непосредственного возбуждения или торможения, а модулируют общую результативность синаптической передачи. Эта регуляторная способность позволяет нейронным сетям адаптировать свои выходные сигналы в соответствии с физиологическими потребностями организма и сигналами внешней среды.
Рецепторы классических нейромедиаторов, как правило, воздействуют на ионные каналы, обеспечивая быстрое (в пределах миллисекунд) возбуждение или торможение постсинаптической клетки. Напротив, рецепторы нейромодуляторов чаще запускают метаболические каскады внутри нейрона, часто опосредованные G-белками и системами вторичных посредников. Такие изменения могут развиваться в течение минут, часов или даже дней и включают модуляцию ферментативной активности, а также, благодаря влиянию на транскрипцию ДНК, модификации синтеза белка. Следовательно, нейромедиаторы обеспечивают быструю синаптическую коммуникацию, тогда как нейромодуляторы участвуют в более медленных и устойчивых процессах, таких как обучение, развитие и формирование мотивационных состояний.
Перечень веществ, выполняющих функции нейромедиаторов или нейромодуляторов, весьма обширен и продолжает пополняться. Классификационная основа для этого списка представлена в таблице 6.6, однако её детальное обсуждение выходит за рамки данного обзора. В последующих разделах приведены фундаментальные обобщения о ключевых нейромедиаторах, причём термин «нейромедиатор» используется в широком смысле, с признанием того, что некоторые посредники более корректно описываются как нейромодуляторы. Важное терминологическое примечание: для обозначения нейронов часто применяется суффикс «-эргический», где отсутствующий префикс указывает на тип высвобождаемого нейромедиатора (например, дофаминергические нейроны выделяют дофамин).

Ацетилхолин (АХ). Ацетилхолин (АХ) служит основным нейромедиатором в периферической нервной системе (ПНС) – в нервно-мышечном соединении, где двигательный нейрон контактирует с клетками скелетных мышц, а также функционирует в головном мозге. Нейроны, секретирующие АХ, называются холинергическими. Тела холинергических нейронов головного мозга сконцентрированы в ограниченном числе областей, однако их аксоны широко распространяются по всей центральной нервной системе (ЦНС). Этот обширный проекционный паттерн лежит в основе разнообразных функций ацетилхолина, связанных с вниманием, памятью и мышечным контролем.
Синтез ацетилхолина происходит в цитоплазме синаптических окончаний из холина (распространённого пищевого нутриента) и ацетилкоэнзима А, после чего молекулы АХ накапливаются в синаптических пузырьках. После высвобождения и активации постсинаптических рецепторов концентрация АХ в синаптической щели снижается благодаря ферменту ацетилхолинэстеразе, который локализован как на пре-, так и на постсинаптической мембранах и быстро гидролизует АХ с образованием холина и ацетата. Освободившийся холин транспортируется обратно в пресинаптическое окончание для повторного использования при синтезе нового АХ. Некоторые виды химического оружия, например зарин, ингибируют ацетилхолинэстеразу, вызывая патологическое накопление АХ в синаптической щели, что приводит к чрезмерной стимуляции постсинаптических рецепторов, неконтролируемым мышечным сокращениям и последующему параличу.
Никотиновые рецепторы ацетилхолина. Хотя рецептор считается специфичным к определённому лиганду (например, к АХ), большинство рецепторов распознают природные или синтетические соединения, обладающие химическим сходством с этим лигандом. Часть АХ-рецепторов активируется не только ацетилхолином, но и алкалоидом никотином, поэтому они получили название никотиновых рецепторов. Никотин составляет 1–2% табачных изделий и также присутствует в средствах для прекращения курения (назальные спреи, жевательные резинки, пластыри). Благодаря гидрофобной структуре никотин быстро всасывается через капилляры лёгких, слизистые оболочки, кожу и гематоэнцефалический барьер.
Никотиновый рецептор представляет собой лиганд-управляемый ионный канал, проницаемый для ионов натрия и калия; однако, поскольку электрохимическая движущая сила для натрия больше, открытие канала приводит к деполяризации. Никотиновые рецепторы присутствуют в нервно-мышечных соединениях, и некоторые их антагонисты являются токсинами, вызывающими паралич. В головном мозге эти рецепторы играют важную роль в когнитивных функциях и поведении: например, одна из холинергических систем, использующая никотиновые рецепторы, усиливает способность обнаруживать значимые стимулы, что критически важно для внимания, обучения и памяти. Наличие никотиновых рецепторов на пресинаптических окончаниях в путях вознаграждения объясняет высокую зависимость от табачных изделий.
Мускариновые рецепторы ацетилхолина. Другой распространённый тип холинергических рецепторов стимулируется как ацетилхолином, так и мускарином (ядом, содержащимся в некоторых грибах); эти рецепторы называются мускариновыми. Они относятся к метаботропным рецепторам, взаимодействуют с G-белками и через них изменяют активность различных ферментов и ионных каналов. Мускариновые рецепторы преобладают в определённых холинергических синапсах головного мозга, а также в соединениях, где отделы ПНС иннервируют периферические железы, ткани и органы (слюнные железы, гладкомышечные клетки, сердце). Атропин – природный антагонист мускариновых рецепторов, широко применяемый в клинической практике, в том числе в виде глазных капель для расширения зрачков при офтальмологических обследованиях.
Болезнь Альцгеймера. У людей с болезнью Альцгеймера (возрастное заболевание мозга, наиболее частая причина снижения интеллекта у пожилых) наблюдается дегенерация многих холинергических нейронов головного мозга. Распространённость болезни составляет 10–15% среди лиц старше 65 лет и достигает 50% среди людей старше 85 лет. Вследствие дегенерации холинергических нейронов заболевание ассоциировано со снижением уровня АХ в определённых областях мозга и даже утратой постсинаптических нейронов, отвечающих на АХ. Эти дефекты наряду с нарушениями в других нейромедиаторных системах связаны со снижением языковых способностей, когнитивной дисфункцией, спутанностью сознания и потерей памяти – характерными симптомами болезни Альцгеймера.
Несколько генетических механизмов повышают риск развития заболевания; например, ген на 19-й хромосоме кодирует белок, участвующий в транспорте холестерина в кровотоке. Мутации генов на хромосомах 1, 14 и 21 связаны с аномально высокой концентрацией бета-амилоидного белка, что коррелирует с гибелью нейронов при тяжёлой форме заболевания, которая может начинаться уже в 30 лет. Факторы образа жизни (диета, физические упражнения, социальная активность, умственная стимуляция) также влияют на потерю холинергических нейронов. Интересно, что синтетические химические вещества, напоминающие нервно-паралитический газ, но нетоксичные, используются для замедления прогрессирования болезни: они повышают концентрацию ацетилхолина в синапсах оставшихся клеток путём ингибирования ацетилхолинэстеразы, но не восстанавливают утраченные холинергические клетки.
Биогенные амины. Биогенные амины – это небольшие заряженные молекулы, синтезируемые из аминокислот, содержащих аминогруппу (R–NH₂). Наиболее распространёнными представителями являются дофамин, норадреналин, серотонин и гистамин. Адреналин – ещё один биогенный амин, но в ЦНС он не является распространённым нейромедиатором, выступая в роли основного гормона мозгового вещества надпочечников. Норадреналин выполняет функции важного нейромедиатора как в ЦНС, так и в ПНС, регулируя возбуждение, артериальное давление и настроение.
Катехоламины. Дофамин (ДА), норадреналин (НА) и адреналин содержат катехоловое кольцо (шестиуглеродное кольцо с двумя соседними гидроксильными группами) и аминогруппу, поэтому они объединены в группу катехоламинов. Катехоламины образуются из аминокислоты тирозина и проходят две одинаковые начальные стадии синтеза (рис. 6.35). Синтез начинается с захвата тирозина аксонными окончаниями и его превращения в L-дигидроксифенилаланин (L-ДОФА) под действием фермента, ограничивающего скорость – тирозингидроксилазы. В зависимости от того, какие ферменты экспрессируются в конкретном нейроне, в конечном итоге может высвобождаться любой из трёх катехоламинов. Ауторецепторы на пресинаптических окончаниях эффективно модулируют синтез и высвобождение катехоламинов, обеспечивая механизм отрицательной обратной связи.
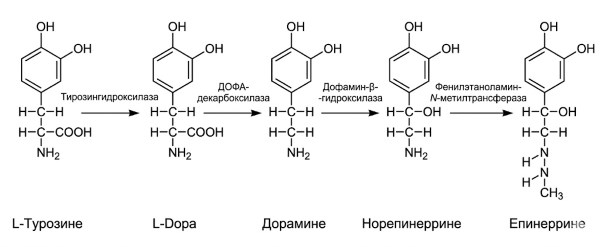
Рисунок 6.35. Путь биосинтеза катехоламинов. Тирозингидроксилаза является ферментом, лимитирующим скорость синтеза. Какой именно нейромедиатор в конечном итоге высвобождается из нейрона, зависит от присутствия одного из трёх других ферментов в данной клетке. Тёмная рамка указывает на наиболее распространённые катехоламины-нейромедиаторы в ЦНС. Адреналин – это гормон, вырабатываемый главным образом надпочечниками.
Снижение концентрации катехоламинов в синаптической щели после активации постсинаптических рецепторов происходит главным образом за счёт активного обратного захвата мембранным транспортным белком в окончание аксона. Катехоламиновые нейромедиаторы также расщепляются как во внеклеточной жидкости, так и внутри аксонного окончания ферментами, например моноаминоксидазой (МАО). Ингибиторы моноаминоксидазы (ИМАО) – препараты, повышающие уровень норадреналина и дофамина в синапсах путём замедления их метаболической деградации; они применяются при лечении некоторых форм депрессии. В ЦНС тела нейронов, выделяющих катехоламины, расположены в стволе мозга и гипоталамусе; несмотря на относительно небольшое количество этих нейронов, их аксоны широко ветвятся и пронизывают практически все отделы головного и спинного мозга. Катехоламины выполняют ключевые функции, связанные с состоянием сознания, настроением, мотивацией, направленным вниманием, движением, регуляцией артериального давления и секрецией гормонов.
Адреналин и норадреналин также синтезируются в надпочечниках. По историческим причинам (физиологи XIX века называли секрет надпочечников «адреналином») прилагательное «адренергический» описывает нейроны, выделяющие норадреналин или адреналин, а также соответствующие рецепторы. Существует два основных класса рецепторов для норадреналина и адреналина: альфа-адренорецепторы и бета-адренорецепторы. Все катехоламиновые рецепторы являются метаботропными и используют вторичные посредники для передачи сигнала. Альфа-адренорецепторы делятся на подклассы α₁ и α₂; они действуют пресинаптически (α₂, подавляя высвобождение норадреналина) или постсинаптически (α₁, стимулируя или ингибируя различные типы K⁺-каналов). Бета-адренорецепторы через стимулирующие G-белки повышают уровень цАМФ в постсинаптических клетках. Выделяют три подкласса бета-рецепторов – β₁, β₂ и β₃ – которые различаются по тканевой локализации, чувствительности к лекарствам и системам вторичных посредников.
Серотонин. Серотонин (5-гидрокситриптамин, 5-НТ) образуется из триптофана – незаменимой аминокислоты. Его действие обычно развивается медленно, что указывает на преимущественно нейромодуляторную роль серотонина. Серотонинергические нейроны иннервируют практически все структуры головного и спинного мозга и действуют через по меньшей мере 16 различных подтипов рецепторов, что отражает широкое модулирующее влияние этого медиатора. В целом, серотонин оказывает возбуждающее действие на пути, участвующие в мышечном контроле, и тормозное – на пути, передающие сенсорную информацию. Активность серотонинергических нейронов минимальна или отсутствует во время сна и максимальна в состоянии бодрствования. Помимо участия в двигательной активности и сне, серотонинергические пути регулируют пищевое поведение, репродуктивные функции и эмоциональные состояния (настроение, тревожность).
Селективные ингибиторы обратного захвата серотонина (СИОЗС) – например, пароксетин (Паксил) – используются для лечения депрессии. Они инактивируют 5-НТ-транспортер пресинаптической мембраны, который обеспечивает обратный захват серотонина, тем самым повышая синаптическую концентрацию нейромедиатора. Интересно, что такие препараты часто ассоциируются со снижением аппетита, но парадоксальным образом приводят к увеличению массы тела из-за нарушения ферментативных путей, регулирующих энергетический обмен. Этот пример иллюстрирует, как ингибиторы обратного захвата широкого спектра действия могут вызывать нежелательные побочные эффекты. Серотонин содержится как в нервных, так и в ненервных клетках; примерно 90% общего серотонина в организме находится в пищеварительной системе, 8% – в тромбоцитах крови и иммунных клетках, и только 1–2% – в головном мозге. Диэтиламид лизергиновой кислоты (ЛСД) стимулирует 5-HT₂А подтип серотониновых рецепторов в мозге, и изменение этого рецепторного комплекса вызывает интенсивные зрительные галлюцинации, характерные для приёма ЛСД.
Аминокислотные нейромедиаторы. Помимо нейромедиаторов, синтезируемых из аминокислот, некоторые аминокислоты сами непосредственно функционируют в качестве нейромедиаторов. Хотя по химической природе аминокислотные нейромедиаторы относятся к биогенным аминам, традиционно их выделяют в отдельную категорию. Аминокислотные нейромедиаторы являются наиболее распространёнными в ЦНС и воздействуют практически на все нейроны.
Глутамат. Среди возбуждающих аминокислот наиболее распространён глутамат – по оценкам, он служит основным нейромедиатором примерно в 50% возбуждающих синапсов ЦНС. Фармакологические манипуляции с глутаматными рецепторами позволили идентифицировать специфические подтипы рецепторов по их способности связывать природные и синтетические лиганды. Хотя существуют метаботропные глутаматные рецепторы, подавляющее большинство являются ионотропными; в постсинаптических мембранах обнаружены два важных подтипа: AMPA-рецепторы (связывают α-амино-3-гидрокси-5-метил-4-изоксазолпропионовую кислоту) и NMDA-рецепторы (связывают N-метил-D-аспартат).
Совместная активность AMPA- и NMDA-рецепторов участвует в долговременной потенциации (ДВП) – механизме, который связывает частую синаптическую активность с длительными изменениями силы передачи сигнала через данный синапс. ДВП считается основным клеточным процессом, лежащим в основе обучения и памяти. На рисунке 6.36 описан пошаговый механизм. Когда пресинаптический нейрон генерирует потенциалы действия (этап 1), глутамат высвобождается из пресинаптических окончаний (этап 2) и связывается как с AMPA-, так и с NMDA-рецепторами на постсинаптических мембранах (этап 3). AMPA-рецепторы действуют как типичные возбуждающие постсинаптические рецепторы: при связывании глутамата канал становится проницаемым для Na⁺ и K⁺, но больший вход Na⁺ создаёт деполяризующий ВПСП (этап 4). Напротив, каналы NMDA-рецепторов также обеспечивают значительный приток Ca²⁺, но для их открытия требуется нечто большее, чем просто связывание глутамата. Ион магния блокирует NMDA-каналы при мембранном потенциале, близком к потенциалу покоя; для вытеснения магния мембрана должна быть значительно деполяризована током, проходящим через AMPA-каналы (этап 5).
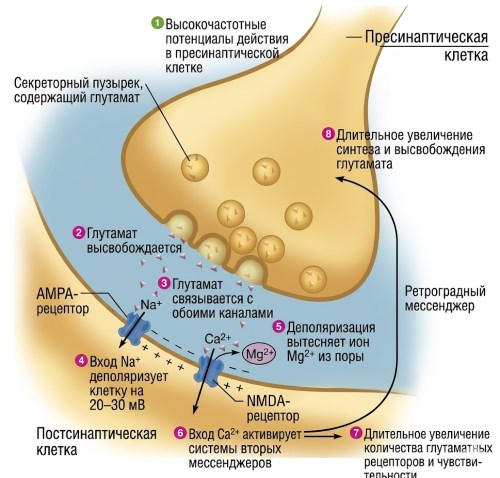
Рисунок 6.36. Длительное усиление глутаматергических синапсов. Эпизоды интенсивного возбуждения в синапсе приводят к структурным и химическим изменениям, которые усиливают силу синаптической сигнализации при последующей активации. Описание каждого шага приведено в тексте. Обратите внимание, что как AMPA, так и NMDA-рецепторы являются неспецифическими катионными каналами, которые также обеспечивают приток K⁺, но указанные чистые потоки Na⁺ и Ca²⁺ наиболее важны для механизма ДВП.
При низких частотах пресинаптических потенциалов действия недостаточная временная суммация ВПСП AMPA-рецепторов предотвращает деполяризацию на 20–30 мВ, необходимую для вытеснения магния, поэтому NMDA-рецепторы не открываются. Когда деполяризация достаточна, NMDA-рецепторы открываются, позволяя Ca²⁺ входить в постсинаптическую клетку (этап 6). Ионы кальция активируют каскад вторичных сигналов, включая постоянную активацию множества протеинкиназ, стимуляцию экспрессии генов и синтеза белка, что в конечном итоге приводит к длительному повышению постсинаптической чувствительности к глутамату (этап 7). Эта система также может активировать долговременное усиление пресинаптического высвобождения глутамата с помощью ретроградных сигналов (этап 8). Каждый последующий потенциал действия в этой пресинаптической клетке вызывает большую постсинаптическую деполяризацию, поэтому многократная активация определённого синаптического паттерна вызывает химические и структурные изменения, облегчающие дальнейшую активность по тем же путям.
NMDA-рецепторы также вовлечены в эксайтотоксичность – явление, при котором повреждение или гибель клеток мозга (например, в результате закупорки или разрыва кровеносных сосудов) быстро распространяется на соседние области. Когда клетки, содержащие глутамат, погибают и их мембраны разрываются, высвободившийся глутамат чрезмерно стимулирует AMPA- и NMDA-рецепторы на близлежащих нейронах. Чрезмерная стимуляция вызывает токсическую концентрацию внутриклеточного Ca²⁺, убивая эти нейроны и вызывая их разрыв, что приводит к прогрессирующему распространению повреждения. Эксперименты и клинические испытания показывают, что введение антагонистов NMDA-рецепторов может помочь минимизировать распространение клеточной гибели после травм головного мозга.
ГАМК. ГАМК (гамма-аминомасляная кислота) является основным тормозным нейромедиатором в головном мозге. Хотя ГАМК не входит в число 20 аминокислот, используемых для синтеза белков, её относят к аминокислотным нейромедиаторам, поскольку она представляет собой модифицированную форму глутамата. За редким исключением, ГАМК-нейроны в мозге представляют собой небольшие интернейроны, которые снижают активность в нейронных цепях. Постсинаптически ГАМК может связываться с ионотропными или метаботропными рецепторами. Ионотропный рецептор увеличивает поток Cl⁻ в клетку, вызывая гиперполяризацию (ТПСП) постсинаптической мембраны. Помимо сайта связывания ГАМК, этот рецептор имеет дополнительные участки для стероидов, барбитуратов и бензодиазепинов. Бензодиазепиновые препараты (например, алпразолам (Ксанакс) и диазепам (Валиум)) снижают тревожность, предотвращают судороги и вызывают сон за счёт увеличения потока Cl⁻ через ГАМК-рецептор.
Синапсы, использующие ГАМК, также являются одной из мишеней этанола (этилового спирта), содержащегося в алкогольных напитках. Этанол стимулирует ГАМК-синапсы и одновременно подавляет возбуждающие глутаматные синапсы, что приводит к глобальному снижению электрической активности мозга. По мере увеличения концентрации алкоголя в крови наблюдается прогрессирующее снижение когнитивных способностей, угнетение сенсорного восприятия (особенно слуха и равновесия), потеря координации движений, нарушение здравого смысла, потеря памяти и, в конечном счёте, потеря сознания. Очень высокие дозы этанола могут быть летальными из-за подавления центров ствола мозга, регулирующих кровообращение и дыхание. Этанол также воздействует на дофаминергические и эндогенные опиоидные сигнальные пути, вызывая кратковременное повышение настроения или эйфорию; вовлечение этих путей лежит в основе долгосрочной алкогольной зависимости у некоторых людей.
Глицин. Глицин является основным нейромедиатором, высвобождаемым из тормозных интернейронов спинного и стволового мозга. Он связывается с ионотропными рецепторами постсинаптических клеток, которые пропускают Cl⁻, предотвращая достижение порога возбуждения потенциалов действия. Нормальная функция глицинергических нейронов необходима для поддержания баланса возбуждающей и тормозной активности в интегрирующих центрах спинного мозга, регулирующих сокращение скелетных мышц. Этот баланс становится очевидным при отравлении нейротоксином стрихнином – антагонистом глициновых рецепторов, иногда используемым для уничтожения грызунов. Поражённые люди испытывают повышенную возбудимость нервной системы, что приводит к судорогам, спастическим сокращениям скелетных мышц и, в конечном счёте, к смерти из-за нарушения работы дыхательных мышц.
Нейропептиды. Нейропептиды состоят из двух или более аминокислот, соединённых пептидными связями. Идентифицировано около 100 нейропептидов, хотя физиологические функции многих из них неизвестны. Эволюция благоприятствовала использованию одних и тех же химических посредников в различных обстоятельствах, и многие нейропептиды были ранее обнаружены в невральной ткани, где они функционируют как гормоны или паракринные вещества; как правило, они сохраняют названия, данные при первом обнаружении.
Нейропептиды образуются иначе, чем другие нейротрансмиттеры, которые синтезируются в окончаниях аксонов. Нейропептиды образуются из крупных белков-предшественников, обладающих незначительной биологической активностью. Синтез этих предшественников, направляемый мРНК, происходит на рибосомах, расположенных только в теле клетки и крупных дендритах нейрона, часто на значительном расстоянии от мест высвобождения пептидов. В теле клетки белок-предшественник упаковывается в везикулы, которые затем транспортируются с помощью аксонального транспорта к терминалям, где белок расщепляется специфическими пептидазами. Многие белки-предшественники содержат несколько пептидов (различных или повторяющихся). Нейроны, которые выделяют один или несколько пептидных нейромедиаторов, называются пептидергическими. Во многих случаях нейропептиды секретируются совместно с другими типами нейромедиаторов и действуют как нейромодуляторы.
Количество нейропептидов, высвобождаемых из везикул в синапсах, значительно меньше, чем у непептидергических нейромедиаторов (например, катехоламинов). Кроме того, нейропептиды могут диффундировать из синапса и воздействовать на удалённые нейроны, и в этом случае их называют нейромодуляторами. Такие действия длятся дольше (сотни миллисекунд), чем при классической нейромедиаторной передаче. После высвобождения нейропептиды взаимодействуют с ионотропными или метаботропными рецепторами и в конечном итоге расщепляются пептидазами, расположенными в мембранах нейронов.
Эндогенные опиоиды – группа нейропептидов, включающая бета-эндорфин, динорфины и энкефалины, – вызвали значительный интерес, поскольку их рецепторы являются местами действия опиатных препаратов (например, морфина и кодеина). Опиатные препараты – мощные анальгетики (обезболивающие без потери сознания), и эндогенные опиоиды, несомненно, участвуют в регуляции боли. Данные также указывают на то, что опиоиды регулируют пищевое и питьевое поведение, функции кровеносной системы, настроение и эмоции.
Газы как нейромедиаторы. Некоторые очень короткоживущие газы также служат нейромедиаторами. Лучше всего изучен оксид азота, однако недавние исследования показывают, что монооксид углерода и сероводород также выделяются нейронами в качестве сигнальных молекул. Газы не выделяются путём экзоцитоза пресинаптических пузырьков и не связываются с рецепторами постсинаптической плазматической мембраны. Они вырабатываются ферментами в окончаниях аксонов (в ответ на вход Ca²⁺) и просто диффундируют из места своего происхождения во внутриклеточную жидкость других нейронов или эффекторных клеток, где связываются и активируют белки. Например, оксид азота, выделяющийся из нейронов, активирует гуанилилциклазу в клетках-мишенях, повышая концентрацию второго посредника – циклического GMP, который затем может изменять активность ионных каналов в постсинаптической клетке.
Оксид азота участвует в широком спектре процессов, опосредованных нервной системой, включая обучение, развитие, толерантность к лекарствам, эрекцию полового члена и клитора, а также сенсорную и моторную модуляцию. Парадоксально, но он также связан с повреждением нервной системы при прекращении притока крови к мозгу или при черепно-мозговой травме. Оксид азота вырабатывается не только в ЦНС и ПНС, но и различными ненейральными клетками, выполняя важные паракринные функции, в частности в кровеносной и иммунной системах.
Пурины как нейромодуляторы. К другим нетрадиционным нейромедиаторам относятся пурины – АТФ и аденозин, которые действуют главным образом как нейромодуляторы. АТФ присутствует во всех пресинаптических пузырьках и высвобождается совместно с одним или несколькими другими нейротрансмиттерами в ответ на вход Ca²⁺ в терминаль. Аденозин образуется из АТФ под действием ферментов во внеклеточном пространстве. Для аденозина описаны как пре-, так и постсинаптические рецепторы. Функции этих веществ в нервной системе и других тканях остаются активной областью исследований.
Сведения об авторах и источниках:
Авторы: Эрик П. Видмайер, Бостонский университет, Хершел Рафф, Медицинский колледж Висконсина, Медицинский центр Авроры Сент-Люк, Кевин Т. Странг, Университет Висконсин-Мэдисон
Источник: Физиология человека: механизмы функционирования организма
Данные публикации будут полезны студентам биологических и медицинских специальностей, начинающим специалистам в области клеточной биологии, биофизики и физиологии, а также всем, кто интересуется основами мембранного транспорта и регуляции клеточного гомеостаза.
Дата добавления: 2026-04-29; просмотров: 113;











