Аквапорины и осмос: механизмы водного транспорта и регуляции объема клеток
Вода, несмотря на свою полярность, способна быстро проникать через плазматические мембраны большинства клеток. Этот процесс обеспечивается семейством мембранных белков — аквапоринами, которые формируют специализированные каналы для трансмембранного переноса молекул воды. Тип и количество таких каналов значительно варьируют в разных клеточных мембранах, что обусловливает различную водопроницаемость клеток. Кроме того, в ряде клеток количество аквапоринов и, соответственно, проницаемость мембраны для воды могут динамически изменяться под действием физиологических сигналов, что представляет собой важный регуляторный механизм.
Данный механизм особенно значим для эпителиальных клеток, выстилающих определенные протоки в почках. Как будет показано в главе 14, одна из ключевых функций почек — регуляция объема воды, выделяемой с мочой, что поддерживает гомеостаз общего количества жидкости в организме. Эпителиоциты почечных протоков содержат большое количество аквапоринов, численность которых может увеличиваться или уменьшаться в зависимости от текущего водного баланса. Например, при обезвоживании количество аквапоринов в мембранах этих клеток возрастает, что способствует дополнительной реабсорбции воды из образующейся мочи обратно в кровоток. Именно эта физиологическая реакция объясняет значительное уменьшение объема мочи при обезвоживании организма.
Осмос и градиенты концентрации воды. Суммарная диффузия воды через полупроницаемую мембрану определяется как осмос. Как и все диффузионные процессы, осмос требует наличия разницы концентраций для создания направленного потока молекул воды. Чтобы понять, как возникает разница в концентрации воды на мембране, необходимо изучить взаимосвязь между растворенными веществами и молекулами воды в растворе. Добавление растворенного вещества в чистую воду эффективно снижает концентрацию молекул воды в этом растворе, поскольку каждая частица растворенного вещества занимает объем, который ранее принадлежал молекуле воды.
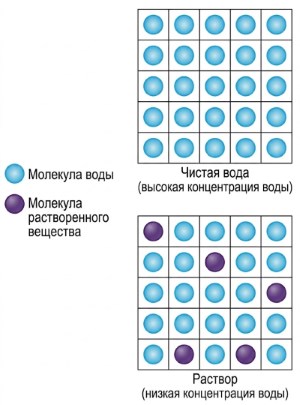
Рисунок 4.16. Добавление молекул растворенного вещества в чистую воду снижает концентрацию воды в растворе
Количественно это выражается следующим образом: один литр чистой воды весит примерно 1000 г, а молярная масса воды составляет 18 г/моль, следовательно, концентрация воды в чистой воде равна 1000/18 = 55,5 М. Уменьшение концентрации воды в растворе приблизительно равно концентрации добавленного растворенного вещества, то есть одна молекула растворенного вещества вытесняет примерно одну молекулу воды. Так, в 1 М растворе глюкозы концентрация воды составляет около 54,5 М, а не 55,5 М. Подобно тому как добавление воды разбавляет растворенное вещество, добавление растворенного вещества «разбавляет» молекулы воды, и более высокие концентрации растворенных веществ прямо коррелируют с более низкими концентрациями воды.
Частицы растворенного вещества и концентрация воды. Степень снижения концентрации воды при добавлении растворенного вещества зависит исключительно от количества частиц (молекул или ионов) в растворе, а не от их химического состава. Например, 1 моль глюкозы, 1 моль аминокислоты или 1 моль мочевины в 1 литре раствора снижают концентрацию воды в одинаковой степени, поскольку каждая из этих молекул остается в растворе в виде отдельной частицы. Однако молекулы, которые ионизируются в растворе, снижают концентрацию воды пропорционально общему числу ионов, образующихся при диссоциации. Многие простые соли почти полностью диссоциируют в водных растворах, и для упрощения можно принять 100%-ную диссоциацию при температуре тела и физиологических концентрациях.
Следовательно, 1 моль хлорида натрия (NaCl) в растворе дает 1 моль ионов натрия (Na⁺) и 1 моль ионов хлорида (Cl⁻), что составляет 2 моля общих растворенных частиц и снижает концентрацию воды вдвое по сравнению с 1 молем неионизирующейся глюкозы. Аналогично, 1 М раствор хлорида магния (MgCl₂) при полной диссоциации образует один ион Mg²⁺ и два иона Cl⁻, что снижает концентрацию воды в три раза сильнее, чем 1 М раствор глюкозы. Таким образом, именно общее количество частиц определяет осмотический эффект.
Осмолярность: общая концентрация растворенного вещества. Поскольку концентрация воды в растворе зависит от суммарного количества частиц растворенного вещества, удобно использовать термин «осмолярность», который обозначает общую концентрацию всех растворенных частиц независимо от их химической природы. Один осмоль определяется как 1 моль частиц растворенного вещества. Соответственно, 1 М раствор глюкозы имеет осмолярность 1 Осмоль/л, тогда как 1 М раствор NaCl содержит 2 осмоль растворенного вещества на литр раствора. Литр раствора, содержащего 1 моль глюкозы и 1 моль NaCl, обладает осмолярностью 3 Осмоль/л.
Раствор с осмолярностью 3 Осмоль/л может содержать 1 моль глюкозы плюс 1 моль NaCl, или 3 моля глюкозы, или 1,5 моля NaCl, либо любую другую комбинацию растворенных веществ, при условии, что общая концентрация частиц равна 3 осмоль/л. Хотя осмолярность количественно определяет концентрацию растворенных частиц, она одновременно задает концентрацию воды: более высокая осмолярность неизменно означает более низкую концентрацию воды. Важно, что любые два раствора с одинаковой осмолярностью имеют одинаковую концентрацию воды, поскольку общее число частиц растворенного вещества в единице объема одинаково.
Осмос через мембраны. Применяя эти принципы к осмосу через мембраны, рассмотрим два отсека объемом 1 литр, разделенные мембраной, проницаемой как для растворенных веществ, так и для воды. Исходно в отсеке 1 концентрация растворенного вещества составляет 2 Осмоль/л, а в отсеке 2 — 4 Осмоль/л. Эта разница создает соответствующий градиент концентрации воды: примерно 53,5 М в отсеке 1 и 51,5 М в отсеке 2. В результате происходит суммарная диффузия воды из отсека 1 в отсек 2 (из области с более высокой концентрацией воды в область с более низкой), тогда как растворенное вещество диффундирует в противоположном направлении.
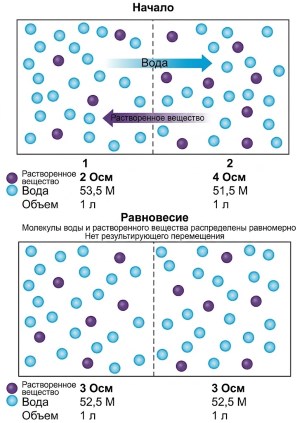
Рисунок 4.17. Между двумя отделениями одинакового объема суммарная диффузия воды и растворенного вещества через мембрану, проницаемую для обоих, приводит к диффузионному равновесию, при этом объем отделений не изменяется.
При диффузионном равновесии в обоих отсеках достигается одинаковая концентрация растворенного вещества (3 Осмоль/л) и воды (52,5 М). Один моль воды переходит из отсека 1 в отсек 2, а один моль растворенного вещества — из отсека 2 в отсек 1. Поскольку растворенное вещество замещает воду в каждом отсеке, полезный объем камер не меняется, когда мембрана проницаема и для воды, и для растворенных веществ. Однако если заменить мембрану на проницаемую только для воды, но не для растворенных веществ, картина меняется.
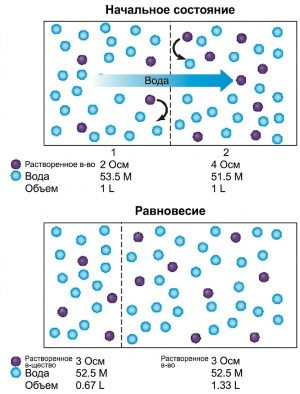
Рисунок 4.18. Движение воды через мембрану, которая проницаема для воды, но не для растворенных веществ, приводит к равновесному состоянию с изменением объемов двух отсеков. В этом случае происходит суммарная диффузия 0,33 л воды из отсека 1 в отсек 2. (Мембрана растягивается при увеличении объема отсека 2, так что существенного изменения давления не происходит.)
Вода диффундирует из отсека 1 в отсек 2, но растворенные вещества не могут двигаться в обратном направлении. Вода продолжает поступать в отсек 2 до выравнивания концентраций воды по обе стороны мембраны. При поступлении воды в отсек 2 концентрация растворенного вещества в нем снижается из-за разбавления, а в отсеке 1 — возрастает по мере выхода воды. Когда достигается диффузионное равновесие, осмолярность обоих отсеков становится одинаковой, что требует переноса достаточного количества воды из отсека 1 в отсек 2 для увеличения объема второго на треть и соответственного уменьшения первого. Именно наличие мембраны, непроницаемой для растворенных веществ, приводит к изменению объема, характерному для осмоса.
Осмотическое давление. В приведенном примере стенки отсеков способны к неограниченному расширению, что позволяет перемещать чистую воду без создания разницы давлений на мембране. Однако если бы стенки отсека 2 имели ограниченную растяжимость (как плазматические мембраны клеток), поступление воды в отсек 2 повысило бы в нем давление, что препятствовало бы дальнейшему притоку воды. Таким образом, попадание воды в отсек 2 можно предотвратить, приложив к нему внешнее давление. Это приводит к важному определению: когда раствор, содержащий растворенные вещества, отделен от чистой воды полупроницаемой мембраной (проницаемой для воды, но не для растворенных веществ), давление, которое необходимо приложить к раствору, чтобы предотвратить поступление в него чистой воды, называется осмотическим давлением этого раствора.
Чем выше осмолярность раствора, тем выше его осмотическое давление. Важно понимать, что осмотическое давление не оказывает активного воздействия на молекулы воды; оно представляет собой величину давления, необходимую для предотвращения осмотического потока. Как и осмолярность, осмотическое давление служит мерой концентрации воды в растворе: чем ниже концентрация воды, тем выше осмотическое давление. Этот принцип имеет прямое отношение к клеточной физиологии.
Внеклеточная осмолярность и клеточный объем. Принципы осмоса непосредственно применимы к клеткам, которые удовлетворяют всем условиям для возникновения осмотического потока воды через мембрану. Как внутриклеточная, так и внеклеточная жидкость содержат воду, а клетки окружены плазматической мембраной, обладающей высокой проницаемостью для воды, но непроницаемой для многих веществ. Вещества, не способные проникать через плазматическую мембрану, называются непроницаемыми растворенными веществами — они не диффундируют через липидный бислой. Большинство внеклеточных растворенных частиц — это ионы Na⁺ и Cl⁻, которые хотя и могут попадать в клетки через ионные каналы, но активно удаляются обратно.
В частности, Na⁺/K⁺-АТФазные насосы постоянно выводят Na⁺ из клетки, поэтому внеклеточный Na⁺ фактически ведет себя как непроницаемое растворенное вещество. Ионы Cl⁻, попадая в клетки, также быстро удаляются благодаря электрическому отталкиванию, создаваемому мембранным потенциалом, и работе различных переносчиков. Внутри клетки основными растворенными частицами являются ионы калия (K⁺) и различные органические вещества. Большинство органических веществ — крупные полярные молекулы, не способные диффундировать через плазматическую мембрану. Хотя K⁺ может выходить из клеток через K⁺-каналы, он активно транспортируется обратно Na⁺/K⁺-АТФазой. В итоге внутриклеточный K⁺ также ведет себя как непроницаемое растворенное вещество, ограниченное внутриклеточной жидкостью.
Тонус и регуляция объема клеток. Нормальная осмолярность внеклеточной жидкости колеблется в пределах 285–300 мОсм (для упрощения в тексте используется значение 300 мОсм). Поскольку вода свободно диффундирует через плазматические мембраны, вода во внутриклеточном и внеклеточном пространствах достигает диффузионного равновесия, что приводит к равной осмолярности около 300 мОсм в обоих отделах. Изменения внеклеточной осмолярности могут вызывать сжатие или набухание клеток (например, эритроцитов) по мере перемещения молекул воды через плазматическую мембрану.
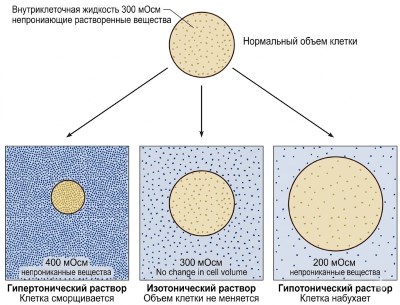
Рисунок 4.19. Изменения объема клеток, вызываемые гипертоническими, изотоническими и гипотоническими растворами (курсивом показано: в изотоническом растворе объем не меняется, в гипотоническом — клетки набухают, в гипертоническом — сжимаются)
Когда клетки с внутриклеточной осмолярностью 300 мОсм помещают в раствор непроницаемых растворенных веществ с такой же осмолярностью 300 мОсм, они не набухают и не сжимаются, поскольку концентрации воды по обе стороны мембраны равны, а растворенные вещества не могут проникать в клетки или покидать их. Такие растворы называются изотоническими — это любые растворы, не изменяющие размер клеток. Изотонические растворы содержат ту же концентрацию непроницаемых растворенных веществ, что и нормальная внеклеточная жидкость.
Гипотонические растворы имеют концентрацию непроницаемого растворенного вещества ниже, чем внутри клеток, что приводит к осмотическому потоку воды внутрь клеток и их набуханию. Напротив, растворы, содержащие более 300 мОсм непроницаемых растворенных веществ (гипертонические растворы), заставляют клетки сжиматься по мере того, как вода диффундирует из клеток в жидкость с более низкой концентрацией воды. Концентрация непроницаемых растворенных веществ в растворе, а не общая осмолярность, определяет его тонус (изотонический, гипотонический или гипертонический). Проникающие растворенные вещества, которые легко проходят через липидный бислой, не влияют на тонус, поскольку их концентрации быстро выравниваются по обе стороны мембраны.
Различие между осмолярностью и тонусом. Другой набор терминов — изоосмотический, гипоосмотический и гиперосмотический — обозначает осмолярность раствора относительно нормальной внеклеточной жидкости, независимо от способности растворенных веществ проникать через мембрану. Эти два набора терминов не являются синонимами. Например, 1-литровый раствор, содержащий по 150 мОсм непроницаемых Na⁺ и Cl⁻ плюс 100 мОсм мочевины (которая быстро проникает через плазматические мембраны), будет иметь общую осмолярность 400 мОсм и являться гиперосмотичным по сравнению с обычной клеткой. Однако этот же раствор будет изотоническим, поскольку мочевина как проникающее растворенное вещество быстро войдет в клетки, выравнивая осмолярность и не вызывая изменения конечного объема клеток.

Первоначально клетки, помещенные в такой раствор, сжимаются из-за выхода воды во внеклеточную жидкость. Но мочевина быстро проникает в клетки, пока ее концентрация не сравняется с внеклеточной. В результате внутриклеточный и внеклеточный растворы достигают одинаковой осмолярности, что устраняет разницу в концентрации воды на мембране, и конечный объем клеток не изменяется. Это происходит даже при том, что внеклеточная жидкость остается гиперосмотичной (400 мОсм) по сравнению с нормальным значением в 300 мОсм. Таким образом, понимание различия между осмолярностью и тонусом критически важно для интерпретации клеточных реакций на изменения внешней среды.
Сведения об авторах и источниках:
Авторы: Эрик П. Видмайер, Бостонский университет, Хершел Рафф, Медицинский колледж Висконсина, Медицинский центр Авроры Сент-Люк, Кевин Т. Странг, Университет Висконсин-Мэдисон
Источник: Физиология человека: механизмы функционирования организма
Данные публикации будут полезны студентам биологических и медицинских специальностей, начинающим специалистам в области клеточной биологии, биофизики и физиологии, а также всем, кто интересуется основами мембранного транспорта и регуляции клеточного гомеостаза.
Дата добавления: 2026-04-29; просмотров: 141;











