Мембранный потенциал покоя нейронов: ионные механизмы, уравнение Нернста и уравнение Голдмана-Ходжкина-Каца
В состоянии покоя нейроны демонстрируют разность потенциалов на своей плазматической мембране, при этом внутренняя среда клетки заряжена отрицательно относительно внеклеточной (рис. 6.8). Эта разность электрических потенциалов называется мембранным потенциалом покоя (сокращённо Vm). По общему правилу, внеклеточная жидкость служит точкой отсчёта напряжения, а полярность мембранного потенциала определяется знаком избыточного заряда внутри клетки. Например, если внутриклеточная жидкость имеет избыток отрицательного заряда, а величина разности потенциалов составляет 70 мВ, то мембранный потенциал определяют как –70 мВ (внутренний по отношению к внешнему). Важно подчеркнуть, что вольты измеряют разницу зарядов на мембране; значение Vm = −70 мВ не указывает на абсолютное количество положительных или отрицательных зарядов по обе стороны мембраны.
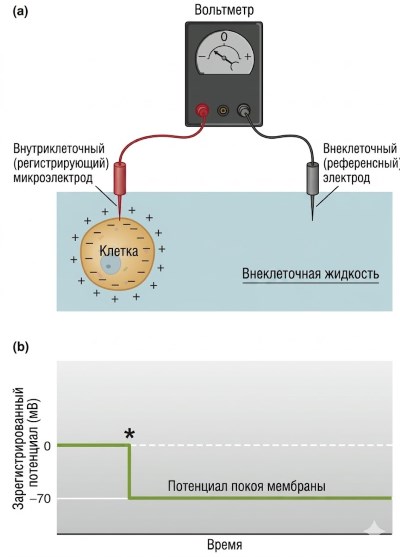
Рисунок 6.8. (а) Устройство для измерения мембранных потенциалов. Вольтметр регистрирует разность потенциалов между внутриклеточным и внеклеточным электродами. (b) Разность потенциалов на плазматической мембране, измеряемая с помощью внутриклеточного микроэлектрода. Звёздочка указывает момент входа электрода в клетку.
Величина и природа мембранного потенциала покоя. Величина мембранного потенциала покоя в нейронах обычно варьирует от –40 до –90 мВ. Этот потенциал остаётся постоянным, если только изменения электрического тока не изменят его; по определению, клетка в таких условиях больше не находится в состоянии покоя. Мембранный потенциал покоя существует благодаря небольшому избытку отрицательных ионов внутри клетки и избытку положительных ионов снаружи. Эти избыточные заряды концентрируются в тонком слое, плотно прилегающем к внутренней и внешней поверхностям плазматической мембраны (рис. 6.9), тогда как основная масса внутриклеточной и внеклеточной жидкости остаётся электрически нейтральной. В отличие от схематических представлений, количество зарядов, распределённых вдоль мембраны для создания потенциала, составляет исчезающе малую долю от общего числа зарядов в обоих отсеках.
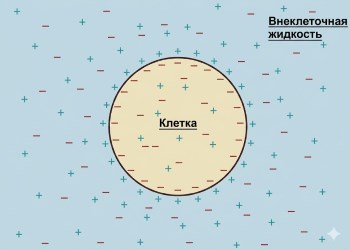
Рисунок 6.9. Избыточные положительные заряды снаружи клетки и избыточные отрицательные заряды внутри скапливаются в плотном слое, прилегающем к плазматической мембране. В действительности эти избыточные заряды составляют чрезвычайно малую долю от общего количества ионов внутри и снаружи клетки.
В таблице 6.2 приведены концентрации ионов натрия (Na⁺), калия (K⁺) и хлорида (Cl⁻) во внеклеточной и внутриклеточной жидкости типичного нейрона. Каждый из этих ионов демонстрирует разницу концентраций по обе стороны мембраны в 10–30 раз. Хотя таблица может создать впечатление несоответствия с утверждением об электронейтральности, следует помнить, что в обеих жидкостях присутствуют и многие другие ионы, включая Mg²⁺, Ca²⁺, H⁺, HCO₃⁻, HPO₄²⁻, SO₄²⁻, а также ионизированные органические соединения (аминокислоты и белки). При учёте всех ионов каждый раствор действительно является электрически нейтральным.

Из всех ионов, способных проходить через мембрану и влиять на её электрический потенциал, Na⁺, K⁺ и Cl⁻ присутствуют в наиболее высоких концентрациях, причём проницаемость мембраны для каждого из них определяется независимо. Na⁺ и K⁺ вносят наиболее важный вклад в формирование мембранного потенциала покоя, хотя в некоторых клетках значимым фактором может быть также Cl⁻. Обратите внимание, что концентрации Na⁺ и Cl⁻ внутри клетки ниже, чем снаружи, тогда как концентрация K⁺ внутри выше. Различия концентраций для Na⁺ и K⁺ поддерживаются Na⁺/K⁺-АТФазой (натрий-калиевым насосом), который выкачивает Na⁺ из клетки и закачивает K⁺ внутрь. Распределение Cl⁻ варьирует в зависимости от типа клетки, как описано далее.
Величина мембранного потенциала покоя зависит главным образом от двух факторов: (1) различий в концентрациях ионов во внутриклеточной и внеклеточной жидкостях и (2) различий в мембранной проницаемости для разных ионов, отражающих количество открытых каналов для каждого иона в плазматической мембране. Третий фактор — прямое воздействие ионных насосов — играет меньшую роль. Рассмотрим каждый из них подробно.
Влияние разности концентраций ионов. Чтобы понять, как разность концентраций Na⁺ и K⁺ создаёт мембранные потенциалы, сначала рассмотрим ситуацию, когда мембрана проницаема (имеет открытые каналы) только для одного иона (рис. 6.10). В этой гипотетической модели предположим, что мембрана содержит K⁺-каналы, но не содержит Na⁺- или Cl⁻-каналов. Изначально в камере 1 содержится 0,15 М NaCl, в камере 2 — 0,15 М KCl, и движения ионов нет, поскольку каналы закрыты (рис. 6.10а). Разность потенциалов отсутствует, так как в двух отсеках равное количество положительных и отрицательных ионов. Однако при открытии K⁺-каналов ионы K⁺ диффундируют вниз по градиенту концентрации из камеры 2 в камеру 1 (рис. 6.10б). После перемещения нескольких ионов калия камера 1 приобретает избыточный положительный заряд, оставляя избыток отрицательного заряда в камере 2 (рис. 6.10в), создавая таким образом разность потенциалов на мембране.
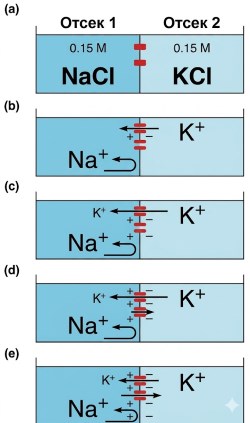
Рисунок 6.10. Создание потенциала на мембране за счёт диффузии K⁺ через каналы (красный). Стрелки обозначают движение ионов; длина стрелки отражает величину потока. Подробное объяснение этапов a–e приведено в тексте.
Возникает дополнительный фактор, влияющий на суммарное перемещение ионов: электрический потенциал. По мере того как камера 1 становится всё более положительной, а камера 2 — более отрицательной, мембранный потенциал начинает влиять на движение K⁺. Отрицательный заряд камеры 2 притягивает K⁺ обратно, а положительный заряд камеры 1 отталкивает их (рис. 6.10г). Таким образом, для всех ионов через мембрану существует электрохимический градиент. Пока поток, обусловленный концентрационным градиентом K⁺, превышает поток, обусловленный мембранным потенциалом, чистое перемещение K⁺ происходит из камеры 2 в камеру 1, и мембранный потенциал постепенно нарастает. В конечном счёте мембранный потенциал становится достаточно отрицательным, чтобы создать поток, равный по величине, но противоположный по направлению потоку от концентрационного градиента (рис. 6.10е). Мембранный потенциал, при котором эти два потока уравновешиваются, называется равновесным потенциалом для данного иона (здесь для K⁺). При равновесном потенциале суммарное движение иона отсутствует, и потенциал больше не изменяется.
Количество ионов, проходящих через мембрану для установления этого равновесного потенциала, ничтожно по сравнению с исходным количеством, поэтому между этапами (а) и (е) не происходит существенного изменения концентрации K⁺ ни в одном из отсеков. Величина равновесного потенциала (в мВ) для любого иона зависит от его концентрационного градиента на мембране. Если бы концентрации по обе стороны были равны, суммарный поток был бы нулевым, и равновесный потенциал также равнялся бы нулю. Чем больше градиент концентрации, тем больше равновесный потенциал, поскольку для уравновешивания диффузионного движения требуется большее электрическое противодействие.
Теперь рассмотрим мембрану, содержащую только Na⁺-каналы (рис. 6.11). Ионы Na⁺ первоначально перемещаются из камеры 1 в камеру 2. Когда камера 2 становится положительной относительно камеры 1, электрическая разность начинает отталкивать Na⁺ обратно, и в конце концов чистое движение прекращается. Снова при равновесном потенциале диффузионный поток уравновешивается электрическим, и лишь незначительное количество ионов натрия реально перемещается. Таким образом, равновесный потенциал для одного иона может отличаться по величине и знаку от равновесных потенциалов других ионов в зависимости от их трансмембранных градиентов концентрации.
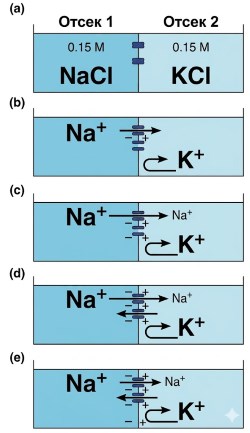
Рисунок 6.11. Создание потенциала на мембране за счёт диффузии Na⁺ через Na⁺-каналы (синий). Стрелки обозначают движение ионов; длина стрелки — величину потока. Через мембрану проходит так мало ионов натрия, что их концентрация существенно не меняется от этапа (а) к этапу (е).
Существует способ предсказать, какая электрическая сила требуется для точного уравновешивания тенденции иона диффундировать вниз по его концентрационному градиенту. Уравнение Нернста описывает равновесный потенциал для любого иона — электрический потенциал, необходимый для уравновешивания заданного концентрационного градиента так, чтобы суммарный ионный поток стал нулевым. Уравнение Нернста имеет вид:

Используя концентрационные градиенты из таблицы 6.2, равновесные потенциалы для Na⁺ (ENa) и K⁺ (EK) составляют:
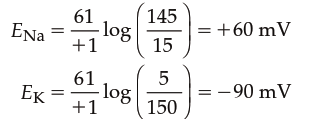
Таким образом, при этих типичных концентрациях поток Na⁺ через открытые каналы будет стремиться приблизить мембранный потенциал к +60 мВ, тогда как поток K⁺ приблизит его к –90 мВ. Если градиенты концентраций изменятся, изменятся и равновесные потенциалы. Гипотетические ситуации на рисунках 6.10 и 6.11 полезны для понимания влияния отдельных проникающих ионов, но в реальных клетках всё сложнее: множество заряженных молекул влияют на общие электрические свойства, и клетки редко бывают проницаемы только для одного иона.
Влияние различных ионных проницаемостей. Уравнение Голдмана–Ходжкина–Каца. Когда в мембране одновременно открыты каналы для нескольких типов ионов, необходимо учитывать проницаемость и градиенты концентрации всех этих ионов для расчёта мембранного потенциала. При заданном градиенте концентрации, чем выше проницаемость мембраны для данного иона, тем больший вклад этот ион вносит в мембранный потенциал. Учитывая градиенты концентрации и относительную проницаемость мембраны (Pион) для Na⁺, K⁺ и Cl⁻, мембранный потенциал покоя (Vm) может быть рассчитан с помощью уравнения Голдмана–Ходжкина–Каца (GHK):
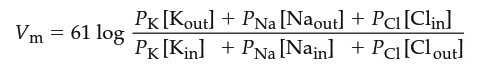
Уравнение GHK является расширенной версией уравнения Нернста, учитывающей проницаемость нескольких ионов. Если установить проницаемости любых двух ионов в ноль, получится равновесный потенциал для оставшегося иона. Обратите внимание, что концентрации Cl⁻ в числителе и знаменателе переставлены по сравнению с Na⁺ и K⁺, поскольку Cl⁻ является анионом, и его перемещение оказывает противоположное влияние на мембранный потенциал. Ионные градиенты и проницаемости сильно различаются у разных возбудимых клеток, однако уравнение GHK может определить мембранный потенциал покоя любой клетки при известных условиях.
Например, если значения относительной проницаемости клетки равны PK=1, PNa=0,04 и PCl=0,45, а концентрации ионов соответствуют таблице 6.2, то мембранный потенциал покоя составит:
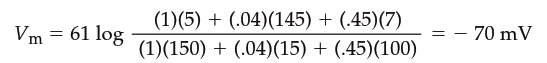
Таким образом, вклад Na⁺, K⁺ и Cl⁻ в общий мембранный потенциал зависит от их концентрационных градиентов и относительной проницаемости. Градиенты концентрации определяют равновесные потенциалы, а относительная проницаемость — степень, в которой мембранный потенциал покоя смещается в сторону этих равновесных потенциалов. В нейронах млекопитающих проницаемость для K⁺ может в 100 раз превышать проницаемость для Na⁺ и Cl⁻, поэтому мембранные потенциалы покоя нейронов обычно довольно близки к равновесному потенциалу для K⁺ (рис. 6.12). Величина равновесного потенциала Cl⁻ также близка к мембранному потенциалу покоя во многих нейронах, однако Cl⁻ имеет минимальное значение для определения потенциалов покоя нейронов по сравнению с K⁺ и Na⁺.
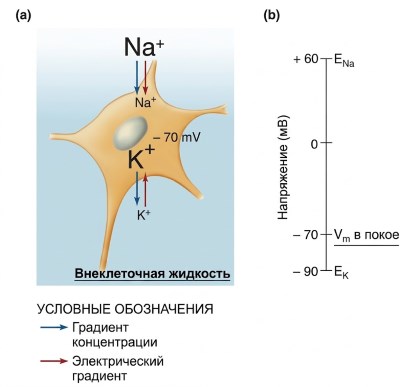
Рисунок 6.12. Силы, действующие на ионы натрия и калия при мембранном потенциале покоя (Vm). (а) При мембранном потенциале покоя, равном –70 мВ, как концентрационный, так и электрический градиенты благоприятствуют вхождению Na⁺ внутрь, тогда как для K⁺ эти градиенты направлены в противоположные стороны. (b) Высокая проницаемость и подвижность K⁺ поддерживают мембранный потенциал покоя на уровне, близком к EK.
Следовательно, потенциал покоя генерируется в основном за счёт выхода K⁺ из клетки вниз по концентрационному градиенту через постоянно открытые K⁺-каналы (называемые каналами утечки или незакреплёнными каналами, в отличие от закрываемых каналов). Это делает внутреннюю часть клетки отрицательной по отношению к наружной. Несмотря на то что поток K⁺ оказывает большее влияние на мембранный потенциал покоя, чем поток Na⁺, потенциал покоя не равен EK, поскольку небольшое количество открытых Na⁺-каналов утечки слегка смещает мембранный потенциал в сторону ENa. Таким образом, в состоянии покоя ионные каналы обеспечивают чистое движение как Na⁺ внутрь клетки, так и K⁺ из клетки.
Вклад ионных насосов. Со временем внутриклеточные концентрации Na⁺ и K⁺ не изменяются благодаря работе Na⁺/K⁺-АТФазы. В покоящейся клетке количество ионов, перекачиваемых насосом, равно количеству ионов, пассивно протекающих вниз по своим электрохимическим градиентам. Пока градиенты концентраций стабильны, а ионная проницаемость плазматической мембраны не меняется, электрический потенциал на мембране покоя остаётся постоянным. До сих пор мы описывали мембранный потенциал как следствие исключительно пассивного движения ионов по электрохимическим градиентам, тогда как градиенты концентраций поддерживаются мембранными насосами. Однако насос Na⁺/K⁺-АТФаза не только поддерживает эти градиенты, но и создаёт их изначально.
Более того, насос помогает более точно устанавливать мембранный потенциал. Na⁺/K⁺-АТФаза выводит из клетки три иона Na⁺ на каждые два вводимых K⁺. Этот неравный перенос положительных зарядов делает внутреннюю среду клетки более отрицательной, чем это было бы при одной лишь ионной диффузии. Когда насос переносит суммарный заряд через мембрану и непосредственно вносит вклад в мембранный потенциал, его называют электрогенным насосом. В большинстве клеток электрогенный вклад в мембранный потенциал довольно мал. Тем не менее насос всегда вносит существенный косвенный вклад, поддерживая концентрационные градиенты, которые определяют диффузионные потоки и разделение зарядов.
Краткое описание развития мембранного потенциала покоя. На рисунке 6.13 показано формирование мембранного потенциала покоя в три концептуальных этапа. Во-первых, под действием Na⁺/K⁺-АТФазы устанавливаются градиенты концентраций Na⁺ и K⁺ (рис. 6.13а). Эти градиенты определяют равновесные потенциалы двух ионов — величину, до которой каждый ион изменил бы мембранный потенциал, если бы он был единственным проникающим ионом. Одновременно насос оказывает небольшой электрогенный эффект, поскольку выкачивает три Na⁺ на каждые два введённых K⁺. Далее, изначально наблюдается больший поток K⁺ из клетки, чем Na⁺ внутрь клетки (рис. 6.13б), так как в покоящейся мембране проницаемость (больше каналов утечки) выше для K⁺, чем для Na⁺. Поскольку на этом этапе чистый отток положительных ионов превышает приток, возникает значительный отрицательный мембранный потенциал, приближающийся к EK. В стационарном состоянии покоя нейрона ионные потоки через мембрану достигают динамического равновесия (рис. 6.13в). Поскольку мембранный потенциал не равен равновесному потенциалу ни для одного из ионов, происходит небольшая, но устойчивая утечка Na⁺ внутрь клетки и K⁺ из клетки. Однако градиенты концентраций не исчезают со временем, поскольку ионный транспорт с помощью Na⁺/K⁺-АТФазы точно уравновешивает скорость пассивного движения ионов в противоположном направлении.
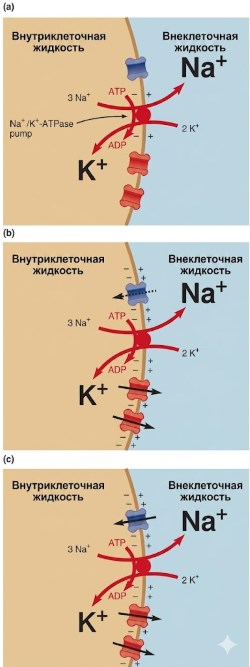
Рисунок 6.13. Краткое описание этапов формирования мембранного потенциала покоя. (а) Na⁺/K⁺-АТФаза создаёт градиенты концентраций и генерирует небольшой отрицательный потенциал. (b) Больший чистый выход K⁺, чем вход Na⁺, делает мембранный потенциал более отрицательным внутри. (c) При постоянном отрицательном мембранном потенциале покоя ионные потоки через каналы и активный транспорт уравновешивают друг друга.
Хлорид-ионы и потенциал покоя. Вернёмся к поведению хлорид-ионов в возбудимых клетках. Плазматические мембраны многих клеток имеют Cl⁻-каналы, но не содержат насосов для перекачки хлорида. Следовательно, в этих клетках концентрация Cl⁻ пассивно распределяется до тех пор, пока равновесный потенциал Cl⁻ (ECl) не сравняется с мембранным потенциалом покоя. Другими словами, отрицательный мембранный потенциал, определяемый Na⁺ и K⁺, выталкивает Cl⁻ из клетки, в результате чего внутриклеточная концентрация Cl⁻ оказывается ниже внеклеточной. Этот концентрационный градиент приводит к обратному входу Cl⁻ в клетку, что точно противоположно электрическому выталкиванию. В отличие от этого, некоторые клетки обладают неэлектрогенной активной транспортной системой, выводящей Cl⁻ из клетки и создающей сильный концентрационный градиент. В таких клетках равновесный потенциал Cl⁻ отрицательнее мембранного потенциала покоя, и суммарная диффузия Cl⁻ внутрь клетки способствует дополнительному отрицательному заряду внутри, делая мембранный потенциал более отрицательным, чем он был бы при участии только Na⁺ и K⁺. Таким образом, вклад хлорида в мембранный потенциал покоя варьирует в зависимости от типа клетки и наличия у неё хлоридных транспортёров.
Сведения об авторах и источниках:
Авторы: Эрик П. Видмайер, Бостонский университет, Хершел Рафф, Медицинский колледж Висконсина, Медицинский центр Авроры Сент-Люк, Кевин Т. Странг, Университет Висконсин-Мэдисон
Источник: Физиология человека: механизмы функционирования организма
Данные публикации будут полезны студентам биологических и медицинских специальностей, начинающим специалистам в области клеточной биологии, биофизики и физиологии, а также всем, кто интересуется основами мембранного транспорта и регуляции клеточного гомеостаза.
Дата добавления: 2026-04-29; просмотров: 147;











