Возбудимость нейронов: мембранный потенциал, потенциалы действия и ионные каналы
Все клетки обладают мембранным потенциалом покоя благодаря работе ионных насосов, наличию концентрационных градиентов и каналов утечки в плазматической мембране. Однако некоторые клетки содержат дополнительные группы ионных каналов, которые при определённых условиях могут активироваться (открываться или закрываться), что позволяет генерировать электрические сигналы для передачи информации между различными участками мембраны. Это свойство называют возбудимостью, а соответствующие мембраны — возбудимыми мембранами. Нейроны и мышечные клетки представляют собой основные типы клеток, обладающих возбудимостью. Электрические сигналы проявляются в двух формах: градуированные потенциалы (локальные изменения) и потенциалы действия (распространяющиеся сигналы), где первые обеспечивают связь на короткие расстояния, а вторые — на большие, что критически важно для нервной и мышечной систем.
Направленные изменения мембранного потенциала. Термины «деполяризация», «реполяризация» и «гиперполяризация» описывают направленные изменения мембранного потенциала относительно уровня покоя в возбудимых клетках (рис. 6.14). Мембранный потенциал покоя называют поляризованным, что указывает на разность суммарных зарядов между наружной и внутренней сторонами мембраны. Деполяризация происходит, когда потенциал становится менее отрицательным (ближе к нулю), чем в покое; овершут (превышение) — это изменение полярности, при котором внутренняя сторона клетки становится положительной относительно наружной. Реполяризация — это возврат деполяризованной мембраны к состоянию покоя, а гиперполяризация — смещение потенциала в более отрицательную сторону.
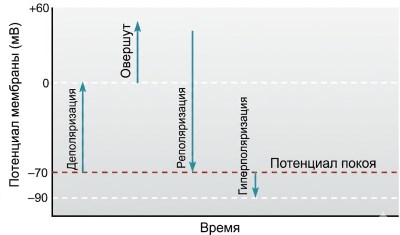
Рисунок 6.14. Деполяризующие, реполяризующие, гиперполяризующие изменения мембранного потенциала и овершут относительно потенциала покоя.
Ионные механизмы сигнальных изменений потенциала. Изменения мембранного потенциала, используемые нейронами в качестве сигналов, возникают вследствие изменений проницаемости клеточной мембраны для ионов. Как показано ранее, ионные каналы могут открываться или закрываться под действием механических, электрических или химических стимулов. Когда нейрон получает химический сигнал от соседней клетки, открываются определённые закрытые каналы, что увеличивает ионный ток через мембрану. Усиленное движение ионов вниз по их электрохимическим градиентам изменяет мембранный потенциал, вызывая либо деполяризацию, либо гиперполяризацию. Специфические свойства этих каналов в конечном счёте определяют тип генерируемого электрического сигнала.
Градуированные потенциалы: локальные изменения. Градуированные потенциалы представляют собой изменения мембранного потенциала, ограниченные небольшим участком плазматической мембраны; они возникают при воздействии определённых изменений окружающей среды на специализированные зоны мембраны. Название отражает тот факт, что величина изменения может варьироваться («градуироваться»). По локализации или функции различают рецепторные потенциалы, синаптические потенциалы и потенциалы кардиостимулятора (таблица 6.3). Когда возникает градуированный потенциал, заряд перемещается между исходным участком и соседними областями, сохраняющими потенциал покоя (рис. 6.15). Химический сигнал временно деполяризует небольшой участок мембраны, открывая катионные каналы, что создаёт менее отрицательный потенциал по сравнению с соседними зонами.

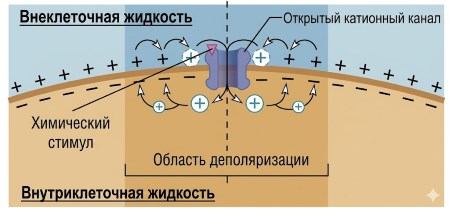
Рисунок 6.15. Деполяризация и градуированный потенциал, вызванные химическим раздражителем. Входящий положительный ток через лиганд-управляемые катионные каналы деполяризует участок мембраны, а локальные токи распространяют деполяризацию на соседние области.
Градуированные потенциалы могут быть как деполяризующими, так и гиперполяризующими (рис. 6.16а), а их амплитуда зависит от силы инициирующего события (рис. 6.16б). Из-за утечки заряда через постоянно открытые каналы, изменение мембранного потенциала затухает с расстоянием от места возникновения (рис. 6.16в). Плазматические мембраны настолько непроницаемы для ионов, что локальные токи практически исчезают в пределах нескольких миллиметров (рис. 6.17). Таким образом, градуированные потенциалы эффективны только на коротких расстояниях, однако при наложении нескольких стимулов до рассеяния первого может происходить суммирование, что особенно важно для сенсорных процессов (глава 7).
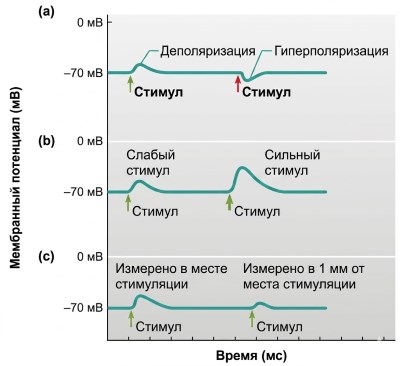
Рисунок 6.16. Градуированные потенциалы в экспериментальных условиях: (а) деполяризующие или гиперполяризующие, (б) варьирующие по величине, (в) затухающие с расстоянием. Потенциал покоя принят за –70 мВ.
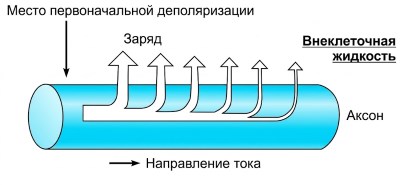
Рисунок 6.17. Утечка заряда (преимущественно K⁺) через плазматическую мембрану уменьшает локальный ток на участках, удалённых от места начальной деполяризации.
Потенциалы действия: быстрые изменения на большие расстояния. Потенциалы действия существенно отличаются от градуированных: это значительные изменения мембранного потенциала (до 100 мВ), например, деполяризация от –70 до +30 мВ с последующей реполяризацией. Эти сигналы очень быстрые (1–4 мс) и могут повторяться с частотой до сотен герц. Распространение потенциалов действия по аксону — основной механизм передачи сигналов на большие расстояния в нервной системе. Для понимания таких изменений необходимо изучить потенциал-зависимые ионные каналы (Voltage-gated channels), которые открываются при изменении напряжения на мембране.
Структура и функция потенциал-зависимых каналов. Существуют десятки типов потенциал-зависимых каналов, различающихся по проводимому иону (Na⁺, K⁺, Ca²⁺, Cl⁻) и кинетическим свойствам. В большинстве нейронов потенциалы действия опосредуются специфическими Na⁺- и K⁺-каналами (рис. 6.18). Оба типа содержат заряженные аминокислотные последовательности, обеспечивающие конформационные изменения в ответ на деполяризацию. При отрицательном мембранном потенциале (покой) каналы закрыты; деполяризация вызывает их открытие. Ключевые различия: (1) Na⁺-каналы реагируют быстрее и открываются раньше, чем K⁺-каналы; (2) Na⁺-каналы имеют дополнительный инактивационный затвор («шар и цепочка»), который блокирует пору вскоре после открытия, ограничивая поток Na⁺.
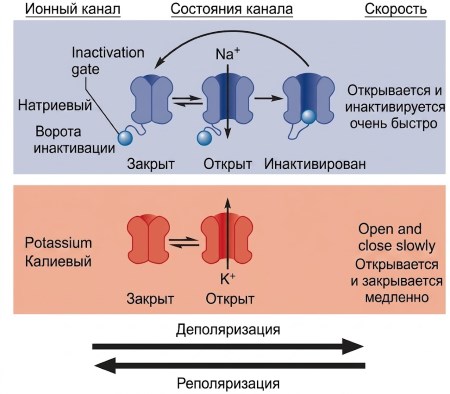
Рисунок 6.18. Поведение потенциал-зависимых Na⁺ и K⁺ каналов. Деполяризация вызывает быстрое открытие Na⁺-каналов, затем их инактивацию, после чего открываются K⁺-каналы. При реполяризации до отрицательных значений оба канала возвращаются в закрытое состояние.
Механизм генерации потенциала действия (пошагово). Интеграция свойств каналов с принципами мембранного потенциала объясняет возникновение потенциала действия (рис. 6.19). Этап 1: потенциал покоя близок к равновесному потенциалу K⁺ (около –90 мВ) из-за большего числа открытых K⁺-каналов утечки. Этап 2: деполяризующий стимул (например, связывание нейромедиатора с лиганд-зависимым каналом) открывает некоторые потенциал-зависимые Na⁺-каналы; при достижении порогового потенциала (около –55 мВ) запускается петля положительной обратной связи — вход Na⁺ усиливает деполяризацию, открывая всё новые Na⁺-каналы. Этап 3: быстрая деполяризация, мембранный потенциал стремится к равновесному потенциалу Na⁺ (+60 мВ), но не достигает его. Этап 4: инактивация Na⁺-каналов и открытие относительно медленных потенциал-зависимых K⁺-каналов. Этап 5: выход K⁺ из клетки реполяризует мембрану до уровня покоя. Этап 6: из-за медленного закрытия K⁺-каналов возникает следовая гиперполяризация. Этап 7: закрытие K⁺-каналов, возврат к потенциалу покоя (рис. 6.20).
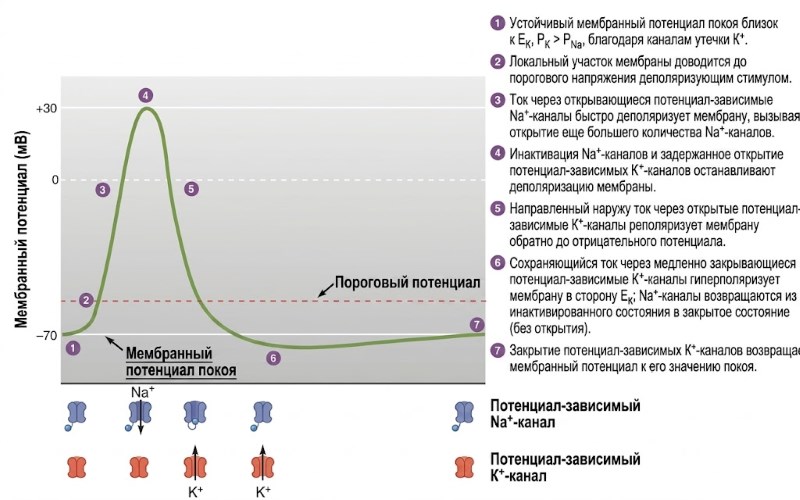
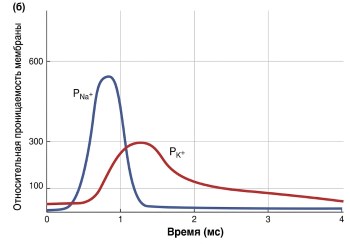
Рисунок 6.19. Изменения (а) мембранного потенциала и (б) относительной проницаемости (P) для Na⁺ и K⁺ во время потенциала действия. Этапы 1–7 описаны в тексте.
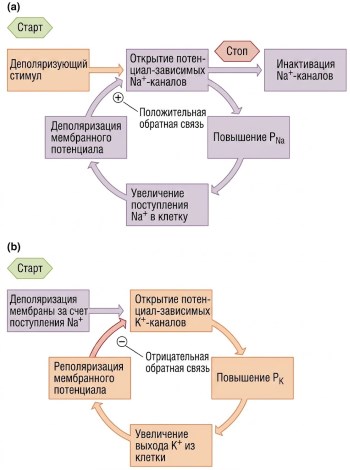
Рисунок 6.20. Обратная связь в потенциал-зависимых каналах: (а) Na⁺-каналы оказывают положительное влияние на мембранный потенциал; (б) K⁺-каналы — отрицательное.
Несмотря на значительные изменения потенциала, количество ионов, пересекающих мембрану за один импульс, ничтожно мало по сравнению с общим внутриклеточным пулом. Однако при повторных потенциалах действия градиенты Na⁺ и K⁺ могут рассеиваться, если бы не непрерывная работа Na⁺/K⁺-АТФазы, которая предотвращает накопление Na⁺ внутри клетки и потерю K⁺.
Порог, принцип «всё или ничего» и сила стимула. Потенциалы действия возникают только тогда, когда деполяризация достигает порогового уровня (примерно на 15 мВ положительнее потенциала покоя). Стимулы ниже порога вызывают подпороговые потенциалы, которые затухают. При достижении порога запускается необратимый цикл положительной обратной связи, и амплитуда потенциала действия не зависит от силы стимула — это принцип «всё или ничего» (рис. 6.21). Таким образом, информация о силе стимула кодируется не амплитудой одиночного импульса, а частотой потенциалов действия в единицу времени.
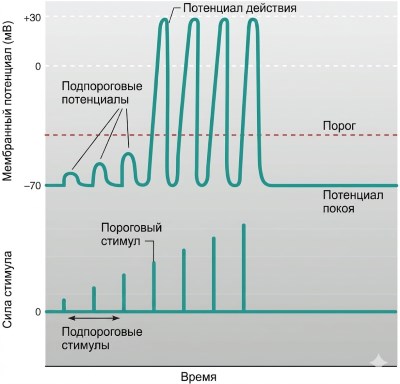
Рисунок 6.21. Изменения мембранного потенциала при увеличении силы возбуждающих стимулов. При достижении порога генерируются потенциалы действия; дальнейшее увеличение стимула не меняет их амплитуду.
Фармакологическая и токсикологическая модуляция. Местные анестетики (прокаин, лидокаин) блокируют потенциал-зависимые Na⁺-каналы, предотвращая генерацию потенциалов действия и, следовательно, проведение болевых сигналов. Некоторые животные вырабатывают токсины, нарушающие нервную проводимость. Например, тетродотоксин из рыбы фугу связывается с Na⁺-каналами и блокирует их; неправильно приготовленная фугу может быть смертельной.
Рефрактерные периоды: абсолютный и относительный. Во время потенциала действия наступает абсолютный рефрактерный период, когда второй стимул, какой бы силы он ни был, не может вызвать новый потенциал действия (рис. 6.22). Это связано с тем, что Na⁺-каналы либо открыты, либо инактивированы. Затем следует относительный рефрактерный период (до 15 мс), совпадающий с фазой следовой гиперполяризации: часть Na⁺-каналов ещё инактивирована, а некоторые K⁺-каналы остаются открытыми, поэтому для достижения порога требуется более сильный стимул. Рефрактерные периоды ограничивают максимальную частоту генерации потенциалов действия (обычно до 100 Гц) и обеспечивают однонаправленность распространения.
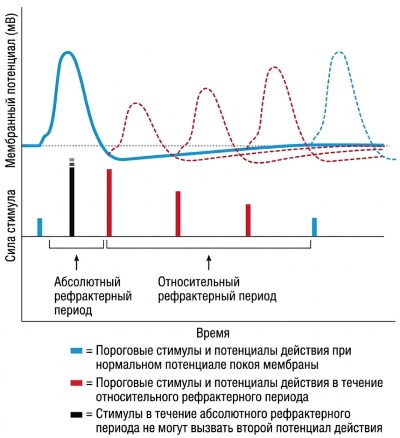
Рисунок 6.22. Абсолютный и относительный рефрактерные периоды, определённые методом парных стимулов. Во время абсолютного рефрактерного периода второй стимул не вызывает ответа; в относительном периоде возможен второй потенциал действия, но для достижения порога требуется более сильный стимул.
Механизмы распространения потенциала действия. Потенциал действия распространяется вдоль аксона благодаря тому, что локальные токи от активной зоны деполяризуют соседний участок мембраны до порога (рис. 6.23). Когда в области 1 генерируется потенциал действия, положительные заряды внутри клетки перемещаются к соседней покоящейся области 2, деполяризуя её и открывая там потенциал-зависимые Na⁺-каналы. Возникший новый потенциал действия, в свою очередь, деполяризует область 3. Поскольку область 1 находится в рефрактерном периоде, распространение идёт только в одну сторону — от недавно активных участков к ещё невозбуждённым. Потенциалы действия не затухают (недекрементальны), так как каждая новая точка генерирует полноценный импульс.
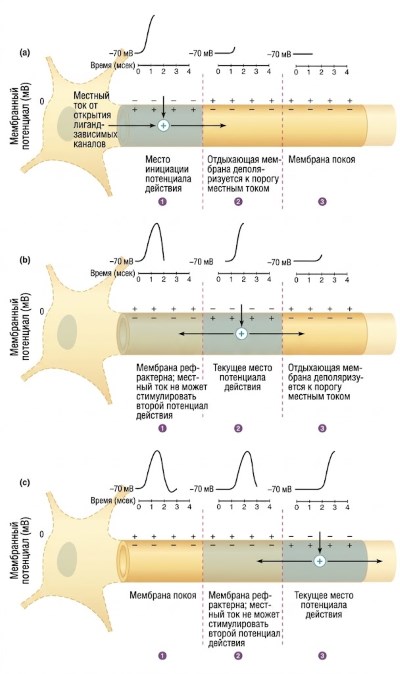
Рисунок 6.23. Однонаправленное распространение потенциала действия. (а) Локальный ток от инициирующей зоны деполяризует область 2. (б) Потенциал действия в области 2 генерирует токи, деполяризующие область 3; область 1 рефрактерна. (в) Потенциал действия в области 3, область 2 рефрактерна.
Факторы, влияющие на скорость проведения: диаметр и миелинизация. Скорость распространения потенциала действия зависит от диаметра аксона и наличия миелиновой оболочки. Чем больше диаметр, тем меньше внутреннее сопротивление и тем быстрее распространяется сигнал. Миелин действует как изолятор, уменьшая утечку заряда и увеличивая расстояние, на котором локальный ток остаётся эффективным. В миелинизированных аксонах потенциал-зависимые Na⁺-каналы сконцентрированы в перехватах Ранвье — участках, свободных от миелина. Потенциал действия «перескакивает» от одного перехвата к другому, что называется сальтаторной проводимостью (от лат. saltare — прыгать, рис. 6.24). Это значительно повышает скорость и энергоэффективность: миелинизированные аксоны тоньше и требуют меньше работы ионных насосов.
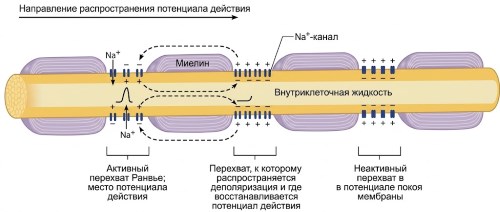
Рисунок 6.24. Миелинизация и сальтаторная проводимость. Потенциал действия генерируется только в перехватах Ранвье, где высока плотность Na⁺-каналов, и «перепрыгивает» между ними, что ускоряет проведение.
Скорости проведения варьируют от 0,5 м/с в тонких немиелинизированных волокнах до 100 м/с в толстых миелинизированных. Например, быстрая острая боль (миелинизированные волокна) достигает мозга практически мгновенно, тогда как тупая пульсирующая боль (немиелинизированные волокна) проводится медленнее.

Генерация потенциалов действия в разных типах нейронов. У афферентных нейронов начальная деполяризация до порога обеспечивается рецепторным потенциалом, генерируемым в сенсорных рецепторах на периферических окончаниях. В большинстве других нейронов деполяризация возникает либо за счёт синаптического потенциала (при синаптическом входе), либо за счёт спонтанных изменений — потенциала кардиостимулятора. Ключевые различия между градуированными потенциалами и потенциалами действия суммированы в таблице 6.4. Таким образом, понимание молекулярных и электрофизиологических механизмов возбудимости лежит в основе всей нейробиологии — от сенсорного восприятия до сложных когнитивных процессов и мышечного сокращения.
Сведения об авторах и источниках:
Авторы: Эрик П. Видмайер, Бостонский университет, Хершел Рафф, Медицинский колледж Висконсина, Медицинский центр Авроры Сент-Люк, Кевин Т. Странг, Университет Висконсин-Мэдисон
Источник: Физиология человека: механизмы функционирования организма
Данные публикации будут полезны студентам биологических и медицинских специальностей, начинающим специалистам в области клеточной биологии, биофизики и физиологии, а также всем, кто интересуется основами мембранного транспорта и регуляции клеточного гомеостаза.
Дата добавления: 2026-04-29; просмотров: 125;











