Порядок реакции равен сумме показателей степеней в уравнении закона скоростей.
Константа скорости реакции I порядка:
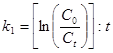
Для реакции II порядка константа скорости реакции: 
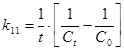
Константу скорости реакции для реакции I порядка можно определить по периоду полураспада:
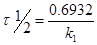
Каждая реакция характеризуется определенным энергетическим барьером для его преодоления необходима энергия активации 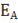 – некоторая избыточная энергия, которой должны обладать молекулы для того, чтобы их столкновение было эффективным, т. е. привело бы к образованию нового вещества. С ростом температуры число активных молекул быстро увеличивается, что и приводит к резкому увеличению скорости реакции.
– некоторая избыточная энергия, которой должны обладать молекулы для того, чтобы их столкновение было эффективным, т. е. привело бы к образованию нового вещества. С ростом температуры число активных молекул быстро увеличивается, что и приводит к резкому увеличению скорости реакции.
Зависимость const скорости реакции k от энергии активации ( 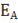 , Дж/моль) выражается уравнением Аррениуса:
, Дж/моль) выражается уравнением Аррениуса:
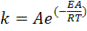 ,где
,где
А – коэффициент, связанный с вероятностью и числом столкновений активных молекул.
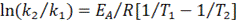 , где
, где
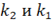 - const скорости реакции при
- const скорости реакции при 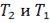
Расчет энергии активации:
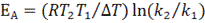
k = 2,72 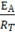
Катализ – этопроцесс, который заключается в изменении скорости химических реакций в присутствии веществ, называемых катализаторами.
Катализатор– это вещество, которое изменяет скорость химической реакции и участвует в ней, входит в состав промежуточных продуктов и после окончания реакции остается неизменным.
Катализаторы: соли, кислоты, оксиды, металлы. Могут находится в любом из трех агрегатных состояниях.
Классификация каталитических реакций:
1. положительный или отрицательный катализ
Положительный катализ – катализ, при котором скорость химической реакции увеличивается.
Отрицательный катализ – катализ, при котором скорость химической реакции уменьшатся.
Вещества, уменьшающие скорость химической реакции, называется ингибиторами.
2. Автокатализ
В этом случае катализатором может быть один из продуктов реакции.
Например: СН3 – СООС2Н5 + Н2О = СН3 СООН + С2Н5ОН.
Данная реакция катализируется уксусной кислотой.
3. гомогенный и гетерогенный катализ.
Гомогенный катализ – катализ, когда катализатор и реагирующие вещества находятся в одной фазе.
Гетерогенный катализ – катализ, когда катализатор и реагирующие вещества находятся в разных фазах.
Чаще всего катализатор – твердое вещество, а реагирующие вещества – жидкости или газы.
Дата добавления: 2019-12-09; просмотров: 844;











