Физические свойства
Газ без цвета, вкуса и запаха, самый лёгкий, t°пл = - 252,6°, t°кип = -259,1°С (ниже только у Не).
Уникальные свойства:
1. Очень теплопроводен; нагретое тело остывает в атмосфере водорода в 6 раз быстрее, чем в воздухе; это свойство роднит водород с металлами.
2. В воде растворим очень плохо (в 1 объёме воды растворяется 0,02 объёма водорода); но очень хорошо растворим в металлах (в 1 объёме палладия растворяется 900 объёмов водорода).
Получение водорода
1.В лаборатории: Zn + 2HCI = ZnCI2 + H2
2.В промышленности:
а)конверсия водяного газа (при повышенной to):
С + Н2О = СО + H2 , СО + Н2О = СО2 + H2
б)конверсия метана (при повышенной to ): СН4 + 2Н2О = СО2 + 4H2
3)В экспедиции (для радиозондов): LiH + Н2О = LiОH + H2
Химические свойства
1. В большинстве реакций водород – сильный восстановитель, но Н2 – не очень активен, а атомарный Н более реакционоспособен (Н2 - 2 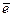 ® 2Н+)
® 2Н+)
а) с галогенами реакции идут по-разному
Н2 + F2 Þ 2HF (со взрывом, при низкой температуре и в темноте);
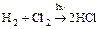 (реакция замещения, механизм свободно-радикальный);
(реакция замещения, механизм свободно-радикальный);
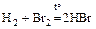 (идёт неполно);
(идёт неполно);
Н2 + J2 Û 2HJ.
б) 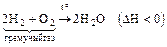 ;
;
г) 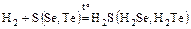 ;
;
д) 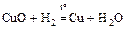 .
.
в) 3Н2 + N2 Û 2NH3;
2. Очень редко водород является окислителем (Н2 + 2 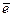 ® 2Н-)
® 2Н-)
2Li + H2 = 2LiH (гидрид).
Гидриды
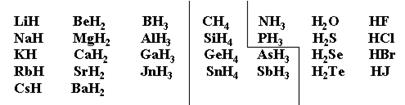

| Н-; ионные связи | Н- и Н+; связи близки к ковалентным неполярным | Н+; ковалентные полярные связи |
1) В зависимости от природы гидриды по-разному гидролизуются:
а) основной гидрид: 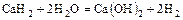 ;
;
б) кислотный гидрид: 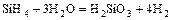 .
.
2) Это сказывается и на реакциях комплексообразования
КН – основной гидрид;
AlH3 – амфотерный;
ВН3 – кислотный.
а) КН + ВН3 ® К[ВН4]
б) КН + AlН3 ® К[AlН4]
в) AlН3 + 3ВН3 ® Al[ВН4]3.
ВОДА (Н2О)
- составляет 50 – 90% любого живого существа; самое распространённое вещество планеты.
Многие физические константы воды приняты за эталон:
t°пл. = 0°С;
t°кип. = 100°С;
плотность = 1 г/см3;
теплоёмкость = 1 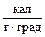 = 4,19
= 4,19 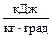 .
.
Валентные орбитали кислорода находятся в состоянии sр3-гибридизации, образуют искажённый тетраэдр, а молекула воды имеет угловую структуру:
угол НОН = 104°28¢ 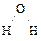 .
.
Поэтому молекулы Н2О очень полярны, что существенно сказывается на различных свойствах жидкой и твёрдой воды. Свойства обусловлены прежде всего структурой, образованием водородных связей (см. темы: химическая связь, электролитическая диссоциация, комплексные соединения). Жидкая и твердая вода существует в виде ассоциатов (Н2О)х.
Дата добавления: 2017-10-04; просмотров: 1189;











