Осмос, осмотическое давление
Осмос – самопроизвольная односторонняя диффузия растворителя через полупроницаемую перегородку в сторону выравнивания концентраций.
Иногда бывает двусторонняя диффузия: молекулы растворителя и растворённого вещества движутся в противоположных направлениях, но такое явление встречается реже. Можно выделить два вида полупроницаемых перегородок (мембран):
1) природные – стенки клеток, оболочки глаза, плавательный пузырь рыб;
2) искусственные – целлофан.
Выравнивание концентрации – это процесс самопроизвольный; термодинамически разрешённый: S > 0, G < 0.
1877 г. Пфеффер установил для идеальных растворов, что Росм. прямопропорционально:
а) концентрации растворённого вещества;
б) абсолютной температуре.
1887 г. Вант-Гофф вывел закон: осмотическое давление раствора равно тому давлению, которое производило бы при данной температуре вещество, будучи в газообразном состоянии и занимая объём, равный объёму раствора.
Росм. = 1000 CRT,
где Росм. в Па;
R – универсальная газовая постоянная;
Т – температура, град. К;
С – моль/л.
или
Росм.= CRT, где Росм. в кПа.
Если учесть, что
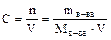 ,
,
то тогда
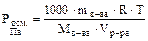 или
или 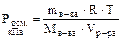 .
.
Этот закон выполняется для растворов неэлектролитов малых концентраций.
Пример: Найти молекулярную массу неэлектролита, если в 5 л раствора содержится 2,5 г вещества при температуре 20°С и Росм. = 2,3×104 Па.
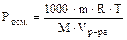 ; Т = 273 + t° = 293 К.
; Т = 273 + t° = 293 К.
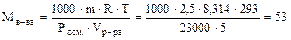 (г/моль).
(г/моль).
Изотонические растворы – растворы с одинаковым осмотическим давлением:
а) природные – кровь, лимфа, морская вода;
б) искусственные – физиологический раствор (0,9% NaCl), раствор глюкозы (5%).
Гипертонические растворы – растворы с высоким Росм. (10% NaCl).
Гипотонические растворы – растворы с низким Росм.
Тургор – осмотическое давление клеточного содержимого. Оно уравновешено эластичным напряжением клеточных стенок: Росм. внутри клетки больше Росм. во внеклеточной жидкости.
Плазмолиз – явление, связанное с погружением клетки в гипертонический раствор: клетка сморщивается, т.к. вода выходит из клетки.
Деплазмолиз - клетка в гипотоническом растворе: она разбухает, т.к. молекулы воды через мембрану идут внутрь клетки.
Пример: Осмотическое давление крови в норме 7,4 – 7,8 атмосферы (С » 0,3 моль/л). Снижение концентрации веществ в плазме крови ведёт к понижению Росм. до 3,6 – 4 атм, что в свою очередь приводит к гемолизу. Полный гемолиз наступает при Росм. = 3 атм: клетки начинают лопаться.
Дата добавления: 2017-10-04; просмотров: 1456;











