Получение сульфокислот
Сульфокислоты получают прямым сульфированием углеводородов или их производных.
Моносульфокислоты получают действием на бензол концентрированной серной кислоты на холоду:
 C6H6 + H2SO4 C6H5 – SO3H + H2O
C6H6 + H2SO4 C6H5 – SO3H + H2O
бензолсульфокислота
Выделяющаяся вода постепенно понижает концентрацию серной кислоты и ослабляет её сульфирующее действие.
1-ой характерной особенностью реакции сульфирования является её обратимость. В процессе реакции происходит гидролиз сульфогруппы, то есть идет реакция десульфирования. При понижении концентрации кислоты до 65% сульфирование прекращается, поэтому реакцию ведут в избытке концентрированной серной кислоты, то есть бензол вводят в кислоту, а не наоборот. Если кислоту вводят в бензол, то образуется побочный продукт реакции – дифенилсульфон:
 2 C6H6 + H2SO4 C6H5 – SO2 – C6H5 + 2 H2O
2 C6H6 + H2SO4 C6H5 – SO2 – C6H5 + 2 H2O
дифенилсульфон
Для отделения сульфокислот от серной кислоты пользуются различиями в растворимости их солей. Кальциевые и бариевые соли сульфокислот растворяются в горячей воде лучше соответствующих солей серной кислоты. Иногда выделяют сульфокислоты в форме натриевых солей высаливанием NaCl. Натриевые соли сульфокислот в этом случае оседают на дно.
Сульфокислоты являются сильными кислотами порядка силы серной кислоты.
Сульфирование проходит по обычному механизму SE2. Электрофильными реагентами сульфирования являются концентрированная серная кислота (92%-93%) или 100%-ный её моногидрат, олеум (раствор оксида серы(VI) 25-35% в H2SO4), хлорсульфоновая кислота (HO – SO2 – Cl) и так далее.
В серной кислоте активным электрофилом является гидросульфониевый ион, образующийся по схеме:

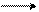 3 H2SO4 SO3H+ + H3O+ + 2 HSO4–
3 H2SO4 SO3H+ + H3O+ + 2 HSO4–



 O– H SO3H SO3H
O– H SO3H SO3H



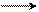

 SO3H+
SO3H+
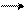
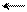
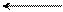
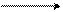


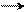
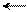


 + S3+ OH + + H+
+ S3+ OH + + H+
O–
сульфониевый π-комплекс σ-комплекс бензолсульфокислота
ион бензола и сульфо-иона сульфогруппы и
бензола
Еще более активным электрофилом является оксид серы (VI), являющийся сильной апротонной кислотой:
 2 H2SO4 SO3 + HSO4– + H3O+
2 H2SO4 SO3 + HSO4– + H3O+
Три атома кислорода сильно уменьшают электронную плотность на атоме серы в оксиде серы(VI) - SO3:


 O– O О
O– O О



 S2+= O или S+ – O– или Sδ+= Oδ–
S2+= O или S+ – O– или Sδ+= Oδ–
O– O О
2-ой характерной особенностью реакции сульфирования является наличие изотопного эффекта. Эта особенность реакции сульфирования заключается в том, что на скорость этой реакции оказывает влияние не образование σ-комплекса, как в других реакциях, идущих по механизму SE2, а диссоциация связи С – Н в σ-комплексе, то есть отрыв протона от него. Это означает, что в σ-комплексе связь С – Н существенно ослаблена и легко разрывается, в результате чего протон переходит к атому кислорода сульфогруппы:
изотопный эффект


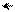
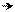





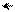
 O O O– O O–Н+
O O O– O O–Н+

 H S S
H S S

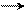


 S+ – O– медленно O быстро О
S+ – O– медленно O быстро О

 С6Н6 + SO3 +
С6Н6 + SO3 +
O
π-комплекс σ-комплекс бензолсульфокислота
(биион)
Дата добавления: 2017-01-16; просмотров: 2779;











