Алюминий и его соединения: получение, физические и химические свойства. Медико-биологическое значение алюминия.
Алюми́ний — элемент главной подгруппы третьей группы третьего периода периодической системы химических элементовД. И. Менделеева, с атомным номером 13. Обозначается символом Al (лат. Aluminium). Относится к группе лёгких металлов. Наиболее распространённый металл и третий по распространённости химический элемент в земной коре (после кислорода икремния).
Простое вещество алюминий (CAS-номер: 7429-90-5) — лёгкий, парамагнитный металл серебристо-белого цвета, легко поддающийся формовке, литью, механической обработке. Алюминий обладает высокой тепло- и электропроводностью, стойкостью к коррозии за счёт быстрого образования прочных оксидных плёнок, защищающих поверхность от дальнейшеговзаимодействия.
Получение
Современный метод получения был разработан независимо американцем Чарльзом Холлом и французом Полем Эру в 1886 году. Он заключается в растворении оксида алюминия Al2O3 в расплаве криолита Na3AlF6 с последующим электролизом с использованием расходуемых коксовых или графитовых электродов. Такой метод получения требует больших затрат электроэнергии, и поэтому оказался востребован только в XX веке.
Для производства 1000 кг чернового алюминия требуется 1920 кг глинозёма, 65 кг криолита, 35 кг фторида алюминия, 600 кг анодной массы и 17 тыс. кВт·ч электроэнергии постоянного тока.[2]
Алюминий — очень активный металл. В ряду напряжений он стоит после щелочных и щелочноземельных металлов. Однако на воздухе он довольно устойчив, так как его поверхность покрывается очень плотной пленкой оксида, предохраняющей металл от контакта с воздухом. Если с алюминиевой проволоки снять защитную оксидную пленку, то алюминий начнет энергично взаимодействовать с кислородом и водяными парами воздуха, превращаясь в рыхлую массу — гидроксид алюминия:
4 Аl + 3 O2 + 6 Н2О = 4 Аl(ОН)3
Эта реакция сопровождается выделением теплоты.
Очищенный от защитной оксидной пленки алюминий взаимодействует с водой с выделением водорода:
2 Аl + 6 Н2О = 2 Аl(ОН)3 + 3 Н2
Алюминий хорошо растворяется в разбавленных серной и соляной кислотах:
2 Аl + 6 НСl = 2 AlСl3 + 3 Н2
2 Аl + 3 Н2SO4 = Аl2(SO4)3 +3 Н2
Разбавленная азотная кислота на холоду пассивирует алюминий, но при нагревании алюминий растворяется в ней с выделением монооксида азота, гемиоксида азота, свободного азота или аммиака, например:
8 Аl + 30 НNО3 = 8 Аl(NО3)3 + 3 N2О + 15 Н2О
Концентрированная азотная кислота пассивирует алюминий.
Так как оксид и гидроксид алюминия обладают амфотерными свойствами, алюминий легко растворяется в водных растворах всех щелочей, кроме гидроксида аммония:
2 Аl + 6 КОН + 6 Н2О = 2 К3[Аl(ОН)6] + 3 Н2
Порошкообразный алюминий легко взаимодействует с галогенами, кислородом и всеми неметаллами. Для начала реакций необходимо нагревание, затем они протекают очень интенсивно и сопровождаются выделением большого количества теплоты:
2 Аl + 3 Вr2 = 2 АlВr3 (бромид алюминия)
4 Аl + 3 O2 = 2 Аl2O3 (оксид алюминия)
2 Аl + 3 S = Аl2S3 (сульфид алюминия)
2 Аl + N2 = 2 АlN (нитрид алюминия)
4 Аl + 3 С = Аl4С3 (карбид алюминия)
Сульфид алюминия может существовать только в твердом виде. В водных растворах он подвергается полному гидролизу с образованием гидроксида алюминия и сероводорода:
Аl2S3 + 6 Н2О = 2 Аl(ОН)3 + 3 Н2S
Алюминий легко отнимает кислород и галогены у оксидов и солей других металлов. Реакция сопровождается выделением большого количества теплоты:
8 Al + 3 Fе3О4 = 9 Fе + 4 Аl2O3
Процесс восстановления металлов из их оксидов алюминием называется алюмотермией. Алюмотермией пользуются при получении некоторых редких металлов, которые образуют прочную связь с кислородом (ниобий, тантал, молибден, вольфрам и др.), а также для сваривания рельсов. Если с помощью специального запала поджечь смесь мелкого порошка алюминия и магнитного железняка Fе3О4 (термит), то реакция протекает самопроизвольно с разогреванием смеси до 3500 °С. Железо при такой температуре находится в расплавленном состоянии.
Применение.
Гидроксид алюминия обладает свойствами поглощать различные вещества, поэтому его применяют при очистке воды.
Сравнительно высокие прочностные характеристики, хорошую тепло- и электропровод-ность, технологичность, высокую коррозионную стойкость. Совокупность этих свойств позволяет отнести алюминий к числу важнейших технических материалов.
Применяется в авиации, судостроение, машиностроение, нефте- газовой промышленности, строительстве.
Алюминий – это микроэлемент. Содержание в организме: 1*10-5% в сыворотке крови, легких, печени, костях, почках, входит в структуру оболочек нервных клеток головного мозга человека. Принимает участие в построении эпителиальной и соединительной тканей, в процессе регенерации костной ткани, в обмене фосфора.
В медицине применяются:
1. Алюмокалиевые квасцы KAl(SO4)2*12 H2O, обладают вяжущим, прижигающим и кровоостанавливающим действием.
2. Гидроксид алюминия Al(OH) 3 , обладает адсорбирующим и обволакивающим действием, понижает кислотность желудочного сока, входит в состав препарата «Альмагель».
Металлы главной подгруппы II группы: общая характеристика, получение, физические и химические свойства. Соли кальция и магния. Жесткость воды. Устранение жесткости воды. Медико-биологическое значение элементов главной подгруппы II группы.
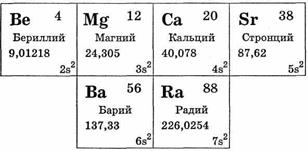
В главную подгруппу II группы входят бериллий Be, магний Mg, кальций Са, стронций Sr, барий Ва, радий Ra. Из них кальций, стронций, барий относятся к семейству щелочноземельных металлов.
Это s-элементы. В виде простых веществ типичные металлы. На внешнем уровне имеют по два электрона. Отдавая их, они проявляют в соединениях степень окисления +2. В окислительно-восстановительных реакциях все металлы подгруппы ведут себя как сильные восстановители, однако несколько более слабые, чем щелочные металлы. Это объясняется тем, что атомы металлов II группы имеют меньшие атомные радиусы, чем атомы соответствующих щелочных металлов, расположенных в тех же периодах. Это связано с некоторым сжатием электронных оболочек, так как s-подуровень внешнего электронного слоя у них завершен, поэтому электроны ими удерживаются сильнее.
Дата добавления: 2016-06-22; просмотров: 8944;











