Химические свойства сульфокислот
Реакции сульфокислот можно разделить на 3 группы:
1) реакции, идущие по сульфогруппе;
2) реакции замещения сульфогруппы другими остатками;
3) реакцие, идущие по бензольному ядру.
1) Реакции, идущие по сульфогруппе
Как сильные кислоты ароматические сульфокислоты взаимодействуют с щелочами, гидроксидами щелочноземельных металлов и органическими соединениями, образуя не гидролизующиеся водой соли. Например, взаимодействие с водным раствором гидроксида натрия:
 C6H5 – SO3H + NaOH C6H5 – SO3Na + H2O
C6H5 – SO3H + NaOH C6H5 – SO3Na + H2O
бензолсульфонат натрия
(натриевая соль бензолсульфокислоты)
Бензолсульфонат натрия применяется в качестве детергента или как моющее средство. Эти соли лучше растворимы в жесткой воде и не образуют хлопьев.
При нагревании солей сульфокислот с РСl5 образуются хлорангидриды, которые применяются как ацилирующие агенты. Полученные хлорангидриды, взаимодействуя с аммиаком, образуют амиды сульфокислот, превращающиеся при хлорировании в хлорамиды соответствующих кислот, которые упрощенно называются «хлорамины»:




 SO2OH SO2ONa SO2Cl SO2NH2 SO2-NH-Cl
SO2OH SO2ONa SO2Cl SO2NH2 SO2-NH-Cl
 |  |  |  |  |




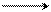
 NaOH PCl5 2NH3 NaOCl
NaOH PCl5 2NH3 NaOCl
–H2O –NaCl, –POCl3 –NH4Cl –NaOH
 |  |  |  |  |
CH3 CH3 CH3 CH3 CH3
п-толуолсульфо- п-толуолсульфонат п-толуолсульфо п-толуолсульфо монохлорамид
кислота натрия хлорид амид п-толуолсульфо-
(амид п-толуолсульфокислоты) кислоты
(хлорамин)
Хлорамины, гидролизуясь, дают хлорноватистую кислоту (НОCl), которая является антисептиком, что нашло применение их для очистки воды.
Из бензолсульфохлоридов или бензолсульфокислот при восстановлении их цинковой пылью в кислоте образуются тиофенолы:
 C6H5 – SO3H + 3 Zn + 6 HCl C6H5 – SH + 3 ZnCl2 + 3 H2O
C6H5 – SO3H + 3 Zn + 6 HCl C6H5 – SH + 3 ZnCl2 + 3 H2O
тиофенол
Ряд важнейших антибиотических лекарств (сульфоамидные препараты) представляют собой производные амидов сульфокислот, например:


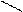



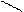


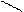 N NH
N NH



 H2N SO2NH ; H2N SO2-NH2-C
H2N SO2NH ; H2N SO2-NH2-C
N NH2
сульфадиазин сульфагуанидин
Дата добавления: 2017-01-16; просмотров: 4796;











