Реакции гидратации алюмината с участием сульфатов
Для регулирования сроков схватывания цемента при помоле клинкера добавляют 4-5 % гипсового камня. В противном случае будет происходить так называемое «ложное схватывание», когда цементный порошок смешиваете с водой он начинает сразу загустевать и схватываться. По ГОСТ 10178-85 начало схватывания цементного теста должно наступать не ранее 45 минут, конец схватывания должен наступать не позднее 10 часов. Сроки схватывания цемента определяют на приборе Вика.
В качестве регулятора сроков схватывания цемента используют двуводный сульфат кальция CaSO4·2H2O (короткая формула CsHx). Регулятором является в основном дигидрат или полугидрат, или смеси обоих видов сульфата кальция. При помоле клинкера с добавками в трубных шаровых мельницах происходит сильный нагрев цемента, так как затрачиваемая на процесс помола энергия используется непосредственно для измельчения лишь частично. Следовательно, при высокой температуре двуводный гипс полностью или частично может дегидратироваться до полуводного. Общее количество вводимого сульфата и отношение введенного дигидрата и полугидрата должно быть согласовано с реакционной способностью клинкера и требованиями в отношении установления поведения цемента (сроков схватывания). Высокое содержание CaSO4·nH2O задерживает сроки начала и конца схватывания цемента до необходимых пределов. В зависимости от концентрации регулятора схватывания могут иметь место различные реакции: если содержание CaSO4·nH2O высокое то С3А реагирует с водой и CaSO4 с образованием соединения, которое называется "эттрингит" (по названию одноименной местности Ettringen в Эйфеле) (уравнение 19). Так как в одном моле эттрингита связано три моля CaSO4, то его также называют "трисульфат" (трехсульфатная форма гидросульфоалюмината кальция ГСАК-3), или в английской литературе как "AFt - фазы". Если в реакционной смеси в настоящее время есть небольшое количество сульфата, то это может обеспечить низкую скорость растворения и реакция алюмината приводит к образованию "моносульфата" (моносульфатной формы гидросульфоалюмината кальция), который также называют "AFm-фаза" (уравнение 20). Формирование моносульфата может также происходить при местном недостатке сульфата кальция (гипса). В дальнейшем ходе гидратации цемента при увеличении концентрации сульфата кальция содержание кристаллов эттрингита будет увеличиваться. Однако эттрингит устойчив только при концентрациях сульфата кальция > 2,35 мг SO42-/л. При снижении этой концентрации в поровой жидкости цементного камня эттрингит становится неустойчивым; он изменяется (переходит) в соответствии с уравнением 21 при взаимодействии с остаточной С3А и водой в моносульфатную форму. Это означает, что концентрация эттрингита при гидратации проходит через максимум, а затем снова уменьшается; одновременно со снижением концентрация эттрингита происходит увеличение концентрации моносульфата.
Высокая концентрация сульфата:
C3A + 3CsH2 + 26H → C3A·3Cs·H32 Уравнение 19
Эттрингит, AFt-фазы
Низкая концентрация сульфата:
C3A + CsH2 + 10H → C3A·Cs·H12 Уравнение 20
Моносульфат, AFm-фазы
Реакция эттрингита с С3А:
C3A + C3A·3CsH32 + 4H → 3C3A·Cs·H12 Уравнение 21
Моносульфат
Реакция алюмината с сульфатом происходит как в ранее описанной реакции хотя и очень быстро, то есть, в течение нескольких минут. ESEM микрофотографии показывают, однако, то что первоначально образованный "первичный" эттрингит в отличие от С-S-H фазы не занимает поровое пространство. Скорее всего, он формируется в виде компактного, очень короткопризменного эттрингита (до 500 нм), который покрывают поверхность С3А или цементного зерна. Благодаря этой "пассивации" происходит продление срока схватывания цементного теста, в течение которого вы можете обрабатывать строительный материал, приготовить и заформовать бетонное изделие. Пассивация не является постоянной, а поверхность гидратирующих частиц цемента частично проницаема для воды и ионов сульфата. Дальнейший ход и скорость гидратации поэтому контролируется скоростью диффузии. Таким образом, на границе раздела С3А/эттрингит реакция идет медленно (почти полностью затормаживается), на поверхности гидратирующей частицы цемента образуется плотная пленка, которая не пропускает воду внутрь, наступает индукционный период. Дальнейшее образование эттрингита и других гидратов внутри пленки приводит к разрыву пленки на поверхности гидратирующей частицы цемента, вода начинает проникать внутрь, наружу выходят продукты гидратации и происходит интенсивная гидратация клинкерных минералов. Благодаря этому процессу и параллельно происходящей перекристаллизацией эттрингита из длинных кристаллов (волокон) в хорошо оформленные кристаллы эттрингита (длина 2,5 мк), реакция С3А усиливается. На рисунке 1.35 показано, как вместо длинных волокон эттрингита после гидратации в течение 4 час в цементной структуре образуются кристаллы в форме кирпича. Для достижения полной конверсии С3A в эттрингит, количество и растворимость поставляемых сульфатных ионов должно [4, 5, 33, 121] очень точно соответствовать реакционной способности С3А. На практике это случается редко. Часто равновесие между эттрингитом, моносульфатом и гидроксидом кальция нарушается. В зависимости от соотношения С3А/CsH2 гидратными продуктами, перечисленными в таблице 1.21, могут быть.
Таблица 1.21- Ожидаемые продукты гидратации при различных соотношениях C3А/CsH2
| С3А/Cs H2 | Продукт гидратации |
| >3 | эттрингит и свободный гипс |
| 3,0 | эттрингит |
| 1,0... 3,0 | эттрингит и моносульфат |
| 1,0 | моносульфат |
| <1,0 | моносульфат и C4AH13, C2AH8 соответственно С3А(Cs,CH)Н12 |
| C3AH6 |
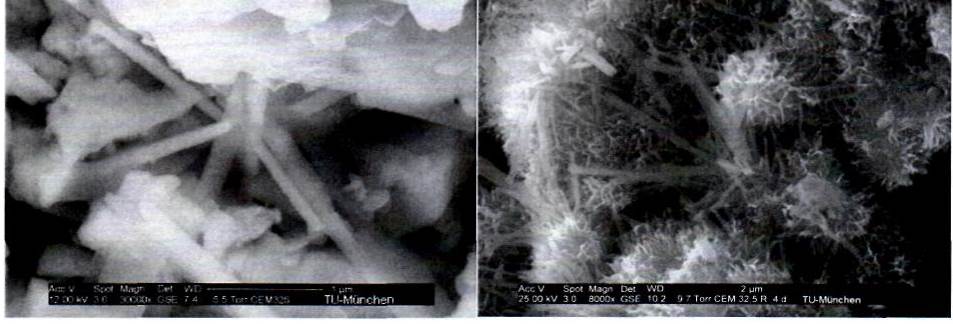
Рисунок 1.35 - Образование эттрингита при гидратации цемента; Слева: кристаллы эттрингита сформировавшиеся через 2 ч гидратации; справа: удлиненные кристаллы эттрингита (длина 1-2,5 мкм) через 4 ч гидратации в структуре CEM I 32,5R
Временные изменения эттрингита, размер и габитус кристаллов могут быть получены с помощью дополнительных химических агентов [131]. Это имеет большое значение для технологичности раствора или бетона. Изображения с высоким разрешением также показывают, что эттрингит часто образуется полисинтетическим или полым (рисунок 1.36).
При определенных обстоятельствах, при тепловой обработке бетона может образоваться "поздний" эттрингит (англ. "Задержка образования Ettringites"). Их не следует путать с формированием первичного или вторичного эттрингита в пределах нормальной гидратации. Тепловая обработка бетона в процессе твердения и развития прочности должны быть ускорены до распалубки. Если температура превышала 70 °С, то в ходе процесса гидратации может предпочтительно образоваться моносульфатная форма вместо эттрингита. Причиной является низкая термическая стабильность эттрингита. Он легко преобразуется при нагревании, выделяя воду и сульфат в моносульфатном порядке. Часть сульфата не связана, как AFm или AFt кормовой части, но, как правило, включены в C-S-H-фазы. В затвердевшем состоянии моносульфат может затем реагировать с сульфатами, которые были включены в C-S-H-фазы с образованием эттрингита. Эта реакция протекает очень медленно. В отличие от раннего формирования эттрингита в пластическом состоянии, это приводит к образованию позднего эттрингита и расширению объема, которые могут привести к разрушению термообработанного бетона не через несколько месяцев, а, как правило, только после нескольких лет [132].
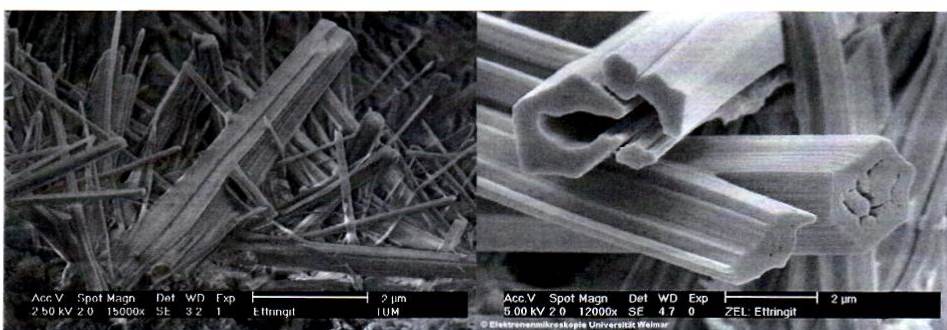
Рисунок 1.36-Эттрингит, полисинтетическим побратимом (слева) и полые (справа)
1.1.10.3 Гидратация феррита (C4AF)
Гидратация C4AF является одним из сегодняшних наименее понятных процессов в гидратации цемента. Например, непонятно, почему чистый C4AF замечательно взаимодействует с водой в то время как C4AF в составе цемента очень медленно реагирует с водой. Последнее является трудно объяснимым процессом. До сих пор неясно, каким образом железо включено в гидратные продукты. Вот описание двух моделей, которые предлагаются авторами. Первый из них описывает разработанную Тейлором идею гидратации к железистому эттрингиту (AFt = Алюминатферрит - трисульфат) и моносульфат; вторая модель основана на последних результатах исследований по ESEM Ф. А. Фингер - Институт проблем материаловедения в Веймаре. В целом было отмечено, что с увеличением содержания железа в алюмоферрите (как C6AF2 в смешанный кристалл серии C2A .... C2F) гидратация идет медленнее [5, 121, 120, 133].
Модель Тейлора
Однако гидратные продукты C4AF являются кальциевоалюминатноферритными гидратами. Аналоговая гидратация С3А состав зависит от содержания сульфата. При отсутствии носителя сульфата первоначально формируются в соответствии с уравнением 22 кальциевый гидроалюмоферрит как промежуточный продукт и смесь железа и алюминия:
2С4AF + 32H → C4(A,F)H13 + 2С2(A,F) + (A,F)H3 Уравнение 22
Нестабильные промежуточные продукты преобразуются в соответствии с уравнением 23 в кристаллы пластинчатой фазы:
C4(A,F)H13 + 2С2(A,F) → 2C3(A,F)H6 +9H Уравнение 23
В присутствии носителя сульфата в форме железистого эттрингита при гидратации первоначально (Алюминат феррит трисульфат, AFt) и, возможно, позднее (в зависимости от сульфатно-листинга) Алюминат феррит-моносульфат (AFm) протекает реакция:
3C4AF + 12CsH2 + 110H → 4C3(A,F)·3CsH32 + 2(A,F)H3 Уравнение 24
Eisenettringit, Aft
4C3(A,F)·3Cs·H32+3C4AF+12CsH2+14H→4C3(A,F)∙CsH12+2(A,F)H3 Урав-е 25
Алюминатферрит-моносульфат, AFm
Модель Старка
Согласно этой модели, относительно медленная гидратация C4AF объясняется выщелачиванием алюминия из зерен C4AF. Это происходит таким образом, что в растворе алюминат реагирует так же, как чистый С3А с эттрингитом с помощью сульфата и Са(ОН)2. Он сформировал Аl-истощенные и, таким образом, Fe-обогащенные зерна C4AF, которые после долгого времени гидратации были все еще видны в микроструктуре. Так как выщелачивание происходит относительно медленно, сульфат-носитель, как правило, быстро переходит в раствор, это может привести к временному образованию вторичного гипса в микроструктуре затвердевшего цементного теста. Эта штукатурка снова исчезает, как только в дальнейшем сульфат необходим для образования эттрингита выщелоченного алюмината. В результате, гидратация C4AF первоначально приводит к образованию безжелезистого эттрингита, который превращается в моносульфат и вторичный гипс позже. Поддерживается, среди прочего, нами тот факт, что, вопреки идее Тейлора - это не гидроксид железа. Для полного прояснения процессов гидратации C4AF необходимы безусловно дальнейшие исследования.
Дата добавления: 2016-10-26; просмотров: 4994;











