Основы термодинамики
21. Удельные теплоемкости газа при постоянном объеме (cV) и при постоянном давлении (cp):
 ;
;  .
.
22. Связь между удельной (с) и молярной (Сm) теплоемкостями:
c = Cm/m; Cm = cm.
23. Уравнение Роберта-Майера:
Cmp – CmV = R.
24. Внутренняя энергия идеального газа :
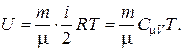
25. Первое начало термодинамики:
Q = DU + A,
где Q – теплота, сообщенная системе (газу); DU – изменение внутренней энергии системы; A – работа, совершенная системой против внешних сил.
26. Работа расширения газа:
в общем случае  ;
;
при изобарическом процессе A = p(V2 – V1);
при изотермическом процессе  ;
;
при адиабатическом процессе 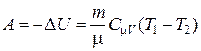 ,
,
или  ,
,
где g = сp/cV – показатель адиабаты.
27. Уравнения Пуассона, связывающие параметры идеального газа при адиабатическом процессе:
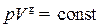 ,
,  ;
;
 ;
; 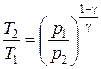 .
.
28. Термический к.п.д. цикла:
 ,
,
где Q1 – теплота, полученная рабочим телом от нагревателя; Q2 – теплота, переданная телом охладителю.
29. Термический к.п.д. цикла Карно:
 ,
,
где T1 и T2 – термодинамические температуры нагревателя и охладителя.
30. Разность энтропий SB – SA двух состояний В и А определяется формулой:
 .
.
Дата добавления: 2016-07-22; просмотров: 1130;











