Полимеры, аморфные тела и керамика
Полимеры. Такими называют вещества с большой молекулярной массой (>104), в которых молекулы построены из большого числа повторяемых структурных единиц – звеньев. Каждое звено представляет собой измененную молекулу исходного низкомолекулярного вещества – мономера. При получении полимеров молекулы мономеров соединяются друг с другом ковалентными связями и образуют макромолекулы. Число n, показывающее сколько раз звено повторяется в молекуле, называется степенью полимеризации и может достигать сотен тысяч и больше.
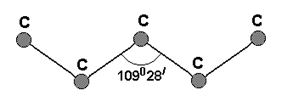
Скелет органической полимерной молекулы состоит из атомов углерода, в которых ковалентные связи носят направленный характер. Поэтому атомы углерода располагаются в вершинах ломаной линии (рис.1.23), звенья которой образуют друг с другом угол в 1100, названный валентным углом. На образование скелета атом углерода использует две связи, другие идут на обрамление. В случае полиэтилена обрамления осуществляется атомами водорода Н, в других случаях могут стоять атомы других элементов или группы атомов – гидроксильные (ОН), метильные (СН3) и т.д. Их называют боковыми заместителями.
|
| Рис. 1.23. Строение скелета молекулы органического полимера |
В большинстве линейных полимеров скелет состоит преимущественно из атомов углерода, у кремнийорганических полимеров он образован атомами кремния и кислорода, которые чередуются.
При наличии в полимере боковых групп нескольких видов есть возможность разместить их вдоль скелета как неупорядочено, так и упорядочено. В первом случае полимеры называются нерегулярными, во втором – регулярными.
Рядом с линейными полимерами существуют разветвленные и пространственные (сетчатые полимеры). Разветвленные полимеры, кроме главной цепи, содержат боковые цепи, число, длина и природа которых могут быть различными. У сетчатых полимеров длинные макромолекулы соединены между собой поперечными связями.
В зависимости от характера связей между линейными молекулами полимеры разделяются на термопластические и термореактивные. Термопластические полимеры способны многократно размягчаться при нагревании и отвердевать при охлаждении без изменения своих свойств. Термореактивные полимеры при нагревании остаются твердыми вплоть до полного термического разложения. Это расхождение в поведении при нагревании объясняется тем, что в термопластических полимерах между молекулами действуют относительно слабые молекулярные (вандерваальсовы) силы. При нагревании связи между молекулами значительно ослабляются, материал становится мягким и податливым. У термореактивных полимеров, кроме упомянутых сил, есть поперечные ковалентные связи между молекулами, благодаря чему термореактивный материал остается твердым при нагревании.
Макромолекулы в полимерном веществе не упакованы плотно, и мерой плотности упаковки служит свободный объем, то есть разница между фактическим удельным объемом вещества и теоретическим удельным объемом при самой плотной упаковке. В зависимости от свободного объема полимер находится в одном из физических состояний: стекловидном, высокоэластичном, вязкотекучем.
Расхождение между физическими состояниями полимеров наглядно оказывается при деформации. В стекловидном состоянии повороты вокруг связей в макромолекулах усложнены, полимер является упругим твердым телом. Под нагрузкой упругая деформация не превышает нескольких процентов и падает до нуля при снятии нагрузки. При деформации происходит искажение валентных углов.
Высокоэластичное состояние оказывается тогда, когда свободный объем достигает 2,5%. В этом состоянии полимер ведет себя как эластичное тело. Под нагрузкой скрученные макромолекулы выпрямляются и вытягиваются, деформация достигает 500-800%. Расстояния между атомами в макромолекулах при этом меняются незначительно. При снятии нагрузки тепловое движение возвращает макромолекулы к равновесным формам, и поэтому высокоэластичная деформация обратима.
В вязкотекучем состоянии полимер ведет себя как вязкая жидкость. Под действием нагрузки макромолекулы выпрямляются и скользят относительно друг друга, и главную часть деформации составляет необратимое вязкое течение. Течение прекращается после прекращения действия нагрузки, и вязкая жидкость сохраняет полученную форму.
Полимеры обладают замечательными свойствами. Они сочетают высокую механическую прочность с высокими деформационными свойствами и высокой адгезией. У пространственных полимеров прочность, как правило, выше, чем у соответствующих им линейных полимеров.
Полимеры проявляют исключительную химическую стойкость, превосходя благородные металлы. В электрическом отношении они имеют низкие диэлектрические потери, высокие объемные и поверхностные сопротивления, высокую электрическую прочность и т.д.
Легкость формирования изделий из полимеров и их механической обработки, возможность получения тонких пленок и волокон и на их основе изготовления различных конструкционных материалов является основой широкого применения полимеров в радиоэлектронике.
Аморфные тела. Для выяснения понятия «аморфный» стоит пояснить различие между ближним и дальним порядками. Пространственным ближним порядком в области к первому и второму соседним атомам обладают все твердые и жидкие материалы. Периодический атомный порядок в кристалле называется дальним, если он распространяется на 10-100 атомных расстояний, как, например, в мелкокристаллических материалах. Аморфными или стекловидными называются твердые тела, которые не обладают дальним порядком. Атомы такого материала располагаются в непрерывной, беспорядочной пространственной сетке.
Стекловидное состояние в отличие от аморфного характеризуется еще и наличием длинных цепей – связей в материале. Стеклообразующими являются окислы SiO2, B2O3, P2O5, GeO2, а также некоторые бескислородные соединения мышьяка, селена, теллура.
Обычное силикатное стекло построено из кремнекислородных тетраэдров SiO4, которые соединяются своими вершинами, образуя трехмерную сетку. Из таких же тетраэдров состоит структура кристаллического кварца. Расхождение между двумя веществами одинакового химического состава объясняется размещением тетраэдров. Углы между связками кремний – кислород в соседних тетраэдрах в кварцевом стекле меняются в широких границах (120– 1800), чем и объясняется неупорядоченное расположение тетраэдров. В кристаллическом кварце тетраэдры расположенные упорядочены и образуют кристаллические решетки. Структура аморфного стекла возникает при охлаждении стеклянной массы, когда повышению ее вязкости препятствует кристаллизации.
Основная масса промышленного стекла, кроме SiO2, содержит окислы других металлов, которые при варке образуют однородную структуру. В зависимости от природы вводимых окислов стекло называют натриевым, свинцовым и т.д. Эти стекла по сравнению с кварцевым стеклом размягчаются при более низких температурах. Ионы металлов могут присоединяться к ненасыщенным связям атомов кислорода кремний кислородных тетраэдров, размещаясь в пустотах трехмерной сетки и локально обрывая ее. Эти ионы имеют значительную подвижность и обусловливают ионную проводимость стекла.
Усложнение химического состава силикатного стекла приводит к изменению его свойств, в том числе и цвета, и является причиной структурной неоднородности. При охлаждении однофазный расплав расслаивается на две или несколько фаз разного химического состава, что и обусловливает многофазную структуру затвердевшего стекла. Расслоение силикатных стекол – характерная черта их структуры.
При определенном соотношении кремния, кислорода и других элементов возможно зарождение и рост кристаллов в стекле, что негативно влияет на прочность. Кристаллизацию предупреждают подбором химического состава стекла и условий его варки.
Напряжения в стеклянных изделиях устраняют нагреванием, температура которого достаточна для перестройки структурных элементов и выравнивания плотности.
Керамика. Это материалы, получаемые при высокотемпературном спекании минеральных порошков. Керамика является пористым материалом, который содержит кристаллические и аморфные фазы, хотя отдельные виды керамики совсем не имеют стекла в своей структуре. Как правило, керамика имеет поликристаллическую структуру с прослойками стекла и с беспорядочным расположением зерен. Кристаллические зерна являются сложными окислами, карбидами или твердыми растворами на их основе с ковалентными или ионными связями.
Пористую керамику используют как огнеупорные материалы, фильтры и диэлектрики в радиоэлектронике.
Ситаллы или стеклокристалические материалы получают из стекла специального состава с помощью контролируемой кристаллизации. Структура ситаллов представляет собой смесь мелких (0,01–1мкм) беспорядочно ориентированных кристаллов (60–95%) и остаточного стекла (40–50%). Такая структура образуется в стеклянных изделиях после двойного нагревания: первое нагревание нужно для формирования центров кристаллизации, второе – для выращивания кристаллов на готовых центрах.
Ситаллы подразделяют на термоситаллы и фотоситаллы. Для образования при нагревании центров кристаллизации в термоситаллы вводят окислы или фториды ТіО2, Р2О5 и др. В фотоситаллах используют малые добавки золота, серебра, платины или меди. Центры кристаллизации формируются под действием ультрафиолетового облучения и нагревания. Необлученные участки после нагревания остаются аморфными.
Фотоситаллы применяют как фоточувствительные материалы. Термоситаллы имеют универсальное применение, в частности, как прочные стабильные диэлектрики для радиодеталей, подложек и т.п.
Контрольные вопросы и задачи
1. Сколько атомов приходится на одну элементарную ячейку в кристаллах с простой, объёмно-центрированной и гранецентрированной кубической структурой?
2. Показать, что для идеальной гексагональной плотноупакованной структуры с плотной упаковкой 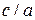 = 1,633.
= 1,633.
3. Записать координаты всех атомов элементарной ячейки алмаза.
4. Рассчитать угол между связями в твердом германии.
5. Доказать, что направление 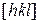 в кубической решетке нормально к плоскости
в кубической решетке нормально к плоскости 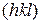 .
.
6. Сколько плоскостей типа 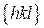 и
и 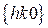 находится в кубических системах?
находится в кубических системах?
7. Какие плоскости в гранецентрированной и объёмно-центрированной кубических структурах имеют наибольшую плотность упаковки атомов.
8. В чем сходство и отличие жидких кристаллов и жидкостей?
9. В чем сходство и отличие кристаллических и аморфных твердых тел?
10. Найдите постоянную решетки алюминия, если она гранецентрированная. Использовать табличные данные о плотности и атомном весе алюминия.
11. Кадмий имеет плотноупакованную гексагональную структуру с постоянными 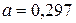 нм и
нм и 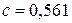 нм. Рассчитайте плотность кадмия. Использовать табличные данные о атомном весе кадмия.
нм. Рассчитайте плотность кадмия. Использовать табличные данные о атомном весе кадмия.
12. При температуре ниже 9100С железо имеет кубическую объемно-центрированную структуру (a–железо), выше 9100С– кубическую гранецентрированную (g– железо). В обеих структурах атомный радиус железа один и тот же. Как изменится плотность железа при переходе его из a– в g–модификацию?
13. Длина волны характеристического рентгеновского излучения, полученного с медного анода составляет 0,1537 нм. Эти лучи, попадая на кристалл алюминия, вызывают дифракцию от плоскостей под брэгговским углом 19,20. Алюминий имеет ГЦК структуру, плотность 2699 кг/м3 и атомный вес 26,98. По этим экспериментальным данным рассчитать число Авогадро.
Литература к главе 1
1. Фридрихов, С.Ф. Физические основы электронной техники [Текст]: учеб. / С.Ф. Фридрихов, С.М. Мовнин. – М.: Высш. школа, 1982. – 608 с.
2. Епифанов, Г.И. Физика твердого тела [Текст]: учеб. пособие / Г.И.Епифанов. – М.: Высш. школа, 1977. – 288 с.
3. Келли, А. Кристаллография и дефекты в кристалах [Текст]: пер. с англ. / А. Келли, Г. Гровс. – М.: Мир, 1974. – 496 с.
4. Уэрт Ч. Физика твердого тела [Текст]: пер. с англ. / Ч. Уэрт, Р. Томсон. – М.: Мир, 1966. – 568 с.
5. Кушта, Г.П. Введение в кристаллографию [Текст]: учеб. пособие / Г.П.Кушта. – Львов: Издательское объединение «Вища школа», 1976. – 238 с.
6. Кособукин, В.А. Физика твердого тела. Структура, группы симметрии и зонный спектр кристаллов [Текст]: учеб. пособие /СПб.: Изд-во Политехнического ун-та, 2007. – 80 с.
7. Гуревич, А.Г. Физика твердого тела [Текст]: учеб. пособие/ СПб.: Невский Диалект, 2004. – 320 с.
[1] Доказательство см. А.Келли, Г.Гровс. Кристаллография и дефекты в кристаллах. – М.: Мир, 1974. – 496 с.
[2] Артур Шёнфлис (Arthur Shönflies, 1853 – 1928) – немецкий математик. Работал в областях кинематики, геометрии, топологии, кристаллографии. В 1888-1891, параллельно с Е.С.Федоровым, вывел 230 пространственных групп. Символы кристаллографических классов «по Шёнфлису» стали основной системой обозначения точечных групп в физике, химии и спектроскопии.
[3] Кюри Пьер (Curie, 1859 – 1906) – французский физик, один из создателей учения о радиоактивности. Открыл (1880) и исследовал пьезоэлектричество. Исследования по симметрии кристаллов (принцип Кюри), магнетизму (закон Кюри, точка Кюри).
[4] Евграф Степанович Фёдоров (1853 –1919) – русский кристаллограф, минералог и математик. Крупнейшее достижение Е. С. Фёдорова – строгий вывод всех возможных пространственных групп (1891 год). Тем самым Федоров описал симметрии всего разнообразия кристаллических структур.
[5] Браве Огюст (Bravais Auguste,1811-1863) – французский физик, член Парижской АН. Работы в области оптики, магнетизма, кристаллографии, метеорологии. Положил начало геометрической теории структуры кристаллов. Установил основные виды пространственных решеток кристаллов (решетки Браве).
[6] Уильям Хэллоуз Миллер (англ. William Hallowes Miller, 1801–1880) – английский кристаллограф. Работы по гидростатике, гидродинамике, минералогии.
[7] Юджин Вигнер (венг. Wigner Jenő Pál; 1902 – 1995) – американский физик и математик венгерского происхождения, лауреат Нобелевской премии по физике в 1963 г. «за вклад в теорию атомного ядра и элементарных частиц, особенно с помощью открытия и приложения фундаментальных принципов симметрии». Работы по теории симметрий в квантовой механике, исследованию атомного ядра, ряд теорем.
Фредерик Зейтц (англ. Frederick Seitz, 1911 – 2008) – американский физик, один из пионеров физики твёрдого тела. В 1962–1969 годах являлся президентом Национальной академии наук США.
[8] Лео́н Николя́ Бриллюэ́н (фр. Léon Nicolas Brillouin, 1889 –1969) – французский и американский физик, основатель современной физики твёрдого тела.
[9] Джон фон Нейман (англ. John von Neumann, 1903 –1957) – венгро-американский математик, сделавший важный вклад в квантовую физику, квантовую логику, функциональный анализ, теорию множеств, информатику, экономику и другие отрасли науки.
[10] Ян Дидерик Ван-дер-Ваальс (1837 –1923) – голландский физик, лауреат Нобелевской премии по физике в 1910 г. за работу над уравнением состояния газов и жидкостей. Большая часть работ относится к области теоретической молекулярной физики. Он исследовал поведение молекул и занимался теориями, описывающими состояния материи.
[11] Лев Васильевич Шубников (1901 –1937) – российский физик-экспериментатор, специалист в области физики низких температур, соавтор открытия «Эффект Шубникова — де Хааза». Основные работы по исследованию сверхпроводимости, антиферромагнетизма, ядерного парамагнетизма твёрдого тела, взаимодействию нейтронов с атомными ядрами, фазовым переходам, технической криогенике.
[12] Вандер Йоханнес де Хааз (нидерл. Wander Johannes de Haas, 1878 –1960) – голландский физик и математик. Известен открытием нескольких важных электромагнитных явлений: эффект Эйнштейна-де Хааза, эффект Шубникова – де Хааза, эффект де Хааза – ван Альфена.
[13] Холл Эдвин Герберт (англ. Edwin Herbert Hall; 1855–1938) – американский физик. Работы посвящены термоэлектричеству, электро- и теплопроводности металлов, термомагнитным и электромагнитным эффектам в железе. Открыл в 1879 одно из важнейших гальваномагнитных явлений – эффект Холла.
[14] Андрей Константинович Гейм (нидерл. Andre Geim; 1958) – советский и нидерландский физик, лауреат Нобелевской премии по физике 2010 года (совместно с Константином Новосёловым), член Лондонского королевского общества, известный в первую очередь как один из первооткрывателей графена.
[15] Константин Сергеевич Новосёлов (род. 1974) – российский и британский физик. Лауреат Нобелевской премии по физике 2010 года (совместно с Андреем Геймом), член Лондонского королевского общества. Самый молодой из ныне живущих нобелевских лауреатов во всех областях.
Дата добавления: 2020-07-18; просмотров: 904;











