Теплоемкость твердых тел
Еще в 19 веке было установлено эмпирическое правило (закон Дюлонга и Пти), согласно которому:
«Молярная изобарная теплоемкость Ср при комнатных и более высоких температурах для различных простых веществ в кристаллическом состоянии одинакова и равна приблизительно 26 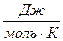 .»
.»
Многие элементы действительно имеют теплоемкость, равную  25…28
25…28 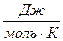 , однако известно немало отступлений: так Ср(В) = 11,1
, однако известно немало отступлений: так Ср(В) = 11,1 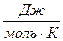 ; Ср(Si) = 20,1
; Ср(Si) = 20,1 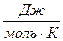 ; Ср(алмаз) = 6,11
; Ср(алмаз) = 6,11 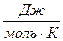 .
.
Для расчета молярной теплоемкости сложных кристаллических веществ Нейманном и Коппом предложено правило аддитивности,согласно которому:
«Молярная теплоемкость химических соединений равна сумме молярных теплоемкостей элементов, входящих в данное соединение.»
Принимая во внимание правило Дюлонга и Пти, можно написать:
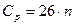 ,
, 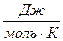 ,
,
где n – число атомов в молекуле.
У ряда неметаллов молярная теплоемкость значительно ниже 26 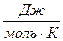 , что следует учитывать при расчете Ср сложных веществ. Величина вклада в молярную теплоемкость сложных веществ приведена ниже в таблице 1.1.
, что следует учитывать при расчете Ср сложных веществ. Величина вклада в молярную теплоемкость сложных веществ приведена ниже в таблице 1.1.
Таблица 1.1 – Эмпирические данные для вычисления теплоемкости
| элемент | С | Н | В | Si | O | F | P | S |
Cр, 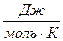
| 7,6 | 9,6 | 11,3 | 15,9 | 16,8 | 21,0 | 22,6 | 22,6 |
У твердых веществ также наблюдается зависимость теплоемкости от температуры:
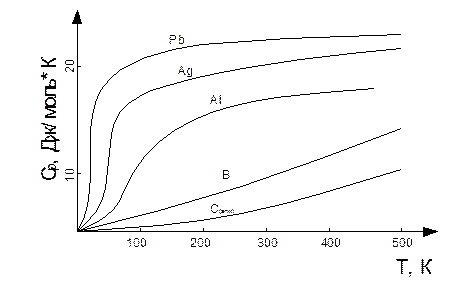
Рисунок 1.1 – Зависимость теплоемкости твердых тел от температуры
Зависимость теплоемкости твердых органических и неорганических веществ как и газов (формула 1.4) от температуры может быть представлена в виде эмпирических уравнений:
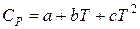 или
или 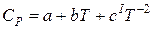
где а, в, с, сl – константы, применяемые в определенном интервале температур.
При очень низких температурах теплоемкость зависит от температуры по уравнению Дебая (закон кубов Дебая):
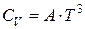
Для расчета средней теплоемкости в интервале температур Т1 – Т2 используется уравнение:
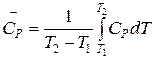
где СР берется в виде уравнения (1.4).
Для веществ с атомной кристаллической решеткой изобарная и изохорная молярные теплоемкости связаны уравнением:
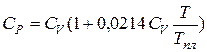
Но без большой погрешности при расчетах можно принять 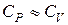 для твердых веществ.
для твердых веществ.
По свойству аддитивности можно рассчитывать теплоемкость сплавов:
1. для молярной теплоемкости
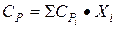
где 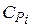 - молярная теплоемкость компонентов сплава; Хi – молярная доля компонента в сплаве.
- молярная теплоемкость компонентов сплава; Хi – молярная доля компонента в сплаве.
2. для удельной теплоемкости
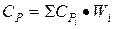
где 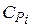 - удельная теплоемкость компонентов сплава; Wi – массовая доля компонента в сплаве.
- удельная теплоемкость компонентов сплава; Wi – массовая доля компонента в сплаве.
Дата добавления: 2016-06-22; просмотров: 4755;











