Структура натрийборосиликатных стёкол
В бинарной системе В2О3 – SiO2 структура аддитивно складывается из фрагментов (островков) структур стеклообразных В2О3 и SiO2. При добавлении первых порций оксида натрия структура исходного стекла не претерпевает существенных изменений. При соотношении Na2O/B2O3 < 1/3 свойства боросиликатных стёкол меняются слабо. Бор остается в тройной координации, идет разрыв полимерной сетки боратной составляющей с освобождением одной из вершин треугольника.
=В− + Na2O → =В−О- Na+
Бор, находящийся в тройной координации, является химически нестойким и легко вымывается кислотами вместе со связанным с ним оксидом натрия. В остатке сохраняется неповреждённый скелет кремнезёма с незначительной примесью оксида натрия. Эти свойства натрийборосиликатного стекла используют для получения молекулярных сит.
Рентгеноструктурный анализ показал две отдельные составляющие: кремнезёмистую и натриевоборатную. Невозможность перехода бора в четверную координацию при малом содержании щелочных металлов вызывает ликвацию.
При дальнейшем повышении концентрации оксида натрия (если Na2O/B2O3 > 1/3) свойства стекол меняются. Резко возрастает парциально-молярный объем В2О3, увеличивается его парциальный показатель преломления, уменьшается парциально-молярный объём. Бор переходит из тройной координации в четверную. Боратная составляющая постепенно исчезает и образуется единый кремне-боратнокислородный каркас. Стёкла не поддаются сквозной промывке кислотами, из них невозможно получить пористые стёкла.
Структуру стёкол исследовали методами инфракрасной спектроскопии, комбинационного рассеяния. При избытке щелочных металлов структурный анализ выявляет образование тетраэдров [ВО4]. Максимальная доля бора в тетраэдрической координации наблюдается при Na2O/В2О3 > 1, так как часть кислорода связывается с кремнием, разрывая мостик Si – O – Si. При дефиците щелочных металлов в спектрах поглощения появляется полоса, характерная для чистого борного ангидрида.
Не все оксиды МеО одинаково отдают бору свой кислород: катионы малого радиуса с интенсивным силовым полем прочнее удерживают анионы кислорода, чем катионы большого радиуса. Концентрация тетраэдров ВО4 при внесении Na2O возрастает не монотонно. Это связано с расходом оксида-модификатора на разрыв сетки из тетраэдров SiO4, т.е. кремнекислородной сетки стекла (рис. 2.15).
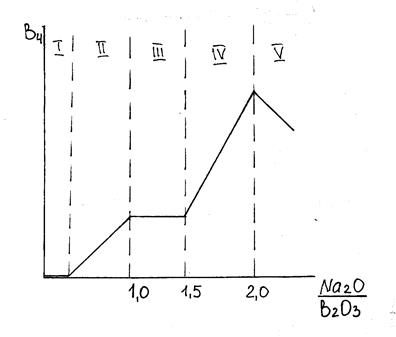
Рис. 2.15. Влияние содержания оксида натрия в стекле
Na2O - В2О3 - SiO2 на концентрацию бора
в четверной координации.
I. Координация бора не меняется, появляется немостиковый кислород:
=В−О−В= + Na2O → 2(=В−О- Na+).
Происходит разрыв бороксольных колец:
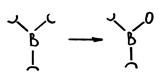
II. Появляются тетраэдры ВО4: Na2O↑ В4↑
Na+ Na+
2(−В=) + Na2O → ≡В−О−В≡
[ВО3]→[ВО4]
III. Na2O↑, B4 = const. Растет содержание Na2O, но бор координацию не меняет. Это связано, с расходом модификатора на разрыв кремнекислородной сетки.
(≡Si−O−Si≡) + Na2O → 2(≡Si−O- Na+)
IV. Na2O↑, В4↑
Na+
≡Si−O−Si≡ + Na2O + −В= → ≡Si−O−В≡
Образуется общий борокремнекислородный каркас.
V. Происходит сращивание структур из тетраэдров SiO4 и тетраэдров ВО4:
Na+ Na+ Na+
≡Si−O−Si≡ + ≡В−О−В≡ → 2(≡Si−O−В≡)
Не все модификаторы способны изменять координацию бора. Небольшие катионы, прочно удерживающие кислород в оксидах, не влияют на полимерную структуру из треугольников ВО3. Изменение координации бора сказывается на химической стойкости, твердости, поверхностном натяжении и других свойствах стёкол.
В двойной системе В2О3-Na2O сначала протекает реакция II, а потом идет разрыв сетки стекла по реакции I. Изменение очередности протекания этих реакций в тройной системе обусловлено влиянием диоксида кремния, ослабляющим боратную составляющую стекла.
Дата добавления: 2018-11-26; просмотров: 929;











