ХИМИЧЕСКИЙ ПОТЕНЦИАЛ
В химических реакциях, в отличие от термодинамических процессов, массы отдельных компонентов изменяются. В этом случае любое из свойств системы может быть представлено как, функция количества вещества m и любых двух переменных р, V, Т,U, S, F идругих. Дифференцируя выражение
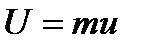 ,
,
где и - внутренняя энергия количественной единицы вещества, получим
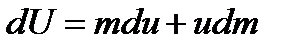 . (13.28)
. (13.28)
Известно, что 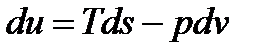 . Отсюда (13.28) примет вид
. Отсюда (13.28) примет вид
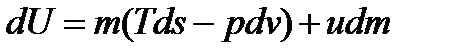 .
.
Так как
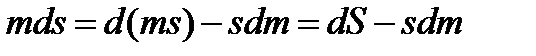 ;
;
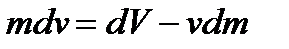 ,
,
то
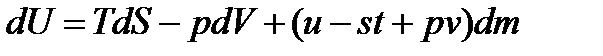 . (13.29)
. (13.29)
Величина 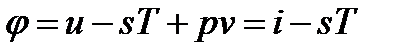 называется химическим потенциалом.
называется химическим потенциалом.
Уравнение (13.29) принимает вид
 .
.
По аналогии можно записать
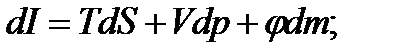
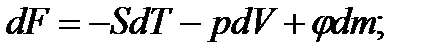
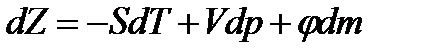 .
.
Вычислив соответствующие производные, получим
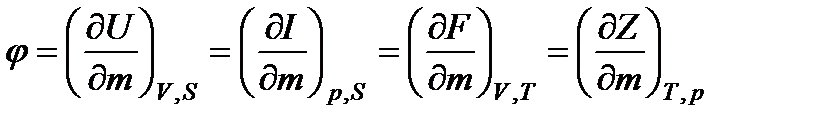 . (13.30)
. (13.30)
Таким образом, химический потенциал является частной производной одной из термодинамических функций по массе при постоянных значениях соответствующих независимых переменных.
Так как все рассмотренные выше термодинамические функции (U, I, S, F, Z) имеют размерность энергии, то, как это следует из формулы (13.30), химический потенциал характеризует изменение энергии при изменении массы данного вещества на единицу. Химический потенциал имеет важное значение в термодинамике фазовых превращений и в химической термодинамике.
Это связано с тем, что здесь рассматриваются процессы, протекающие с перераспределением массы системы.
Дата добавления: 2016-06-05; просмотров: 2061;











