Количество вещества.
Макроскопические тела состоят из огромного количества молекул. Поэтому измерять количество атомов или молекул в штуках неудобно. В СИ количество вещества характеризуется числом его структурных элементов. Оно выражается в молях. Моль равен количеству вещества рассматриваемой системы, которое содержит столько же структурных элементов, сколько структурных элементов (атомов) содержится в 0,012 кг изотопа углерода 12С.
Таким образом, моль любого вещества содержит, по определению, одинаковое число структурных элементов. Это число называют постоянной Авогадро. Она равна
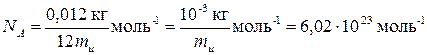 .
.
Понятие моля относится к числу структурных элементов вещества. Поэтому они всегда должны быть указаны, иначе определение количества вещества в молях теряет смысл. Например, неправильно говорить, что в сосуде содержится два моля воды. Правильно сказать, что в сосуде содержится два моля молекул воды. Это означает, что в сосуде имеется 2× 6,02×1023 молекул Н2О.
В молекулярной физике пользуются также понятием молярной массы, которая определяется как масса одного моля вещества:
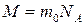 ,
,
где m0 – масса молекулы. Молярная масса выражается в килограммах на моль (кг/моль). Перепишем последнюю формулу в виде
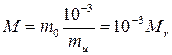 [кг/моль].
[кг/моль].
В частности, молярная масса вещества, состоящего из изотопов углерода 12С, равна 12×10-3 кг/моль. Относительные атомные массы приведены в таблице Менделеева. Относительные молекулярные массы могут быть с достаточной точностью найдены в виде суммы относительных масс атомов, составляющих молекулу.
Дата добавления: 2021-09-25; просмотров: 502;











