Физические свойства и строение
Пиридин представляет собой бесцветную жидкость с т.кип. 115,30С. Он обладает характерным неприятным запахом, смешивается во всех отношениях с водой, этанолом, диэтиловым эфиром; устойчив при хранении.
Пиридин является шестичленным гетероароматическим аналогом бензола. Его плоская молекула имеет сопряженную систему из шести π-электронов. Все атомы цикла находятся в состоянии sp2- гибридизации и вносят по одному π-электрону в ароматический секстет:




 • •
• •









 • •
• •






 N••
N••
 • •
• •


Неподеленная пара электронов атома азота находится вне π-сопряженной системы и занимает sp2-орбиталь, ориентированную в плоскость цикла и имеющую σ-симметрию.
То есть атомы углерода и атом азота находятся в sp2- гибридизации, и неподеленная пара электронов атома азота не участвует в образовании ароматической связи; поэтому она свободна и находится в плоскости кольца, но вне кольца. Отсюда основные свойства пиридина будут сильнее, чем у пиррола.
π-Электроный секстет придает молекуле пиридина ароматический характер. Введение атома азота в кольцо мало влияет на стабильность системы. Значение энергии резонанса пиридина практически равно энергии резонанса бензола.
 0,140 нм
0,140 нм

 1200 0,139 нм
1200 0,139 нм
 N 0,134 нм
N 0,134 нм
молекулярная диаграмма пиридина
Ароматическая делокализация π-электронов в молекуле пиридина иллюстрируется следующим набором резонансных структур:







 |  |  |  | ||||||||||
 |  |  | |||||||||||





 •• •• ••
•• •• ••
N N N N







 •• •• •• ••
•• •• •• ••
резонансные структуры пиридина
В большей части этих структур атом азота имеет отрицательный заряд, что соответствует его большей электроотрицательности. Степень разделения зарядов в молекуле пиридина характеризует сравнительно высокий дипольный момент. В соответствии с этим пиридин рассматривают как электронодефицитный гетероцикл.
+ 0,055




 0,00
0,00
μ = 2,26 D
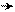 + 0,105
+ 0,105
N– 0,23
••
распределение π-электронной плотности и значение дипольного момента
в молекуле пиридина
Вследствие большей электроотрицательности атома азота электронная плотность смещена к гетероатому, а в α- и γ-положениях кольца возникают положительные заряды, то есть атом азота в пиридине обедняет кольцо электронной плотностью и выступает как ориентант 2-го рода в реакциях электрофильного замещения.
При сравнении реакционной способности в реакциях электрофильного замещения бензола, пятичленных гетероциклов и пиридина на первом месте будут располагаться пятичленные гетероциклы (пиррол, фуран и тиофен), затем бензол и на последнем месте будет находиться пиридин:
 |  | ||||||||
 |  |  | |||||||

 SE : > > > >
SE : > > > >

 •• •• ••
•• •• ••
 N O S N
N O S N
H ••
пиррол фуран тиофен бензол пиридин
Электроотрицательные значения энергий граничных орбиталей пиридина сравниваются с соответствующими значениями для бензола и пиррола:
 Электронное сродство (А1), эВ – 2,38
Электронное сродство (А1), эВ – 2,38

 –2
–2
– 1,15


 –1
–1
– 0,62
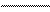 | |||||
 |  | ||||
Потенциал ионизации (I1),эВ 8,85






 – 9
– 9


 9,24
9,24
 –10 9,70
–10 9,70
бензол пиррол пиридин
Дата добавления: 2017-01-16; просмотров: 1982;











