Химические свойства нафталина
Молекулы конденсированных бензоидных углеводородов содержат (4n+2) π-электронов. Они частично удовлетворяют правилу Хюккеля, которое сформулировано для моноциклических аннуленов. Конденсированные бензоидные углеводороды обладают поэтому многими свойствами ароматических соединений и прежде всего склонностью к реакциям электрофильного ароматического замещения. В целом, эти углеводороды более активны в реакциях SEAr по сравнению с бензолом.
Реакции замещения
1) Замещение электрофильного характера- SEAr
Замещение SEAr идут легче, чем у бензола. Заместитель становится в α-положение, так как возникает энергетически более выгодный σ-комплекс. При α-замещении нарушается ароматичность только одного кольца, а при β-замещении – двух колец:































 Н Х Н Х Н Х
Н Х Н Х Н Х
 α δ+ +
α δ+ +
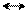
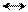
 +
+
δ+ +
 + Х+
+ Х+




















 δ+ Х + Х Х
δ+ Х + Х Х
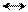
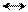

 δ+ + δ+ Н Н + Н
δ+ + δ+ Н Н + Н
β
Х








 Н
Н
+
Х+ = Г+, NO2+, SO3H+ и другие
Ниже показан ряд реакций электрофильного замещения в нафталине.

 О
О

 С
С








 О СН3
О СН3
 СН3-С
СН3-С
 Cl
Cl
AlCl3, C2H2Cl4 1-ацетилнафталин
 NO2
NO2





















 HNO3 NO2
HNO3 NO2
 H2SO4 +
H2SO4 +

нафталин 1-нитронафталин (95%) 2-нитронафталин (5%)
 Br
Br






 Br2, 400C
Br2, 400C
 CCl4
CCl4







 1-бромнафталин CH3
1-бромнафталин CH3
CH3Cl, AlCl3
1-метилнафталин
Как видно, эти реакции идут преимущественно в α-положения нафталина – положения 1,4,5,8.
Вступление электрофильного агента в β-положения-положения 2,3,6,7 – наблюдается реже. Как правило, это происходит в специфических условиях. В часности, сульфирование нафталина моногидратом при 600С протекает как кинетически контролируемый процесс ( в этих условиях реакция необратима) с преимущественным образованием 1 –нафталинсульфокислоты.
 SO3H
SO3H





















 H2SO4, 600C SO3H
H2SO4, 600C SO3H
 2 + + 2 H2O
2 + + 2 H2O
нафталин 1-нафталинсульфо- 2-нафталинсульфо
кислота (85%) кислота (15%)
 SO3H
SO3H





















 1600C SO3H
1600C SO3H
 2 + H2SO4 + + 2 H2O
2 + H2SO4 + + 2 H2O
нафталин 2-нафталинсульфо- 1-нафталинсульфо-
кислота (85%) кислота (15%)
Сульфирование нафталина купоросным маслом (94%-я H2SO4) при 1600С протекает как термодинамически контролируемый процесс. В этих условиях реакция сульфирования обратима. 2-Нафталинсульфокислота является термодинамически более устойчивой и накапливается в реакционной смеси. Такой же состав приобретает смесь после нагревания чистой 1-нафталинсульфокислоты при 1600С в купоросном масле.
Ацетилирование нафталина по Фриделю-Крафтсу – еще один пример зависимости изомерного состава продуктов от условий реакции. В противоположность ацетилированию в тетрахлорэтане или сероуглероде, когда преимущественно образуется 1-ацетилнафталин, при применении нитробензола в качестве растворителя ацетильная группа встает в β-положение. Полагают, что громоздкий комплекс ацилирующего агента с нитробензолом не может атаковать α-положение нафталина по пространственным причинам.

 O
O

















 О C
О C
 + СН3 – С · AlCl3 · C6H5NO2 CH3
+ СН3 – С · AlCl3 · C6H5NO2 CH3
Cl –HCl,
–AlCl3,–C6H5NO2
нафталин хлористый ацетил 2-ацетилнафталин

 Температура также влияет на соотношение α- и β-ацилов нафталина. Например, при 00С соотношение 1΄-ацетонафтона к 2΄-ацетонафтону составляет 3 : 1. а при 300С практически образуется только 2΄-ацетонафтон. O
Температура также влияет на соотношение α- и β-ацилов нафталина. Например, при 00С соотношение 1΄-ацетонафтона к 2΄-ацетонафтону составляет 3 : 1. а при 300С практически образуется только 2΄-ацетонафтон. O











 C O
C O














 AlCl3, C6H5Cl CH3 C
AlCl3, C6H5Cl CH3 C
 + CH3COCl + CH3
+ CH3COCl + CH3
нафталин ацетилхлорид 1΄-ацетонафтон 2΄-ацетонафтон
2) Замещение нуклеофильного характера- SNAr
Нуклеофильное замещение у нафталина происходит трудно, но легче, чем у бензола, например, в присутствии амида натрия нафталин образует 1-аминонафталин или α-нафтиламин.
 NH2
NH2
 |  |
 + NH2Na + NaH
+ NH2Na + NaH
нафталин амид натрия 1-аминонафталин гидрид натрия
Дата добавления: 2017-01-16; просмотров: 3875;











