С конденсированными бензольными кольцами
Соединения, в которых два или более бензольных цикла сконденсированы, (то есть имеют два общих атома углерода) в единой молекуле, образуют класс конденсированных бензоидных углеводородов. Они в значительных количествах присутствуют в каменноугольной смоле. Эти соединения, как и другие ароматические углеводороды, характеризуются значительной энергией сопряжения. Их также называют аренами.
Нафталин, антрацен и фенантрен являются простейшими представителями этого класса.
 |  |  |

Нафталин антрацен фенантрен
Энергия 225 кДж/моль 347 кДж/моль 380 кДж/моль
сопряжения: (61 ккал/моль) (83 ккал/моль) (91 ккал/моль)
К конденсированным бензоидным системам относятся и пирен:

Для каждого конденсированного бензоидного углеводорода может быть написано значительное число резонансных структур, например, у нафталина некоторые резонансные структуры имеют вид:





















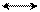 | 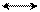 |
I II III
Как видно, резонансные структуры нафталина неравноценны. Наиболее стабильной является та резонансная структура, в которой наибольшее число колец соответствует формуле бензола Кекуле. Из трех способов расположения двойных связей (I, II, III) всех ближе к истине формула I. В ней оба кольца – бензольные и проявляются как бы остатки двух диеновых систем в отличие от формул II и III, где лишь одно кольцо бензольное.
Нафталин обладает меньшей ароматичностью по сравнению с бензолом. В частности, в молекуле нафталина наблюдаются значительные отклонения длин С-С-связей от ароматических значений (значения длин связей в показанных ниже формулах даны в нанометрах). Такие же отклонения имеются в молекулах антрацена и фенантрена.
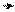

 0,1425 0,1456 0,1408
0,1425 0,1456 0,1408
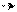












 0,1361
0,1361


 0,1421 0,1411
0,1421 0,1411

 0,1417
0,1417
0,1334
Хотя показанные выше углеводороды и не являются моноциклическими, как того требует правило Хюккеля, в каждом из них имеется плоская система сопряженных двойных связей, а общее число π-электронов удовлетворяет правилу ароматичности (4n+2). Электроны в молекулах этих углеводородов находятся только на связывающих дважды занятых МО. В качестве примера результаты расчетов по методу МОХ приведены для нафталина и антрацена:
ЕМО 



 α – 2β
α – 2β
 |  |


 α – β
α – β


α


 α + β
α + β







 α+2β
α+2β
 |  |


Конденсированные бензоидные углеводороды также легко вступают в реакции электрофильного замещения и проявляют тем самым свойства ароматических соединений.
Нафталин
Нафталин (нафтален) – основная составная часть каменноугольной смолы, которая является сырьем для получения нафталина и его производных. Открыт нафталин Гарденом в 1819 г., его состав установлен Воскресенским А.А. в 1838 г., а строение нафталина изучил Эрленмейер в 1866 году.
Эмпирическая формула нафталина – С10Н8, структурная формула представлена в виде двух бензольных конденсированных колец:








 8(α) 1(α)
8(α) 1(α)

 7(β) 2(β)
7(β) 2(β)
6 (β) 3(β) или
5(α) 4(α)
Для нафталина характерно существование изомеров: двух однозамещенных (α- и β –производных), десяти двухзамещенных для одинаковых заместителей и 14 изомеров для двух разных заместителей:


 СН3 СН3 СН3
СН3 СН3 СН3
















 СН3 СН3
СН3 СН3

 СН3
СН3
1-метилнафталин 2-метилнафталин 1,2-диметилнафталин 1,3-диметилнафталин
(α-метилнафталин) (β-метилнафталин) (орто-диметилнафталин) (мета-диметилнафталин)







 СН3 СН3 СН3 СН3
СН3 СН3 СН3 СН3










 Н3С
Н3С
 |  |


 Н3С
Н3С
СН3 СН3
1,4-диметилнафталин 1,5-диметилнафталин 1,7-диметилнафталин
(пара-диметилнафталин) 1,6-диметилнафталин
СН3 СН3



















 СН3 Н3С СН3 СН3
СН3 Н3С СН3 СН3
 |  |  |


СН3 Н3С
1,8-диметилнафталин 2,3-диметилнафталин 2,6-диметилнафталин
(пери-диметилнафталин) 2,7-диметилнафталин (амфи-диметилнафталин)
Приставки, придуманные для обозначения остальных положений, не привились.
Дата добавления: 2017-01-16; просмотров: 2154;











