Валентные изомеры бензола
В истории ароматических соединений существовало несколько формул изображения строения бензола. Например, формулы:











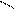



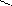
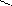
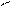
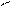




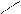
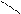

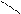








Кекуле Дьюара Тиле центрическая диагональная призматическая
Армстронга- Клауса Ладенбурга
Байера
Создатели этих формул стремились отразить наиболее типичные черты бензольной молекулы. Последующие исследования показали выдающуюся прозорливость создателей некоторых формул.
В 1963 году был синтезирован дьюаровский бензол. Ван Тамелен получил его при фотохимическом облучении бензола. В 1968 году Уорд и Уишнок облучением бензола в жидком состоянии дальним ультрафиолетовым светом (1650-2000 А0) получили валентный изомер бензола – дьюаровский бензол, а именно, бицикло[2.2.0]гексадиен-2,5, наряду с двумя другими валентными изомерами бензола – бензваленом и фульвеном:












 или
или
 бензол Дьюара
бензол Дьюара




 hυ
hυ
 | |||
 | |||

бензвален

 СН2
СН2



Фульвен
При фотохимическом облучении 1,2,4-тритрет-бутилбензола вследствие пространственных факторов нарушается одноплоскостное строение бензольного кольца и образуется смесь валентных изомеров:




 С(СН3)3 С(СН3)3 (СН3)3С С(СН3)3 С(СН3)3
С(СН3)3 С(СН3)3 (СН3)3С С(СН3)3 С(СН3)3



















 6 11 2 С(СН3)3 hυ С(СН3)3 (СН3)3С
6 11 2 С(СН3)3 hυ С(СН3)3 (СН3)3С






 + +
+ +




 5 3
5 3
 4С(СН3)3 C(CН3)3 C(CН3)3 C(CН3)3
4С(СН3)3 C(CН3)3 C(CН3)3 C(CН3)3
1,2,4-тритрет-бутил- замещенный бензол замещенный замещенный
бензол Дьюара призматический бензвален
бензол Ладенбурга
Все три валентных изомера при нагревании необратимо изомеризуются в производные бензола. Все три изомера бензола не являются ароматичными соединениями,
так как плоскостная система нарушена.
Валентный изомер фульвен является и структурным изомером бензола, но он также неароматичен. Для него характерны свойства полиена с локализованными двойными связями. В молекуле фульвена нет делокализации π-электронов:



 0,148 нм
0,148 нм




 0,146 нм 0,151 нм
0,146 нм 0,151 нм

 0,135 нм
0,135 нм
0,134 нм
Таким образом, бензол имеет четыре валентных изомера: бензол Дьюара, бензвален, призман Ладенбурга и фульвен. Фульвен к тому же является и структурным изомером бензола в связи с его плоским строением.
Итак, при образовании валентных изомеров происходит перестройка π- и σ-связей, сопровождающаяся изменением межъядерных расстояний и валентных углов, без перемещения атомов или атомных групп.
В отличие от валентных изомеров существуют валентные таутомеры, которые находятся в состоянии динамического равновесия, часто сильно смещенного в сторону одного из таутомеров, и различаются значениями межъядерных расстояний и валентных углов. Валентная таутомерия также сопровождается перестройкой π- и σ-связей без перемещения атомов. Например, взаимное превращение циклооктатетраена и бициклооктатриена:








 1000С
1000С

–200С
циклооктатетраен бициклотриен
Дата добавления: 2017-01-16; просмотров: 2958;











