Опыт №5. Получение динитрофенилгидразона.
В пробирку поместите одну лопаточку 2,4-динитрофенилгидразина и такое же количество CH3COONa (кристаллы), добавьте 1 мл 2 Н раствор HCl. Хорошо перемешайте и прибавьте 2-3 капли чистого ацетона. При сильном встряхивании образуется жёлтый кристаллический осадок гидразона ацетона. Напишите схему реакции образования 2,4-динитрофенилгидразона ацетона.
ГЛАВА 5. КАРБОНОВЫЕ КИСЛОТЫ.
Вопросы к занятию.
1. Электронное строение карбоксильной группы.
2. Кислотность и основность карбоновых кислот с точки зрения протолитической теории.
3. Влияние на кислотность карбоновых кислот структуры органического заместителя в молекуле кислоты.
4. Классификация, изомерия и номенклатура карбоновых кислот.
5. Химические свойства карбоновых кислот.
6. Механизм реакции этерификации.
7. Хлорангидриды, ангидриды, амины и нитрилы производные карбоновых кислот.
8. Ди- и трикарбоновые кислоты и особенности их поведения.
9. Медико-биологическое значение карбоновых кислот.
Строение, номенклатура и физико-химические свойства
Карбоновых кислот
Органические соединения, содержащие карбоксильную группу 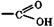 называются одноосновными карбоновыми кислотами, две – двухосновными и т. д. В зависимости от природы углеводородного остатка различают карбоновые кислоты: предельные, непредельные, ароматические, гетероароматические, гидрокси- и оксокислоты, аминокислоты и др. Одноосновные карбоновые кислоты общей формулы CnH2n+1COOH называются предельными кислотами.
называются одноосновными карбоновыми кислотами, две – двухосновными и т. д. В зависимости от природы углеводородного остатка различают карбоновые кислоты: предельные, непредельные, ароматические, гетероароматические, гидрокси- и оксокислоты, аминокислоты и др. Одноосновные карбоновые кислоты общей формулы CnH2n+1COOH называются предельными кислотами.
По систематической номенклатуре ИЮПАК названия карбоновых кислот образуют от названий родоначальных углеводородов с тем же числом атомов углерода с добавлением окончания -овая кислота. Названия циклических и ароматических карбоновых кислот образуют добавлением к названию родоначального углеводорода слов карбоновая кислота. Нумерацию цепи начинают с атома углерода карбоксильной группы. Для кислот использу-
ются и тривиальные названия, которые применяют также для замещенных кислот, обозначая положение заместителей греческими буквами. В этом случае углеродный атом, соседний с карбоксильной группой, обозначается как α-углерод, затем β-углерод, γ-углерод:
γ β α
R—СН2—СН3—СН2СООН и т. д.
Для названия аниона карбоновой кислоты RCOOӨ используется ее латинское тривиальное название с суффиксом -am, a для названия ее молекулярного остатка без гидроксильной группы, т. е. ацила 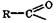 - то же название, но с суффиксом -ил. Примеры тривиальных и систематических названий некоторых карбоновых кислот, их анионов и ацильных групп приведены в табл. 12.
- то же название, но с суффиксом -ил. Примеры тривиальных и систематических названий некоторых карбоновых кислот, их анионов и ацильных групп приведены в табл. 12.
Название функциональных производных карбоновых кислот (эфиров, амидов и т. д.) формируется на основе названий их ацильного остатка.
|
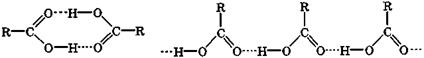
Низшие предельные монокарбоновые кислоты (C1—C9) представляют собой жидкости, а высшие предельные и ароматические кислоты - твердые вещества. Для карбоновых кислот характерна значительная межмолекулярная ассоциация вследствие образования циклических димеров или линейных ассоциатов за счет водородных связей:
ассоциативный циклический димер линейные ассоциаты
Таблица 12.
Дата добавления: 2019-09-30; просмотров: 919;











