Получение заготовок из порошковых, композиционных и неметаллических материалов
Металлокерамика
Порошковой металлургией называют область техники, охватывающую совокупность методов изготовления порошков металлов и изделий из них или их смесей с неметаллическими порошками без расплавления основного компонента.
Порошковая металлургия позволяет получать не только изделия различных форм (рисунок 5.31) и назначений, но и создавать принципиально новые материалы, которые другим путем получить или очень трудно или невозможно. У таких материалов можно получить уникальные свойства (жаропрочность, износостойкость, стабильные магнитные свойства, низкий или высокий коэффициент трения и др.). При этом способе в большинстве случаев коэффициент использования материала составляет около 100%.
| Рисунок 5.31 Типы деталей, получаемых методами порошковой металлургии |
Типовая технология производства деталей методом порошковой металлургии включает четыре основные операции:
- получение порошка исходного материала;
- формование заготовок;
- спекание;
- окончательную обработку.
Получение металлических порошков. Методы получения металлических порошков делят на механические и физико-химические, дающие возможность получать очень чистые шихтованные материалы.
При использовании механических методов исходный материал измельчается в порошок без изменения химического состава. К этим методам относятся: получение порошка размолом в шаровых, вихревых и вибрационных мельницах, грануляцией (распыление расплавленного металла газом или водой).
При физико-химических методах изменяется химический состав исходного сырья или его агрегатное состояние (восстановление окислов металлов газами или твердым восстановителем, электролиз водных растворов солей или распыленных сред, карбинольный метод и некоторые другие методы).
Методы получения порошков приведены в таблице 5.1
Таблица 5.1 Методы получения металлических порошков
| Методы | Характеристика | Материалы | Форма и размеры частиц, мкм | Примечание | |
| 1. Механические методы | |||||
| Размол в шаровых мельницах | Диаметр барабана 250…1500 мм, скорость вращения 30…120 об/мин | Черные и цветные металлы | Неправильный многогранник, 100…1000 | Порошки загрязняются продуктами истирания шаров и футеровки мельниц- | |
| Размол в вихревых мельницах | Скорость вращения пропеллеров 3000 об/мин | Железо, медь, алюминий, серебро, губчатый титан и их сплавы | Тарельчатая пластинка с зазубренными краями 50…200 | Можно размалывать отходы металлообрабатывающих цехов (стружку, обрезку) | |
| Виброизмельчение | 1400…1500 колебаний в минуту | Хрупкие карбиды, окислы металлов, керамика и др. | Неправильный многогранник, 20…60 | – | |
| Грануляция | Заливка в воду тонкой струей | Чугун, медь и др. | Сфероид, 100…3000 | Применяется для спекания пористых деталей | |
| 2. Физико-химические методы | |||||
| Восстановление из окислов | Восстановители твердые (углерод, магний) и газообразные (водород, окись углерода) | Железо, вольфрам, титан, молибден, никель, кобальт и др. | Неправильный многогранник, 50…200 | Наиболее дешевый метод. Получающаяся металлическая губка размалывается | |
| Электролиз | Осаждение порошка при электролизе солей металлов | Чистые и редкие металлы | Дендрит, 1…100 | Можно получать чистые порошки из загрязненного сырья | |
| Карбонильный | При 200…300° С распадается на порошок и окись углерода | Железо (магнитное), никель, кобальт | Сфероид, 1…820 | ||
| Восстановление гидратом кальция | Хром | Дендрит, 8…20 | Известь вымывается водой | ||
Для грубого размельчения используют щековые, валковые и конусные дробилки и бегуны; при этом получают частицы размером 1…10 мм, которые являются исходным материалом для тонкого измельчения, обеспечивающего производство требуемых металлических порошков. Исходным материалом для тонкого измельчения может быть и стружка.
Для размола пластичных материалов используют процесс измельчения, в котором разрушающие удары наносят сами частицы измельчаемого материала. Для этого используют вихревые мельницы.
Распыление и грануляция жидких металлов является наиболее простым и дешевым способом изготовления порошков металлов с температурой плавления до 1600о С: алюминия, железа, сталей, меди, цинка, свинца, никеля и других металлов и сплавов.
Сущность измельчения расплава состоит в дроблении струи расплава либо высоко энергонасыщенным газом или жидкостью, либо механическим распылением, либо сливанием струи расплава в жидкую среду (например, воду). В зависимости от свойств расплава и требований к качеству порошка распыление осуществляют воздухом, азотом, аргоном, гелием, а для защиты от окисления – инертным газом.
Наиболее часто применяемый физико-химический метод – восстановление металлов из окислов и солей. Простейшая реакция восстановления может быть представлена так:
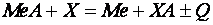
где 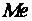 – любой металл;
– любой металл; 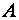 – неметаллическая составляющая (кислород, хлор, фтор, солевой остаток и др.) восстанавливаемого химического соединения металла;
– неметаллическая составляющая (кислород, хлор, фтор, солевой остаток и др.) восстанавливаемого химического соединения металла; 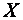 – восстановитель;
– восстановитель; 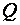 – тепловой эффект реакции.
– тепловой эффект реакции.
В качестве восстановителей используют – водород, окись углерода, диссоциированный аммиак, конвертированный природный газ, кокс, древесный уголь, металлы (кальций, магний, алюминий, натрий, кадмий и др.).
Железные порошки получают восстановлением окисленной руды или прокатной окалины. Железо в указанных материалах находится в виде окислов: Fe2O3, Fe3O4, FeO.
Медные, никелевые и кобальтовые порошки легко получают восстановлением окислов этих металлов, так как они обладают низким сродством к кислороду. Сырьем для производства порошков этих металлов служат либо окись меди Cu2O, CuO, закись никеля NiO, окись-закись кобальта Co2O3, Co3O4, либо окалина от проката проволоки, листов и т.д.
Восстановление проводят в муфельных или в трубчатых печах водородом, диссоциированным аммиаком или природным газом. Температура восстановления сравнительно низка:
o меди – 400...500 0С;
o никеля – 700...750 0С;
o кобальта - 520..570о С.
Длительность процесса восстановления 1...3 ч при толщине слоя окисла 20..25 мм. После восстановления получают губку, которая легко растирается в порошок.
Электролиз наиболее экономичен при производстве химически чистых порошков меди. Физическая сущность электролиза состоит в том, что при прохождении электрического тока водный раствор или расплав соли металла, выполняя роль электролита, разлагается, металл осаждается на катоде, где его ионы разряжаются
Ме+ne=Me
Сам процесс электрохимического превращения происходит на границе электрод (анод или катод) - раствор. Источником ионов выделяемого металла служат, как правило, анод, состоящий из этого металла, и электролит, содержащий его растворимое соединение.
Дата добавления: 2019-02-08; просмотров: 1117;











