Расчет дозировочных расходов
Для составления нитрационной кислотной смеси имеются данные.
1. Абсолютный состав и масса отработанной кислотной смеси после стока в аппарате НУОК:
| HNO3 | 3,797 т, |
| H2SO4 | 10,962 т, |
| H2O | 3,066 т |
| ‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾ | |
| всего 17,825 т. |
2. Массовый состав и масса кислот первой фракции:
| HNO3 | 1,14 т, |
| H2SO4 | 3,3 т, |
| H2O | 1,06 т |
| ‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾ | |
| всего 5,5 т. |
3. Общее количество кислотной смеси, поступающее на укрепление,
q3= q2+ q′1=17,825+5,5=23,325 т,
ее абсолютный состав:
| HNO3 | 3,797+1,140= | 4,037 т, |
| H2SO4 | 10,962+3,3= | 14,262 т, |
| H2O | 3,066+1,06= | 4,126 т |
| ‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾ | ||
| всего 23,325 т |
и массовая доля компонентов этих кислот:
| HNO3 | 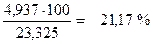 , ,
|
| H2SO4 | 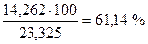 , ,
|
| H2O | 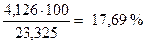
|
| ‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾‾ | |
| всего 100 %. |
4. Состав приготавливаемой рабочей кислотной смеси HNO3 – 24 %; H2SO4 - 60 %; H2O – 16 %.
5. Массовая доля азотной кислоты – 98 %.
6. Массовая доля серной кислоты – 92,5 %.
7. Масса нитрационной рабочей кислотной смеси В1=26 т.
Определим количества азотной кислоты N, серной кислоты S и отработанной кислотной смеси А2, необходимые для составления В рабочей кислотной смеси.
Для расчета запишем уравнения материального баланса:
| – по азотной кислоте | A2y2+Nn=By, |
| – по серной кислоте | A2x2+Ss=B1x, |
– для всей кислотной смеси A2+N+ S=B.
Подставив цифровые значения, получим
A2∙21,17+N∙98=26,24,
A2∙61,14+S∙92,5=26,60,
A2+N+ S=26.
Решив эту систему уравнений, определяем необходимые количества:
– отработанной кислотной смеси А2=22,5,
– азотной кислоты N=1,51 т;
– серной кислоты S=1,99 т.
Отработанная кислотная смесь имеет абсолютный состав:
| HNO3 | 22,5∙0,2117= | 4,76 т, |
| H2SO4 | 22,5∙0,6114= | 13,75 т; |
В переводе на моногидрат дозировочный расход кислот составит:
| HNO3 | 1,51∙0,98= | 1,48 т; |
| H2SO4 | 1,99∙0,925= | 1,84 т. |
Избыток отработанной кислотной смеси, поступающей на регенерацию, равен
А′2=23,325–22,5=0,825 т
абсолютного состава:
| HNO3 | 0,825∙0,2117= | 0,174 т, |
| H2SO4 | 0,825∙0,6114= | 0,504 т. |
Дата добавления: 2016-06-15; просмотров: 1579;











