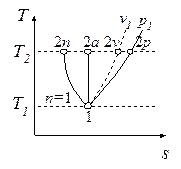Методические указания
При расчетах изменения калорических параметров (Du, Dh, Ds), теплоты и работы в процессах идеального газа в одних случаях допускается подставлять температуру как в градусах Цельсия, так и в градусах Кельвина, например 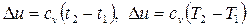 , в других - только в градусах Кельвина, например
, в других - только в градусах Кельвина, например
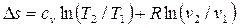 .
.
В одних величинах допускается при записи размерности использовать как градусы Цельсия (0С), так и градусы Кельвина (К), например, удельной теплоемкости,
с, Дж/(кг.0С), или с, Дж/(кг.К),
в других - только градусы Кельвина, например, удельной газовой постоянной и энтропии,
R, Дж/(кг.К), s, Дж/(кг.К).
Почему это так?
Дифференцирование связи температур
T = t + 273,15
дает dT = dt, т.е. разность температур в абсолютной шкале и в стоградусной шкале одна и та же. Это значит, что цена одного градуса в обеих шкалах одинакова. Следовательно, когда речь идет о разности температур, правомерно использовать любые градусы:
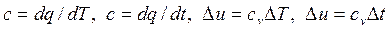 .
.
В тех случаях, когда речь идет о температуре или об отношении температур,
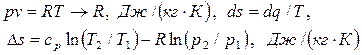
температура подставляется только в градусах Кельвина.
Задачи
1. При сжатии в компрессоре параметры воздуха изменились от p1 =1 бар, t1 = 20 0С, до p2 = 6 бар , t2 = 440 0С. Рассчитайте изменение энтальпии (Dh), внутренней энергии (Du), энтропии (Ds):
а) используя таблицы термодинамических свойств газов [7]; таблица для воздуха дана в Приложении.
б) при постоянной теплоемкости, принятой согласно молекулярно-кинетической теории газов.
2. Рассчитайте изменение энтальпии воздуха при нагреве его от 0 до
300 0С:
а) используя формулу зависимости теплоемкости от температуры для воздуха
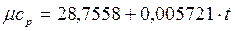 , кДж/(кмоль.0С);
, кДж/(кмоль.0С);
б) используя табличные значения средних теплоемкостей cpm (см. Приложение).
3. Рассчитайте эксергию потока гелия с параметрами p= 6 бар, t = 400 0С. Параметры окружающей среды: toc = 20 0С, poc = 1 бар. Мольная масса гелия m = 4 кг/кмоль.
Решение
Эксергия потока гелия
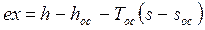 .
.
Поскольку гелий - одноатомный газ, его теплоемкость постоянна и равна:
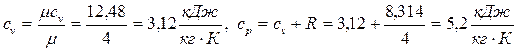 .
.
Тогда
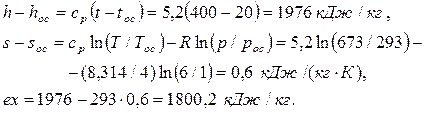
Ответ: ex= 1800,2 кДж/кг.
4. Параметры воздуха изменились от p1 = 1 бар, t1 = 0 0С до t2 = 200 0С:
а) в изобарном процессе;
б) в изохорном;
в) в адиабатном;
г) в политропном с показателем n = 1,2.
Определите для каждого из процессов показатель политропы (n), теплоемкость (c), изменение энтропии (Ds), теплоту (q). Представьте процессы в
T-s- диаграмме.
Теплоемкость принять постоянной согласно молекулярно-кинетической теории газов.
5. При адиабатном сжатии параметры воздуха изменились от p1 = 1 бар, t1 = 10 0С до p2 = 30 бар.
Определите конечную температуру воздуха для случаев:
а) с учетом зависимости теплоемкости от температуры, используя табличные значения p0;
б) без учета зависимости теплоемкости от температуры, приняв ее постоянной, согласно молекулярно-кинетической теории газов.
Решение
1. Из табл. 2 Приложения для воздуха при t1 = 10 0С берется значение p01 =1,1323.
С помощью соотношения (4.55) рассчитывается
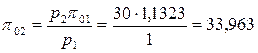 .
.
По значению p02 из таблицы находится t2 = 458,5 0С.
2. Температура воздуха рассчитывается по соотношению (4.48) при
k = 1,4:
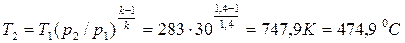 .
.
Ответ: а) t2 = 458,5 0С; б) t2 = 474,9 0С.
Ответы
1. а) Dh= 434 кДж/кг, Du= 313,6 кДж/кг, Ds = 0,4 кДж/(кг×К) ;
б) Dh= 420 кДж/кг, Du= 301,1 кДж/кг, Ds= 0,376 кДж/(кг×К).
2.а) Dh= 306,4 кДж/кг, б) Dh= 305,7 кДж/кг.
4.
| Процессы | n | c, кДж/(кг..К) | D s, кДж/(кг.К) | q, кДж/кг | |||
| Изобарный | 0,55 | ||||||
| Изохорный | µ | 0,72 | 0,396 | 79,2 | |||
| Адиабатный | 1,4 | ||||||
Политропный | 1,2 | -0,72 | -0,396 | -79,2 |
T-s- диаграмма
Дата добавления: 2021-07-22; просмотров: 523;