Образование полных и неполных эфиров с неорганическими и органическими кислотами.
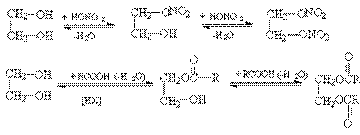
Если в качестве этерифицирующих агентов используются ангидриды и хлорангидриды карбоновых кислот, то реакции этерификации диолов протекают необратимо:
Окисление диолов
Процесс окисления диолов протекает обычно по сложной схеме, включающей последовательные и параллельные реакции.
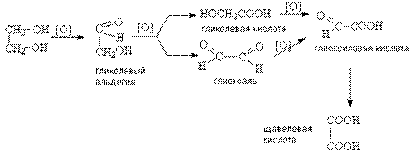
При этом, как и в случае одноатомных спиртов, по продуктам окисления можно судить о структуре диола. Так, если при окислении диола состава C4H8(OH)2 в продуктах окисления обнаруживается только уксусная кислота, то диол может иметь только формулу 2,3 – бутандиола.
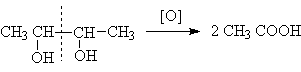
В этом плане характерной реакцией окисления, являющейся тестом на установление структуры
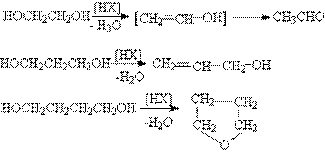
Дегидратация
Реакции дегидратации диолов могут иметь межмолекулярный или внутримолекулярный характер. Эти реакции относятся к реакциям нуклеофильного замещения. Поэтому для электрофильного отщепления “плохой” уходящей группы – OH требуется кислотный катализ.
ПРОСТЫЕ ЭФИРЫ
Простые эфиры можно рассматривать как производные спиртов, в которых атом водорода гидроксильной группы замещен на углеводородный радикал.
По характеру атомов углерода, связанных с кислородным атомом, простые эфиры можно подразделить на следующие типы:
1. Эфиры, содержащие связи С(sp3)O.
К ним относятся эфиры структуры ROR/и циклические эфиры.
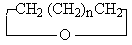
2. Эфиры содержащие связь С(sp2)O
К ним относятся
1. алкилалкениловые (виниловые) эфиры
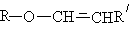
1. диалкениловые эфиры
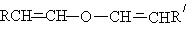
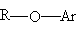
1. алкилариловые эфиры
1. диариловые эфиры
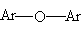
3. Эфиры, содержащие связь С(sp)O
RC C-OR/
Диалкиловые эфиры
Диалкиловые эфиры являются наиболее важными представителями класса простых эфиров. Их эмпирическая формула СnH2n + 2O или СnH2n + 1OCmH2m + 1.
Дата добавления: 2017-04-05; просмотров: 2224;











