Генетика деления клеток
Регуляция жизненного цикла может осуществляться внутриклеточными факторами и внеклеточно. Общий контроль активности деления клеток обеспечивают факторы различной природы, к которым относятся протоонкогены, антионкогены, факторы роста, кейлоны.
Протоонкогены - группа генов-активаторов, контролирующих нормальное клеточное деление и дифференцировку. Продукты этих генов - особые белки воздействуют на разные механизмы регуляции деления клетки: на уровне активирующего сигнала, его рецептора в мембране, второго посредника или транскрипции. К настоящему времени известно более 50 протоонкогенов.
Активация функции протоонкогенов и развитие опухолей.Изменения структуры и усиление активности экспрессии протоонкогенов вызывает развитие опухолей, что определило их название. Повышение активности протоонкогенов может быть связано с изменениями строения ДНК (в результате мутаций), увеличением количества генов (генной амплификации) или их размещением вблизи активного промотора. Измененные мутацией, но активные протоонкогены, называются онкогенами.
Антионкогены. Злокачественная трансформация клетки может возникнуть не только вследствие повышения активности протоонкогенов, но и в результате снижения активности другой группы генов, называемых антионкогенами. Антионкогены – гены, продукты которых – белки-супрессоры опухолевого роста, угнетают деление клеток. Из них наиболее подробно изучены гены RB (ретинобластомы), DCC, APC, WT1, NF1 и р53.
Ген р53 - один из наиболее мощных и универсальных антионкогенов - естественный онкосупрессор - обеспечивает поддержание стабильности генетического аппарата («охранитель» клеточного генома) и контролирует клеточный цикл. В нормальных условиях его экспрессия умеренная, при повреждении ДНК она резко усиливается. Активация гена р53 приводит к остановке клеточного цикла для репарации ДНК, в которой активное участие принимает продукт этого гена - белок р53 - благодаря способности связываться с поврежденным участком ДНК и регулировать восстановление его структуры. При тяжелых повреждениях, не устранимых путем репарации ДНК, р53 запускает программу апоптоза. Оба вида реакций защищают организм от репликации и амплификации (умножения) генетически поврежденного материала. Белок р53 индуцирует синтез продуктов генов р21, р15 и р16, которые блокируют особые ферменты (циклинзависимые киназы), обеспечивающие переход G1→S и прохождение других периодов клеточного цикла. Открытие гена p53 удостоено Нобелевской премии по физиологии и медицине за 2002 г.
Инактивация функции антионкогенов и развитие опухолей. Потеря функции гена р53 (в результате мутации) приводит к утрате контроля над клеточным циклом: клетки-мутанты продолжают активно пролиферировать, несмотря на повреждения ДНК. Выявлена четкая связь между утратой функции гена р53 и развитием более 50 видов злокачественных опухолей у человека. Так, изменения гена р53 обнаружены в 55-70% случаев рака легкого, в 25-30% - рака молочной железы. Опухоли с потерей функции гена р53 характеризуются наиболее злокачественным течением. В некоторых видах опухолей (в 60% меланом и лейкозов, в 80% глиом) обнаруживаются изменения гена р16; описаны опухоли, связанные с дефектами гена р15. Клетки рака шейки матки часто содержат инактивированные гены RB и р53. Мутация гена RB обнаруживается при ретинобластоме, опухолях костей, мочевого пузыря, легкого и молочной железы. Делеция гена DCC характерна для опухолей толстой и прямой кишки, АРС - для аденоматозного полипоза толстой кишки.
Факторы роста являются важными стимуляторами клеточного деления. Они представляют собой белки, усиливающие митотическую активность в определенных тканях (тканях-мишенях). Их действие опосредуется специфическими рецепторами на плазмолемме клеток. К ним относятся фактор роста нервов (ФРН), эпидермальный фактор роста (ЭФР), тромбоцитарный фактор роста (ТРФР), инсулиноподобные факторы роста (ИФР), фактор роста фибробластов (ФРФ), колониестимулирующие факторы (КСФ) - стимуляторы отдельных этапов гематопоэза, интерлейкины (ИЛ) -1, -2 и -3. Список факторов роста постоянно расширяется. Высказывается предположение, что большинство типов клеток реагирует не на один специфический фактор роста, а на их комбинации. Некоторые факторы роста циркулируют в крови, но большинство действует в тканях локально (паракринно).
Кейлоны - факторы, подавляющие клеточное деление. Кейлоны представляют собой класс гормоноподобных регуляторов, они являются полипептидами или гликопротеинами и обладают тканевой и клеточной специфичностью. Кейлоны образуются всеми зрелыми дифференцированными клетками и локально воздействуют на незрелые клетки этой же ткани, способные к делению. Они обеспечивают поддержание численности клеточной популяции. Уменьшение численности популяции клеток (например, потеря клеток эпидермиса при ранении или лейкоцитов при кровотечении) вызывает снижение ингибирующего воздействия кейлонов и подъем митотической активности в соответствующей ткани. Кейлоны участвуют в регуляции роста тканей, заживления ран, иммунных реакций и других процессах.
В организме клетки большинства тканей постоянно разрушаются, погибают и замещаются. Эти процессы происходят не только вследствие патологии, но в ходе нормальной жизнедеятельности (физиологическая регенерация, эмбриональное развитие). Различают два внешне похожих, но принципиально различных типов гибели клеток: апоптоз и некроз.
Апопто́з - генетически обусловленный процесс физиологической гибели клеток. При апоптозе ядро и цитоплазма уменьшаются в объеме, распадаются на глыбки и растворяются, что связано с активацией гидролитических ферментов лизосом. Морфологически апоптоз проявляется гибелью единичных, беспорядочно расположенных клеток, что сопровождается формированием округлых, окруженных мембраной телец («апоптотические тельца»), которые тут же фагоцитируются окружающими клетками. Апоптоз наряду с пролиферацией и миграцией клеток обеспечивает дифференцировку и специализацию тканей, способствует приобретению характерных для определенного биологического вида признаков организации. Например, у эмбриона человека в результате апоптоза исчезают закладки шейных ребер и зачатки хвоста, образуются полости тела и просветы сосудов. Он является механизмом постоянного контроля размеров органов. При снижении апоптоза происходит накопление клеток, например, опухолевый рост. При увеличении апоптоза наблюдается прогрессивное уменьшение количества клеток в ткани, развивается ее атрофия. Генетический контроль апоптоза обеспечивает ген p53. Белок - продукт этого гена способен при определенных условиях блокировать клеточное деление и запускать процесс самоликвидации дефектной клетки.
Механизм апоптоза выяснен совсем недавно, кроме того, явления апоптоза и некроза настолько похожи, что еще нередко для описания некоторых физиологических процессов разрушения клеток вместо термина «апоптоз» используют термин «некроз».
Некро́з - омертвение ткани под влиянием нарушения кровообращения, химического или термического воздействия (ожог, отморожение), травмы и др. Область некроза окружается особой зоной клеток, которые затем отторгаются или подвергаются гнойному расплавлению; на месте дефекта ткани образуется рубец. Некроз клеток возникает в нефизиологических условиях, в связи с действием неблагоприятных факторов, то есть это процесс патологический. В результате некроза происходит выпадение функции в связи с гибелью структурных элементов ткани или органа и интоксикацией, обусловленной наличием очага воспаления.
ГЕНЕТИКА СТАРЕНИЯ
По данным В.Н. Ярыгина [1], старение представляет собой всеобъемлющий процесс, охватывающий все уровни структурной организации особи - от макромолекулярного до организменного. Главным биологическим результатом старения является прогрессивное повышение вероятности смерти. Временной интервал между рождением и смертью (равный возрасту смерти) или длительность существования особи называется продолжительностью жизни. Продолжительность жизни обусловлена генетически и зависит от многих факторов. Так в различных странах мира продолжительность значительно отличается. Традиционно лидирует по этому показателю Япония (82,15 лет), за ней следуют западные страны (Франция, Канада, Греция, Германия и др.), Россия в этом списке занимает 17 место (66,0 лет).
Факторы, определяющие продолжительности жизни.
Определяющим фактором средней продолжительности жизни является уровень жизни - уровень материального положения, возможность получения квалифицированной медицинской помощи, хорошие жилищные и санитарно-гигиенические условия, оптимальные условия труда. Т.о. продолжительность жизни - это показатель экономической развитости государства и уровня жизни его граждан. В экономических развитых странах этот показатель значительно превосходит таковой малоразвитых и неразвитых стран. В малоразвитых странах этот показатель близок к такому уровню, какой был в развитых странах 2000-3000 лет назад.
Для отдельного человека, по мнению геронтологов, продолжительность жизни зависит от:
· наследственности (на 50%).
· условий жизни (30%),
· состояние окружающей среды (17-20%) - загрязненные воды, воздух, продукты питания отнюдь не способствуют росту продолжительности жизни Благоприятное влияние оказывают жизнь в деревне, отдаленность от дорог и др.
Иногда называют еще и
· образ жизни – характер питания, физической активности, режима сна и отдыха, отсутствие вредных привычек и т.д. Хотя геронтологи не совсем согласны с этим утверждением: согласно наблюдениям, среди долгожителей аскетов мало. Так среди кубинцев, средняя продолжительность жизни которых составляет 78 лет, широко распространены такие вредные привычки, как лень, чрезмерное употребление алкоголя, кофе и сигар. Однако не вызывает сомнения, что благоприятное влияние оказывает полноценный отдых и сон (особенно в пожилом возрасте), двигательная активность улучшает обмен веществ и обеспечивает активное кровоснабжение органов и тканей. Во многом от выбранного образа жизни зависит, как долго человек будет оставаться здоровым и энергичным.
· пол - известно, что женщины живут больше мужчин, практически во всех странах. Самая большая разница в продолжительности жизни мужчин и женщин наблюдается в странах бывшего СССР: Россия (14 лет), Украина (11.8 лет), Беларусь (11.8 лет). Казахстан (10.9 лет), Азербайджан (8.8 лет) и др. Отмечена закономерность: с уменьшением средней продолжительности жизни в стране, уменьшается разрыв продолжительности жизни между мужчинами и женщинами. Отчасти это связано с социальными и физиологическими факторами:
- социальный фактор: мужчина больше пристрастны к вредным привычкам (алкоголь, курение и наркотики), которые не только сокращают продолжительность жизни, но и в большинстве случаев являются причиной преждевременной смерти. Так же считается, что укорочению жизни мужчин способствует более тяжелый физический труд и плохие условия труда. Жертвами убийств и несчастных случаев, согласно статистике, чаще становятся мужчины. Также среди мужчин больше случаев суицида. Большинство мужчин менее внимательны к своему здоровью, чем женщины.
- физиологический фактор: наличие гормона эстрогена (у мужчин его намного меньше), регулирующего уровень холестерина в организме, что делает женщин менее подверженными сердечным заболеваниям. У женщин уровень эстрогена снижается после климакса или в связи с гормональными нарушениями, что влечет развитие патологии сердечно-сосудистой системы. Однако считается, что в доисторические времена мужчины жили дольше женщин (35 к 30 годам жизни), что было связано с репродуктивной функцией женщин - тяжелыми родами и многочисленными осложнениями.
Продолжительность жизни в пострепродуктивном периоде, как обобщающий показатель, широко используется в исследованиях генетики старения.
Ряд наблюдений легли в основу достаточно распространенной точки зрения о наследуемости продолжительности жизни и, следовательно, о генетическом контролеили даженаличии особойгенетической программы старения.
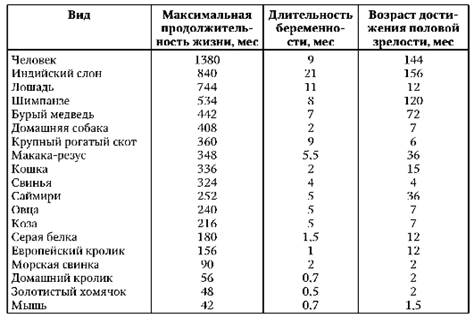
Во-первых, максимальная продолжительность жизни ведет себя как видовой признак. При этом она положительно связана с такими важными эволюционно закрепленными показателями биологии вида, как длительность эмбрионального периода и возраст достижения половой зрелости(табл. 1).
Таблица 1.
Максимальная продолжительность жизни, длительность эмбрионального периода и возраст достижения половой зрелости у различных видов млекопитающих животных.
Во-вторых, величины продолжительности жизни у однояйцевых близнецов более близки (конкордантны), чем у разнояйцовых. Попарные различия по этому показателю составляют в среднем 14,5 года для первых и 18,7 года для вторых. Сходная картина наблюдается при сопоставлении колебаний длительности жизни среди лабораторных животных одной линии и различных линий. Так, у мышей получены линии с продолжительностью жизни от 120 до 700 сут.
В-третьих, описаны наследственные болезни с ранним проявлением признаков старости и одновременно резким сокращением продолжительности жизни. Например, при синдроме Хатчинсона-Гилфорда (инфантильная прогерия, или постарение в детском возрасте) уже на первом году жизни отмечаются задержка роста, раннее облысение, морщины, атеросклероз. Половой зрелости такие субъекты, как правило, не достигают, и смерть наступает в возрасте до 30 лет. Для названного синдрома установлено аутосомно-рецессивное наследование.
В-четвертых, в лабораторных условиях путем близкородственных скрещиваний получены инбредные линии плодовой мухи и мыши, существенно различающиеся по средней и максимальной продолжительности жизни. Гибриды 1-го поколения от скрещивания родителей из разных короткоживущих линий (рис. 1) живут дольше родителей, что расценивают как явление гетерозиса.
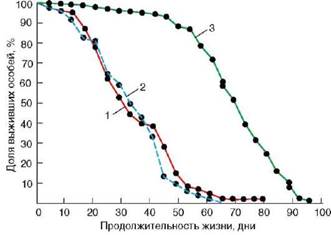
Рис. 1.Явление гетерозиса, заключающееся в увеличении длительности жизни гибридов первого поколения от скрещивания плодовых мух из двух ко-роткоживущих линий: 1 - инбредная линия К; 2 - инбредная линия В; 3 - гибриды F1 (В x К)
В-пятых, замечено, что среди плодовых мух особи, гомозиготные по аллелю зачаточных крыльев, имеют меньшую продолжительность жизни, чем мухи дикого типа (плейотропия). Потомки от скрещивания мутантов и мух дикого типа по рассматриваемому показателю проявляют единообразие и близки к последним. Среди гибридов 2-го поколения от скрещивания таких потомков между собой происходит расщепление по продолжительности жизни в отношении 3:1 (дикий тип: мутантный тип). Аналогично описанной мутации у мыши также обнаружено много примеров влияния отдельных генов на продолжительность жизни, причем в сторону ее снижения. Сходным примером у человека является мутация, приводящая к развитию синдрома Марфана и фенотипически проявляющаяся в дефектном развитии соединительной ткани: наряду с «паучьими» пальцами, подвывихом хрусталика, пороком сердца, повышенным выбросом в кровь адреналина. Такие субъекты отличаются сокращенной продолжительностью жизни.
В-шестых, для людей выявлена положительная связь между длительностью жизни родителей и потомков.
Приведенные материалы, свидетельствуя в пользу генетического контроля длительности жизни и старения, не дают ответа на важные вопросы о том, насколько велика сила этого контроля и через какие конкретные генетические механизмы он осуществляется. Представление о величине наследуемости продолжительности жизни получают, определяя коэффициент наследуемости -он отражает меру сходства между родственниками по изучаемому признаку. По данным разных авторов, коэффициент корреляции между продолжительностью жизни детей и родителей составляет от 0,02 до 0,13, т.е. низок. Сходные цифры получены для мышей: 0,01-0,40. Родители и дети принадлежат к разным поколениям, а условия проживания меняются. С целью избежать занижения значений коэффициента корреляции за счет различий в условиях жизни сопоставляли продолжительность жизни братьев и сестер. В данном случае коэффициент корреляции оказался выше: 0,15-0,30. Однако и здесь значения существенно ниже тех, которые характеризуют признаки с высокой наследуемостью. К примеру, коэффициент наследуемости роста составляет около 0,70.
Данные по коэффициенту наследования долголетия полезно дополнить примерами, раскрывающими их биологический смысл. Так, если пронаблюдать 25-летних людей, предки которых жили либо достаточно мало, либо, наоборот, достаточно долго, то различие между этими группами по средней продолжительности жизни составит всего 2-4 года. Тем не менее, существуют данные о некоторой связи между средней длительностью жизни предков и потомков, прослеживаемой до 70-летнего возраста (табл. 2).
Таблица 2.
Связь между продолжительностью жизни предков и потомков
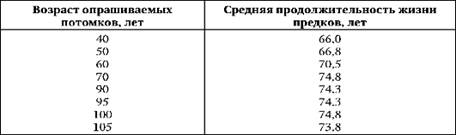
Изучение связи между продолжительностью жизни родителей и детей, достигших 20-летнего возраста, показало, что превышение родителями средней продолжительности жизни на 10 лет добавляет к жизни детей 1 год.
Дата добавления: 2017-02-13; просмотров: 4294;











