Типы окислительно-восстановительных реакций
Рассмотренные выше примеры относятся к типу межмолекулярных реакций, т.е. таких, в которых окислитель и восстановитель представляют различные вещества.
Окисление-восстановление происходит не только при взаимодействии нескольких веществ, но при определенных условиях и в одном веществе, т.е. изменение окислительного числа атомов происходит в одной и той же молекуле. Такие реакции относятся к внутримолекулярным реакциям.
Обычно это реакции термического разложения веществ.
Например
КСlO3 → КСl + O20
 Сl5+ + 6
Сl5+ + 6 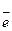 = Сl-1 2
= Сl-1 2
2O-2 - 4 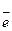 = O20 3
= O20 3

2Сl5+ + 6O-2 = 2Сl
2КСlO3 = 2КСl + 3O2
В реакциях самоокисления - самовосстановления или диспропорционирования в отличие от процессов внутримолекулярного окисления - восстановления происходит одновременное уменьшение и увеличение окислительного числа атомов одного и того же элемента. Например,
K2MnO4 + H2O → KMnO4 + MnO2 + КОН
 MnO42- -
MnO42- - 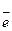 = MnO4- 2
= MnO4- 2
MnO42- + 2H2O + 2 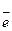 = MnO2 + 4OH- 1
= MnO2 + 4OH- 1

3MnO42- + 2H2O = 2MnO4- + MnO2 + 4OH-
или в молекулярной форме
3K2MnO4 + 2Н2O = 2KMnO4 + 4КОН + MnO2
Из трех молекул K2MnO4 две выступают в качестве восстановителя, одна - в качестве окислителя.
В заключение следует отметить, что окислительно-восстановительные реакции составляют важный раздел курса, т.к. большинство протекающих в природе и используемых в технике процессов являются окислительно-восстановительными.
Знание вопросов теории окислительно-восстановительных процессов позволяет выбрать наиболее эффективные процессы получения металлов из руд, химической и электрохимической обработки металлов, получения различных неорганических веществ и многое другое.
Дата добавления: 2016-12-09; просмотров: 2334;











