Свойства ковалентной связи
Особенностью ковалентной химической связи является ее насыщаемость, направленность и полярность.
Насыщаемость связи. Из приведенных выше примеров следует, что молекулы существуют в устойчивом состоянии
строго определенного состава H2, CH4, BF3, BH4-, BH3 и т.д., но не H3, CH5 и т.д. Таким образом, при образовании ковалентной связи происходит ее насыщение. Объяснить это можно следующим образом: пара электронов (H2, CH4) образующих связь всегда будут отталкивать неспаренный электрон приближающегося третьего атома, т.к. в электронной паре (H2) представлены обе возможности ориентации спина. Кроме того, насыщаемость ковалентной связи можно объяснить тем, что для образования химической связи необходимо оптимальное накопление электронной плотности между ядрами, а ее избыток или недостаток приводит к повышению полной энергии системы.
Направленность связи. Наиболее прочные химические связи возникают в направлении максимального перекрывания атомных орбиталей. Поскольку атомные орбитали имеют определенную форму, то их максимальное перекрывание возможно при определенной пространственной ориентации. Направленность – важнейшее свойство ковалентной связи, зависящее от типа взаимодействующих электронов и числа атомов. Направленность связи объясняется тем, что электронные облака различной формы имеют определенное пространственное направление. s – облако имеет форму сферы, p – облако – форму гантели, расположенные вдоль трех осей (px py pz).
s, p и d - связи. В зависимости от направления перекрывания атомных орбиталей различают s, p и d - связи.
s - связь возникает при перекрывании атомных орбиталей вдоль оси, соединяющей ядра взаимодействующих атомов. Простейший случай s - связи наблюдается у молекулы H2, образуется за счет перекрывания s – орбиталей атомов водорода (рис. 10, а); s - связь может возникнуть также при перекрывании s и p – орбиталей (б); двух p – орбиталей (в); двух d – орбиталей (г); d и s – орбиталей; d и p – орбиталей
а б
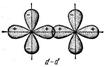
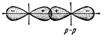
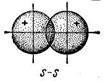
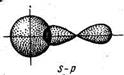
в г
Рис. 10. Схема перекрывания орбиталей
при образовании s - связи
p - связь осуществляется при перекрывании атомных орбиталей по обе стороны оси, соединяющей ядра атомов. При взаимодействии двух p – орбиталей, расположенных перпендикулярно оси, соединяющей ядра атомов, возникают две области перекрывания (рис. 11). Соответственно p - связь характеризуется двумя областями перекрывания, расположенными по обе стороны, соединяющей ядра атомов.
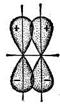
Рис. 11. Схема перекрывания p – орбиталей
при образовании p - связи
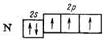
Например, рассмотрим строение молекулы N2
|
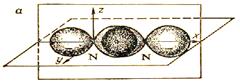 |
Связь осуществляется за счет перекрывания 3 - p – электронных облаков вдоль оси x, y и z
Рис. 12. Образование s - связи в молекуле N2
Перекрывание электронных облаков происходит вдоль линии, соединяющей центры атомов, а также перпендикулярно линии, соединяющей центры
 |
Рис. 13. Образование p - связей в молекуле N2
Как видно, в молекуле N2 между атомами азота осуществляется одна s - связь (рис. 12) и две p - связи (рис. 13).
|
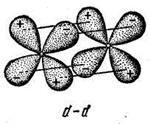
Рис. 14. Схема образования d - связи
d - связь возникает при перекрывании двух d – атомных орбиталей, расположенных в параллельных плоскостях, четырьмя лепестками (рис. 14).
Таким образом, s– электроны могут участвовать лишь в образовании s - связи, p– электроны – в образовании s и p - связей, а d– электроны – как в образовании s и p - связей, так и d - связей.
p - и d - связи налагаются на s - связи, вследствие чего образуются двойные и тройные, как, например, в молекуле азота. Количество связей, образующих между атомами, называется кратностью (порядком) связи. С увеличением кратности связи изменяются длина связи и ее энергия. Энергия двойной связи не увеличивается в два раза, а энергия тройной связи не увеличивается в три раза по сравнению с энергией одинарной связи. Это вызвано тем, что энергия p - связи меньше, чем энергия s - связей; p - связь менее прочная, чем s - связь и разрушается при химических взаимодействиях в первую очередь.
Гибридизация атомных орбиталей. При образовании нескольких химических связей иногда участвуют различные атомные орбитали одного и того же атома. Например, в молекуле метана четыре химические связи образованы путем перекрывания трех p и одной s – орбитали атома углерода с четырьмя s – орбиталями атомов водорода. Так как энергия и форма s и p – орбиталей различны, то можно было бы ожидать, что одна из четырех связей в молекуле метана будет отличать-
ся от других связей по прочности и по характеру направленно-
сти. Однако эксперименты показали, что все четыре связи в молекуле метана равноценны. Этот и другие подобные факты удалось объяснить при помощи теории гибридизации. Согласно этой теории при образовании молекул происходит изменение формы и энергии атомные орбиталей. Вместо неравноценных, например, s и p – орбиталей образуются равноценные гибридные орбитали, имеющие одинаковую форму и энергию, т.е. происходит гибридизация (смешение) атомных орбиталей. При образовании химических связей с участием гибридных орбиталей выделяется больше энергии, чем при образовании связей с участием отдельных s и p – орбиталей, поэтому гибридизация атомных орбиталей приводит к большему понижению энергии системы и соответственно повышению устойчивости молекулы.
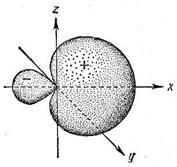
Рис. 15. Форма sp – гибридной орбитали
Гибридная орбиталь по форме отличается от атомных орбиталей. Так, гибридная s и p – орбиталь отличается большей вытянутостью по одну сторону от ядра, чем по другую (рис. 15).
Электронная плотность в области перекрывания гибридного электронного облака будет больше электронной плотности в области перекрывания отдельно s и p – орбиталей. Поэтому связь, образованная электронами гибридной орбитали характеризуется большей прочностью, чем связь, образованная электронами отдельно s - или p - орбитали.
Дата добавления: 2016-12-09; просмотров: 2042;











