Закон действующих масс
Состав топлива
Органическая часть твердых и жидких топлив состоит из большого количества сложных химических соединений, образованных пятью химическими элементами: углерод (С), водород (Н), сера (S), кислород (О) и азот (N). Кроме того, топливо содержит минеральные примеси (А), которые превращаются при сжигании в золу и влагу (W). Поэтому химический состав твердых и жидких топлив определяется не по количеству химических соединений, а по суммарной массе химических элементов в топливе в процентах на один килограмм, т. е. по элементному составу топлива.
Горючими элементами топлива являются углерод, водород, сера. Углерод является основным горючим элементом топлива, имеет высокую теплоту сгорания (34,4 МДж/кг) и составляет большую часть горючей массы топлива. Водород также имеет высокую теплоту сгорания (120,5 МДж/кг), но его содержание в топливе невелико (2-4% в твердом и 10-11% в жидком). Сера имеет невысокую теплоту сгорания (9,3 МДж/кг), и ее содержание в топливе невелико (0,3-0,5%), поэтому она не представляет ценности как горючий элемент. Но поскольку при сжигании топлива образуется диоксид серы, сернистость топлива является важной характеристикой. В твердом топливе сера присутствует в органическом виде Sор, в составе горючих минеральных веществ (пиритная Sп или колчеданная сера FeS2, CuS), в составе негорючих минеральных веществ (сульфатная сера Sсфт). Общее содержание серы в топливе Sоб складывается из трех составляющих:
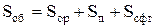 .
.
Сумма двух первых слагаемых определяет содержание в топливе горючей серы:
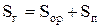 .
.
Различают пять основных состояний топлива. Рабочее состояние топлива (верхний индекс р (r)) – это состояние топлива с таким содержанием влаги и зольностью, с которым оно добывается, отгружается или используется:
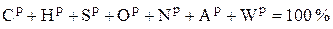 . (1.1)
. (1.1)
Аналитическое состояние топлива (верхний индекс а (а)) – состояние топлива, характеризуемое подготовкой пробы. Подготовка предусматривает размол до размеров частиц 0,2 мм и приведение в равновесие с условиями лабораторного помещения:
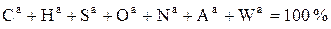 . (1.2)
. (1.2)
Сухое состояние топлива (верхний индекс с (d)) – состояние топлива без содержания общей влаги (кроме гидратной):
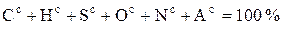 . (1.3)
. (1.3)
Горючее (условное сухое беззольное) состояние топлива (верхний индекс г (daf)) – условное состояние топлива, не содержащего общей влаги и золы:
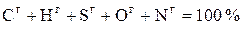 . (1.4)
. (1.4)
Органическое состояние топлива (верхний индекс о (о)) – условное состояние топлива без содержания влаги и минеральной массы:

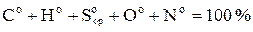 . (1.5)
. (1.5)
| Wвн | Wа | О | N | H | C | Sор | Sп | Sсфт | А |
| Органическое состояние (о) | |||||||||
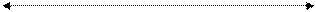  Горючее состояние (г) Горючее состояние (г)
| |||||||||
 Сухое состояние топлива (с) Сухое состояние топлива (с)
| |||||||||
| Аналитическое состояние топлива (а) | ||||||||
 Рабочее состояние топлива (р) Рабочее состояние топлива (р)
|
Рис. 1.1. Схема состояний топлива
Для получения коэффициента пересчета состава топлива, например, из горючего состояния в рабочее необходимо сделать следующие преобразования. Запишем уравнение для рабочего состояния в следующем виде, %:
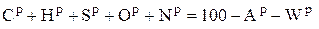 , (1.6)
, (1.6)
и разделим (1.6) на (1.4). В результате получим соотношение
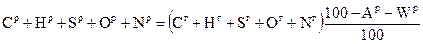 . (1.7)
. (1.7)
Таким образом, для каждого элемента, например для углерода, справедливо соотношение
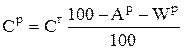 , %. (1.8)
, %. (1.8)
Аналогичным образом определяются коэффициенты пересчета для любых других состояний (табл. 1.1).
Таблица 1.1
Коэффициенты пересчета из одного состояния в другое
| Заданное состояние топлива | Искомое состояние топлива | ||
| Рабочее | Сухое | Горючее | |
| Рабочее | 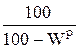
| 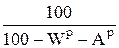
| |
| Сухое | 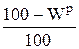
| 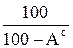
| |
| Горючее | 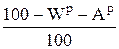
| 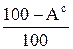
|
В отличие от твердого и жидкого топлива газообразное топливо представляет собой механическую смесь горючих и негорючих газов, поэтому его состав задается в объемных процентах.
1.2. Теплота сгорания топлива
Теплота сгорания характеризует энергетическую ценность топлива и представляет собой количество тепловой энергии, выделяющейся в ходе химических реакций окисления горючих элементов газообразным кислородом. Различают высшую и низшую теплоту сгорания. Высшей теплотой сгорания Qв топлива называется количество теплоты, выделяющееся при полном сгорании 1 кг твердого или жидкого топлива (1 м3 газообразного топлива) при условии конденсации водяных паров и охлаждении всех продуктов сгорания до 0 °С. Низшая теплота сгорания Qн отличается от высшей на величину теплоты испарения влаги топлива и влаги, образующейся при горении водорода. При сжигании топлива в энергетических установках температура уходящих газов превышает 100 °С, влага, содержащаяся в продуктах сгорания, остается в парообразном состоянии и теплота испарения теряется. Количество водяного пара (кг) в продуктах сгорания, которое приходится на 1 кг топлива, представляет собой сумму количества влаги, содержащейся в исходном топливе Wр/100 и образовавшейся при окислении водорода топлива 9Hр/100 ( 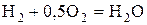 ); из одного килограмма водорода образуется 9 кг влаги). Удельная теплота конденсации водяного пара в нормальных физических условиях составляет 2500 кДж/кг. В итоге теплота конденсации водяных паров, образовавшихся из 1 кг топлива, составляет, кДж/кг:
); из одного килограмма водорода образуется 9 кг влаги). Удельная теплота конденсации водяного пара в нормальных физических условиях составляет 2500 кДж/кг. В итоге теплота конденсации водяных паров, образовавшихся из 1 кг топлива, составляет, кДж/кг:
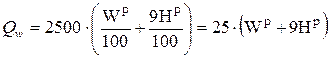 . (1.9)
. (1.9)
Тогда взаимосвязь высшей и низшей теплоты сгорания имеет вид, кДж/кг:
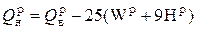 . (1.10)
. (1.10)
| Рис. 1.2. Калориметрическая установка: 1 – калориметрическая бомба; 2 – калориметрический сосуд; 3 – наружная оболочка; 4 – термометр; 5 – крышка; 6 – мешалка с приводом |
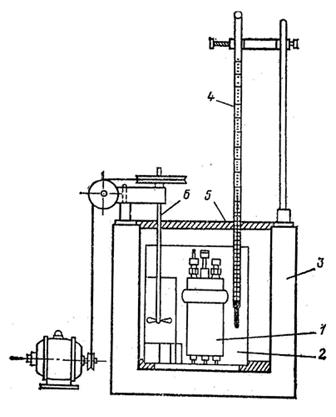
Наиболее надежным способом определения теплоты сгорания является ее экспериментальное измерение на специальных установках – калориметрах (рис. 1.2, СТ СЭВ 1463-78). Сущность метода заключается в том, что навеску топлива сжигают в атмосфере сжатого кислорода в герметически закрытом металлическом сосуде – калориметрической бомбе, которую погружают в определенный объем воды. Количество теплоты, выделяющееся при сгорании этого топлива, определяют по повышению температуры этой воды.
Тепловой эффект, измеряемый с помощью калориметра, соответствует высшей теплоте сгорания, так как образующийся при горении в бомбе водяной пар конденсируется. Однако реальное значение Qв не совпадает c измеренным, поэтому ему присвоено специальное обозначение 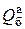 - теплота сгорания аналитической пробы в бомбе. Отличие
- теплота сгорания аналитической пробы в бомбе. Отличие 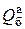 от
от 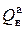 обусловлено значительно завышенной концентрацией кислорода в бомбе, приводящей к несколько иному составу продуктов сгорания. Так, сера окисляется не до SO2, а до SO3, причем SO3 растворяется в воде с дополнительным тепловым эффектом. Кроме того, происходит частичное окисление азота с образованием азотной кислоты.
обусловлено значительно завышенной концентрацией кислорода в бомбе, приводящей к несколько иному составу продуктов сгорания. Так, сера окисляется не до SO2, а до SO3, причем SO3 растворяется в воде с дополнительным тепловым эффектом. Кроме того, происходит частичное окисление азота с образованием азотной кислоты.
В практике электростанций теплоту сгорания используемого топлива определяют опытным путем, дающим более точные результаты. При проведении теплотехнических расчетов нередко возникает необходимость оценки теплоты сгорания топлива по данным элементного состава. Метод определения теплоты сгорания по данным элементного состава топлива основан на использовании закона Гесса, согласно которому теплота прямого превращения топлива в продукты сгорания СО2, Н2О, SО2 равна теплоте сгорания С, Н2, S за вычетом теплоты разложения исходных углеводородов топлива на простые вещества. В реальных топливах О, H и C связаны между собой в очень сложные молекулы с различными энергиями связи. Поскольку на разрыв этих связей при сжигании затрачивается различное количество энергии, поэтому до сих пор ни одно из модельных представлений не позволило получить универсальной формулы, позволяющей рассчитывать теплоту сгорания любого топлива. Наиболее удачной, т.е. простой и точной, является формула Д.И. Менделеева с эмпирически подобранными коэффициентами для соответствующих горючих элементов, ккал/кг:
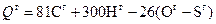 . (1.11)
. (1.11)
Теплота сгорания твердого и жидкого топлива в рабочем состоянии рассчитывается так, кДж/кг:
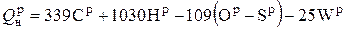 , (1.12)
, (1.12)
содержание элементов выражается в процентах.
Для газообразных топлив при точно известном их составе теплота сгорания 1м3 сухого газа, МДж/м3, может быть достаточно точно подсчитана по формуле
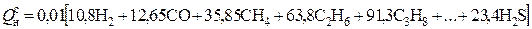 . (1.13)
. (1.13)
Здесь содержание соответствующих газовых компонентов подставляют в процентах.
Топочные устройства одинаковой мощности могут потреблять существенно разные количества топлива, так как теплота сгорания у разных видов меняется в широких пределах. Для сравнения экономичности работы на различных видах топлива введено понятие условного топлива, имеющего теплоту сгорания Qу = 7000 ккал/кг (29,33 МДж/кг). Тепловая мощность топочного устройства N связана с расходом B топлива и теплотой сгорания очевидным соотношением, МВт,
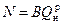 . (1.14)
. (1.14)
Расход условного Bу топлива связан с расходом В натурального топлива соотношением
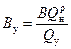 .
.
1.3. Влага твердого топлива
Вода в твердом топливе находится в виде капель, пленок, капиллярной влаги и молекул, адсорбированных на поверхности. Влага также может входить в состав минеральных соединений. В зависимости от конкретных форм связи с топливом различают нижеследующие виды влаги:
1. Гидратная влага – вода, входящая в состав кристаллогидратов, которые присутствуют среди минеральных примесей топлива и представлены в виде силикатов (Al2O3·2SiO2·2H2O, Fe2O3·2SiO2·2H2O) и сульфатов (CaSO4·2H2O, MgSO4·2H2O). Удаление гидратной влаги происходит только при достаточно высоких температурах. Доля гидратной влаги возрастает с увеличением зольности топлива и обычно составляет лишь несколько процентов от общего содержания воды в топливе.
2. Сорбционная влага включает в себя адсорбционную влагу (за счет адсорбции на поверхности раздела газовой и твердой фаз) и коллоидную, входящую в структуру органического топлива. Характерной особенностью сорбционной влаги является зависимость равновесного содержания сорбционной влаги от внешних условий – температуры и влажности воздуха.
3. Капиллярная влага – влага, которая заполняет поры. Поры с диаметром более 10-5 мм заполняются при прямом контакте с водой, в порах с меньшим размером возможна конденсация влаги из воздуха.
4. Поверхностная влага – влага, располагающаяся снаружи частиц топлива. Длительность существования поверхностной влаги зависит от начальной влажности топлива и от температуры и влажности воздуха.
Отсутствие четких границ между отдельными видами влаги затрудняет их определение. Для удобства определения влаги в угле в соответствии с принятыми на практике методами анализа общую влагу угля подразделяют на внешнюю и влагу воздушно-сухого топлива.
С точки зрения представления о видах влаги такое деление можно определить следующим образом. При высушивании угля на воздухе удаляется свободная влага с внешней поверхности частиц и капиллярная влагаиз открытых трещин и пор. В воздушно-сухом угле остается адсорбционная и гидратная влага. Влага общая, кроме гидратной, удаляется при высушивании угля при t = 105 °С.
Определение общей влаги проводят двухступенчатым методом по ГОСТ 27314-87. Общую влагу Wоб рассчитывают как сумму внешней влаги Wвн и влаги воздушно-сухого топлива Wh.
Первую ступень – определение внешней влаги – проводят сушкой навески угля до постоянной массы при комнатной температуре или в сушильных шкафах при t = 40 °С для бурых и при t = 50 °С для каменных углей и горючих сланцев.
Вторая ступень – определение влаги воздушно-сухого топлива – проводится из пробы, доведенной до воздушно-сухого состояния при определении внешней влаги и затем измельченной до размеров лабораторной пробы (крупность частиц менее 3 мм). Влагу воздушно-сухого топлива определяют высушиванием при 105-110 °С в течение 3-4 часов либо ускоренным методом высушивания при температуре (160±5)°С (время сушки 5-10 минут).
При расчете внешней влаги Wвн убыль массы относят к навеске исходного влажного топлива, а при расчете Wh – к навеске воздушно-сухого. Для того чтобы иметь возможность сложить эти величины, необходимо отнести их к одинаковому состоянию топлива – исходному влажному топливу. Если принять массу исходного влажного топлива за 100 %, а массу воздушно-сухого топлива за (100–Wвн), то для пересчета содержания влаги воздушно-сухого топлива содержание влаги в исходном уголе надо умножить Wh на коэффициент 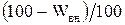 . Отсюда найдем содержание общей влаги, %, по формуле
. Отсюда найдем содержание общей влаги, %, по формуле
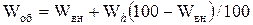 . (1.15)
. (1.15)
Наличие в топливе влаги неблагоприятно отражается на его основных технологических характеристиках: снижает теплоту сгорания, увеличивает объем продуктов сгорания, что приводит к снижению КПД топочных устройств.
Изменение теплоты сгорания твердого топлива при изменении его влажности от 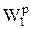 до
до 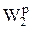 может быть рассчитано по выражению, кДж/кг,
может быть рассчитано по выражению, кДж/кг,

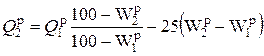 . (1.16)
. (1.16)
Увеличение влажности топлива ведет к снижению подвижности его частиц вплоть до полной потери сыпучести. Влага, соответствующая такому состоянию, при котором топливо лишается сыпучести, называется влагой сыпучести. Для большинства топлив влага сыпучести всего на несколько процентов превышает рабочую.
Наибольшее содержание влаги в топливе, при котором еще не происходит его смерзание при отрицательных температурах, характеризуется влагой смерзания, которая обычно меньше рабочей. Влага смерзания уменьшается при снижении выхода летучих и зольности. На практике нашли применение следующие способы борьбы со смерзанием: обезвоживание (путем отстаивания, нагревания и центрифугирования), вымораживание с перелопачиванием, добавка несмерзающихся материалов, обмасливание нефтепродуктами, разгрузка с применением устройств для дробления, обогрев бункеров, разогрев в вагонах.
1.4. Минеральные примеси твердого топлива
Присутствие в твердых топливах минеральных компонентов обусловлено следующими причинами:
1. Наличие минеральных органических веществ в исходном органическом материале, из которого образовалось топливо. Количество примесей такого происхождения (солей) невелико – до 0,5% сухой массы топлива. Их называют первичными примесями.
2. Накопление в залежи вместе с органическим материалом минеральных веществ, заносимых водой и ветром и образующихся в результате жизнедеятельности бактерий. Вместе с первичными примесями их называют внутренними примесями.
3. Попадание в топливо минералов из окружающих горных пород при разработке месторождения. Доля их зависит от геологии пласта и способа его разработки. С увеличением механизации добычи эта доля минеральных примесей значительно возрастает.
Примеси твердого топлива образованы большим числом различных минеральных веществ, главными из которых обычно являются алюмосиликаты (Al2O3·2SiO2·2H2O), кремнезем (SiO2), карбонаты (CaCO3, MgCO3, FeCO3), сульфиды (FeS2, CaS), сульфаты (CaSO4, MgSO4), соли щелочных металлов (NaCl, KCl). Помимо перечисленных основных компонентов в минеральных примесях твердого топлива присутствуют часто в повышенных концентрациях соединения многих редких элементов: платины, палладия, никеля, кобальта, германия, урана и др.
При сжигании топлива многие компоненты его минеральных примесей подвергаются химическим преобразованиям, при которых масса и состав образующейся золы всегда отличаются от массы и состава исходных минеральных примесей топлива:
1. При температуре выше 500 °С протекают реакции дегидратации, т. е. удаление гидратной влаги из гипса, алюмосиликатов (глин), оксидов и гидроксидов железа с образованием Аl2О3, SiO2, Fe2О3 и Н2O:
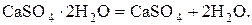
2. В интервале температур 500-900 °С происходит разложение карбонатов с выделением диоксида углерода:
Са(Мg, Fе)СО3 =Са (Мg, Fе)O+СО2.
3. При 400-500 °С начинается окисление дисульфидов железа:
4FeS2+11O2=2Fe2O3+8SO2.
4. Разложение сульфата железа протекает при 850-950 °С:
2FeSO4=2FeO+2SO2+O2.
5. Окисление соединений Fe+2 до Fe+3 начинается при температуре более 400 °С:
FеО+О2=2Fе2О3.
6. Улетучивание хлоридов и соединений щелочных металлов происходит при температуре выше 500 °С.
7. Образование сульфата кальция происходит в интервале температур 700-1000 °С:
2СаО+2SO2+О2=2СаSO4.
Эта реакция протекает по мере выделения SO2 при сгорании органической серы и окислении дисульфида железа, а также разложения карбонатов, содержащихся в минеральной массе углей. Именно благодаря протеканию этой реакции возможно эффективное связывание оксидов серы в топках с низкотемпературным кипящим слоем. При температурах выше 1000 °С начинается диссоциация сульфатов.
При рассмотрении реакций, происходящих с минеральными примесями топлив, можно сделать следующие общие выводы:
1. В процессе сжигания углей химический состав минеральной массы значительно изменяется, поэтому масса и состав золы никогда не равны массе и составу минеральных веществ угля.
2. Среди реакций, протекающих в минеральной массе при озолении углей, преобладают реакции разложения, поэтому зольность угля почти всегда получается несколько меньше, чем содержание минеральной массы.
3. Каждая из приведенных реакций протекает на определенных стадиях озоления угля и в определенном интервале температур. В соответствии с этим масса и состав золы, полученной при озолении одного и того же угля, при разных температурах (800 и 1500 °С) будут значительно отличаться друг от друга.
Следовательно, зольность угля – понятие в известной мере условное, так как масса и состав золы зависят в основном от условий озоления топлива и прежде всего от скорости озоления и конечной температуры прокаливания.
Зольность угля – это масса золы, определяемая в установленных условиях, отнесенная к единице массы угля и выраженная в процентах. Стандартный метод определения зольности углей (ГОСТ 11022-75, СТ СЭВ 1461-78) заключается в полном сжигании навески топлива (озолении), прокаливании зольного остатка до постоянной массы при (815±15) °С и определении массы образовавшейся золы. Метод может выполняться по двум вариантам: медленное и ускоренное озоление. При медленном озолении зольный остаток прокаливают в течение 1 ч при анализе бурых углей и горючих сланцев и 1,5 ч при анализе каменных углей и антрацитов. Сущность ускоренного озоления заключается в постепенном продвижении лодочек с навесками в нагретую до (815±15) °С муфельную печь. Лодочки помещают на пластинку из жаропрочного материала, устанавливают на откинутую крышку муфеля и выдерживают в таком положении 3-5 мин. Затем пластинку продвигают внутрь муфеля со скоростью 2 см/мин, закрывают дверцу печи и прокаливают зольные остатки бурых углей и горючих сланцев 25 мин, каменных углей и антрацитов – 35 мин.
Несгоревшая часть топлива образует очаговые остатки, которые в зависимости от условий сжигания и от местонахождения в разных частях топки и газоходах могут принимать форму шлака или золы. Шлак – это минеральная масса, подвергшаяся высокотемпературному нагреву, в результате которого она приобрела значительную прочность за счет оплавления и спекания. Зола – порошкообразный остаток топлива. Различают летучую золу – пылевидные фракции, уносимые уходящими газами, и провал – более крупные фракции золы. Условия сгорания топлива в топочных устройствах резко отличаются от лабораторных условий озоления, в результате чего состав и свойства очаговых остатков не совпадают с таковыми для лабораторной золы. Отличия обусловлены следующими основными причинами:
1. Время пребывания топлива в топке существенно меньше, чем при стандартном озолении (5 с в котле БКЗ-75 и ~ 30 мин при стандартном озолении).
2. Температура в топке значительно больше, чем при стандартном озолении (1500 °С в факеле и 815 °С при стандартном озолении).
3. Ограниченное количество окислителя в топочном устройстве и наличие восстановительных зон приводит к тому, что некоторые окислительные реакции в минеральной части проходят не полностью.
4. Образование расплава благоприятствует взаимодействию между отдельными компонентами минеральной части топлива.
Поведение очаговых остатков при высоких температурах (их размягчение, плавление, текучесть образующегося расплава) относится к числу важнейших технологических характеристик топлива, влияющих на конструкцию топки, ее надежность, а также на эксплуатационные затраты. Очаговые остатки как многокомпонентные системы не имеют определенной температуры плавления. Переход из твердого состояния в жидкое происходит в определенном температурном интервале. Наибольшее раcпространение при определении плавкости золы и шлака получил метод конусов (ГОСТ 2057-82). Из золы прессуют пирамидку высотой 13 мм с основанием 6 мм (рис. 1.3), которую затем помещают в высокотемпературную муфельную печ, и постепенно повышают в ней температуру. В ходе нагревания образца фиксируют следующие температуры: температуру начала деформации tA, которую определяют по появлению первых признаков оплавления конуса; температуру полусферы tB, при которой образец превращается в полусферу с высотой, равной примерно половине основания, и температуру перехода в жидкоплавкое состояние tC, при котором образец растекается по подставке.
Шлакование котла - прогрессирующее накопление в топке и газоходах отложений очаговых остатков, сопровождающееся упрочнением этих отложений. Интенсивность шлакования во многом зависит от состава и свойств минеральной части топлива. Накопление шлаковых отложений начинается с появления на поверхности так называемого первичного слоя, в образовании которого важное место занимает конденсация паров легколетучих компонентов минеральной части топлива – главным образом оксидов (K2O, Na2O) и хлоридов (NaCl, KC) щелочных металлов. На поверхности первичного слоя происходит рост рыхлого вторичного слоя отложений, температура поверхности которого быстро увеличивается и может превысить температуру появления жидкой фазы, что ускоряет рост толщины слоя.
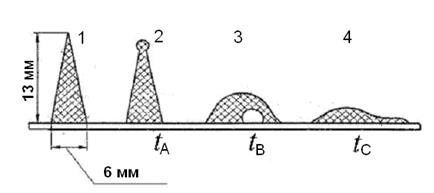
Рис. 1.3. Характерные конфигурации образца при определении плавкости золы методом конусов: 1 – до нагрева; 2 – начало деформации, 3 – размягчение; 4 – жидкоплавкое состояние
При сжигании твердого топлива во многих случаях целесообразен перевод минеральной части топлива в расплавленное состояние и непрерывный вывод образующегося шлака через лётку в нижней части топки. Такой метод удаления очаговых остатков получил название жидкое шлакоудаление.
1.5. Выход летучих веществ и характеристика коксового остатка
При нагревании твердого топлива до высоких температур происходит разложение углеводородов (в основном кислородсодержащих молекул) с образованием газообразных продуктов (CO, H2, CH4, CO2 и др.), получивших название «летучие вещества». Выход летучих веществ из твердого топлива происходит в интервале температур 110-1100 °С. После удаления летучих веществ из зоны нагрева остается твердый остаток, называемый коксовым остатком.
Выход летучих веществ в горючем состоянии «г» является одним из классификационных параметров каменных углей и антрацитов. Выход летучих веществ и характеристики нелетучего остатка позволяют оценить пригодность углей для коксования, а также предугадать поведение топлива в технологических процессах переработки и предложить рациональные способы сжигания.
Выход летучих веществ зависит, главным образом, от температуры нагрева пробы и увеличивается с повышением температуры в результате более глубокого разложения топлива. Известно, что основная масса летучих веществ образуется при нагреве угля до 800-850 °С. При дальнейшем повышении температуры выход летучих веществ увеличивается незначительно.
Выделение основной массы летучих веществ заканчивается через 6-7 мин нагрева при 850 °С. Дополнительная выдержка при этой температуре незначительно увеличивает выход летучих веществ.На выход летучих веществ значительно влияет скорость прогрева частиц угля.
Сущность стандартного метода определения выхода летучих веществ (ГОСТ 6382-80, СТ СЭВ 2033-79) заключается в нагревании навески аналитической пробы топлива массой 1 г без доступа воздуха при t = (850±10) °С в течение 7 мин. Выход летучих веществ определяется в зависимости от потери массы исходной навески с учетом содержания влаги в топливе.
Способность углей спекаться имеет большое значение при их технологическом использовании. Спекающиеся угли служат сырьем для получения кокса, который применяют в качестве восстановителя в доменном процессе при выплавке металла из руд. Такие угли более ценные, чем неспекающиеся, которые используются для энергетических целей.
Спекание углей представляет собой сложный процесс, в котором условно можно выделить две стадии:
1) размягчение частиц угля, благодаря чему они становятся пластичными (переход в пластическое состояние);
2) образование из пластической массы твердого остатка.
Спекающиеся каменные угли переходят в пластическое состояние при температуре выше 300 °С. При температуре 500-550 °С пластическая масса затвердевает и образуется спекшийся твердый остаток – полукокс. При дальнейшем повышении температуры вплоть до 1000 °С происходит увеличение твердости и прочности кокса.
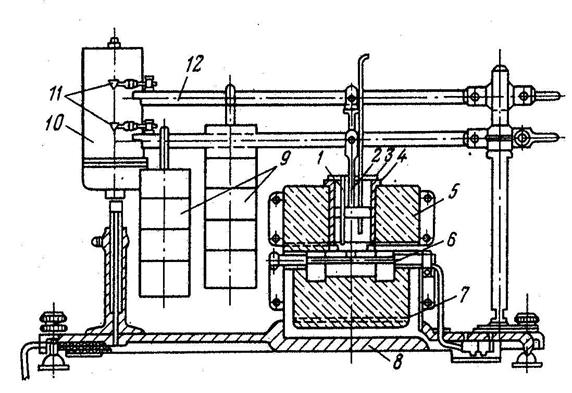
Рис. 1.4. Пластометрический аппарат:
1 – трубка для термопары; 2 – штемпель; 3 – прижимная планка; 4 – стакан; 5 – верхний кирпич; 6 – нагреватель; 7 – нижний кирпич; 8 – плита; 9 – груз; 10 – барабан с часовым механизмом; 11 – перья; 12 – рычаг
Методика определения пластометрических показателей установлена ГОСТ 186-69 и СТ СЭВ 5775-86. Испытания проводят в пластометрическом аппарате (рис. 1.4), основными составными частями которого являются: пластометрический стакан из стали с вынимающимся дырчатым дном; пластометр, состоящий из стальной иглы, передвижной шкалы и указателя; штемпель с отверстиями для удаления летучих продуктов; рычаги и грузы для создания давления на загрузку угля; карборундовые нагреватели, помещенные в корпус из огнеупорных кирпичей.
Условия проведения испытаний в пластометрическом аппарате сходны с условиями коксования углей в промышленности. Уголь находится под нагрузкой и нагревается с одной стороны от дна стакана. При этом на разных расстояниях от поверхности нагрева уголь будет находиться на разных стадиях превращения в кокс. Ближе всего к поверхности нагревания будет находиться слой кокса и полукокса, затем слой пластической угольной массы (пластический слой), а над пластической массой – уголь, который еще не перешел в пластическое состояние. Эти слои располагаются параллельно поверхности нагрева. При повышении температуры часть пластической массы затвердевает, слой полукокса увеличивается, а нагревающийся уголь переходит в пластическое состояние. Чем дольше уголь находится в пластическом состоянии, тем толще становится пластический слой.
С помощью пластометрического метода определяют толщину пластического слоя у – это максимальное расстояние между поверхностями раздела «уголь – пластическая масса» и «пластическая масса – полукокс» (рис. 1.5).
Для проведение испытаний навеску угля (100±1) г крупностью менее 1,6 мм помещают в пластометрический стакан. Сверху на уголь устанавливают штемпель с рычагом, на который подвешен груз. Давление на угольную загрузку составляет 0,1 МПа. Нагревание проводят таким образом, чтобы через 30 мин после начала опыта температура на поверхности дна стакана достигала 250 °С. Затем до 730 °С нагрев ведут со скоростью 3°С в минуту. Начиная с
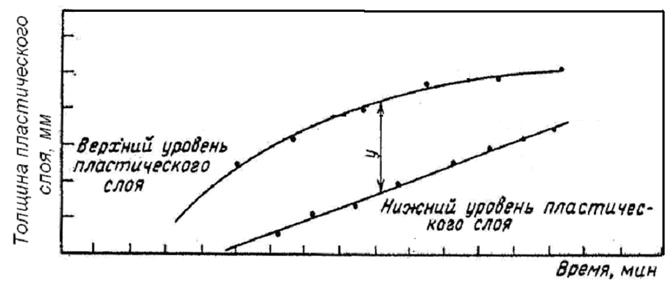
Рис. 1.5. График пластометрических испытаний
350 °С через определенные промежутки времени измеряют верхний и нижний уровни пластического слоя.
1.6. Характеристики и классификация твердого топлива
Древесина. Характерные свойства: V г=85 %, W р=40 %, А р=0,6 %, 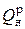 =10-12 МДж/кг, сера практически отсутствует. Древесина как топливо используется редко и в основном в виде отходов (опил, щепа).
=10-12 МДж/кг, сера практически отсутствует. Древесина как топливо используется редко и в основном в виде отходов (опил, щепа).
Торф. Характерные свойства: V г=70 %, W р=48-53 %, А р=3-19 %, 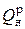 =8,4-10,5 МДж/кг, высокое содержание кислорода. По способу добычи различают кусковой и фрезерный (мелкая крошка) торф. Торф характеризуется плохой сыпучестью, склонностью к слеживанию, повышенной взрывоопасностью, высокой гигроскопичностью и легкостью смерзания.
=8,4-10,5 МДж/кг, высокое содержание кислорода. По способу добычи различают кусковой и фрезерный (мелкая крошка) торф. Торф характеризуется плохой сыпучестью, склонностью к слеживанию, повышенной взрывоопасностью, высокой гигроскопичностью и легкостью смерзания.
Горючие сланцы. Характерные свойства: V г=85-90 %, А с=40-65 %, W р £ 13 %; 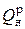 =5,5-13,9 МДж/кг, сера практически отсутствует.
=5,5-13,9 МДж/кг, сера практически отсутствует.
В топливном балансе страны доля древесины, торфа и сланцев невелика, эти топлива относятся к местным низкосортным видам, которые следует использовать вблизи места добычи.
Основное ископаемое твердое топливо – угли, которые делятся на два основных вида: бурые и каменные.
Бурые угли. Характерными свойствами бурого угля являются большая гигроскопичность, определяющая высокую влажность, большой выход летучих V г > 40 %; невысокая теплота сгорания, отсутствие спекаемости, склонность к самовозгоранию. По принятой классификации к бурым углям относят угли с высшей теплотой сгорания рабочей массы беззольного топлива 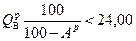 МДж/кг. По содержанию влажности в рабочем состоянии бурые угли делятся на три группы: Б1 (Wp > 40 %), Б2 (Wр 30-40 %), Б3 (Wр £ 30 %).
МДж/кг. По содержанию влажности в рабочем состоянии бурые угли делятся на три группы: Б1 (Wp > 40 %), Б2 (Wр 30-40 %), Б3 (Wр £ 30 %).
Каменные угли. К каменным относятся угли с высшей теплотой сгорания в условном беззольном состоянии 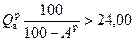 МДж/кг и с массовым выходом летучих Vг > 9 %. Каменные угли весьма разнообразны по своим свойствам и составу, поэтому их единая классификация затруднена. Поскольку единой классификации не существует, используются бассейновые классификации. В число классификационных признаков входят выход летучих, характеристика нелетучего остатка коксования и степень спекаемости угля. По этим признакам выделены основные марки каменных углей, в частности для Кузнецкого бассейна (табл. 1.2). Угли марок от газового жирного до отощенного спекающегося пригодны для получения металлургического кокса и являются сырьем металлургической промышленности. Каменные угли малой (длиннопламенные и газовые) и высокой степени углефикации (слабоспекающиеся, тощие, антрациты) используются в качестве топлива в энергетике и коммунальном хозяйстве.
МДж/кг и с массовым выходом летучих Vг > 9 %. Каменные угли весьма разнообразны по своим свойствам и составу, поэтому их единая классификация затруднена. Поскольку единой классификации не существует, используются бассейновые классификации. В число классификационных признаков входят выход летучих, характеристика нелетучего остатка коксования и степень спекаемости угля. По этим признакам выделены основные марки каменных углей, в частности для Кузнецкого бассейна (табл. 1.2). Угли марок от газового жирного до отощенного спекающегося пригодны для получения металлургического кокса и являются сырьем металлургической промышленности. Каменные угли малой (длиннопламенные и газовые) и высокой степени углефикации (слабоспекающиеся, тощие, антрациты) используются в качестве топлива в энергетике и коммунальном хозяйстве.
Для использования углей в ряде производств важно поставлять уголь с определенным размером кусков. Угли по ГОСТ 19242-73 подразделяют на классы в соответствии с размером кусков, мм:
плитный (П)…………………100 - 200
крупный (К)……………….…50 - 100
орех (О)………………………25 - 50
мелкий (М)…………………...13 - 25
семечко (С)……………………6 - 13
штыб (Ш)…………………...…0 - 6
рядовой (Р)……………………0 - 200
Таблица 1.2
Классификация каменных углей Кузнецкого бассейна [4]
| Наименование угля | Обозначение | Группы | Выход лету-чих Vг, % | Толщина пласти-ческого слоя, мм |
| Длиннопламенный | Д | - | >37 | - |
| Газовый | Г | Г6 | >37 | 6-16 |
| Г17 | >37 | 17-25 | ||
| Газовый жирный | ГЖ | - | 31-37 | 6-25 |
| Жирный | Ж | 1Ж26 | > 33 | 26 и более |
| 2Ж26 | 33 и менее | 26 и более | ||
| Коксовый жирный | КЖ | КЖ14 | 25-31 | 14-25 |
| КЖ6 | 25-31 | 6-13 | ||
| Коксовый | К | К13 | <25 | 13-25 |
| К10 | 17-25 | 10-12 | ||
| Коксовый второй | К2 | - | 17-25 | 6-9 |
| Отощенный спекающийся | ОС | - | <17 | 6-9 |
| Слабоспекающийся | СС | 1СС | 25-17 | - |
| 2СС | 17-25 | - | ||
| Тощий | Т | - | Менее 17 | - |
| Антрацит | А | - | Менее 7 | - |
1.7. Жидкое топливо
Основным видом жидкого энергетического топлива является мазут, получаемый в процессе переработки нефти. Мазуты получают на нефтеперерабатывающих заводах одновременно с производством других продуктов (моторных топлив, масел и др.). В зависимости от условий различают неглубокую переработку нефти (разгонку) и глубокую (крекинг). При разгонке нефть разделяется на узкие фракции по температурам их выкипания без разрушения молекулярной структуры, а при крекинге достигается разрушение молекул исходных углеводородов, с образованием новых соединений. Наряду с легкими продуктами при крекинге нефтяных фракций образуются более сложные и тяжелые жидкие углеводороды – гудрон и полугудрон, а также твердые вещества высокой степени науглероженности.
Мазут, получаемый при неглубокой переработке нефти, называют прямогонным, при глубокой переработке нефти – крекинг-мазутом.
В соответствии с ГОСТ 10585-75 установлены следующие марки мазутов: флотский Ф 5 и Ф 12; топочный М 40 и М 100. Марка мазута характеризует максимальное значение условной вязкости при температуре 50 °С. Флотские мазуты относятся к категории легких топлив, топочный мазут марки М 40 – к категории средних топлив, топочный мазут марки 100 – к категории тяжелых топлив.
В пределах марок топочные мазуты подразделяются на три сорта в зависимости от содержания серы: малосернистые (Sр £ 0,5 %), сернистые (Sр = 0,5-2,0 %) и высокосернистые (Sр = 2,5-3,5 %). Для мазута, получаемого при переработке высокосернистой нефти, допускается содержание серы не более 4,3 %.
Соединения, образующие мазут, состоят из пяти основных элементов: углерода, водорода, серы, кислорода и азота. Элементный состав горючей массы зависит от состава исходной нефти и глубины ее переработки. Минеральные примеси в мазутах представляют собой в основном соли щелочных металлов, а также продукты коррозии резервуаров. Зольность топочных мазутов весьма незначительна и обычно не превышает 0,1 %. Содержание воды в мазутах колеблется в
Дата добавления: 2016-11-26; просмотров: 2820;











