ВМС (высокомолекулярные соединения). Физико-химические свойства высокомолекулярных соединений и их растворов.
План лекции:
1 Основные понятия химии полимеров. Строение высокомолекулярных соединений.
2 Изоэлектриеская точка полиамфолитов
3 Термодинамика образования растворов биполимеров
4 Осмотическое давление растворов биополимеров
5 Мембранное равновесие
6 Аномальная вязкость растворов ВМС
7 Агрегативная устойчивость растворов ВМС и ее нарушение
8 Коллоидная защита
Основные понятия химии полимеров. Строение высокомолекулярных соединений.
Многие высокомолекулярные соединения (ВМС) являются полимерами с молекулярной массой >104. Молекулы биополимеров состоят из большого числа мономерных звеньев - повторяющихся одинаковых групп атомов. Структурные единицы ВМС - макромолекулы (104-106 г/моль). Размер макромолекул весьма велик по сравнению с размерами обычных молекул. Например, если длина молекулы этана составляет несколько ангстрем, то длина некоторых линейных макромолекул составляет 4000- 8000 Ǻ (при поперечном размере 3-7,5 А). Моделью подобных молекул могут служить нити длиной от 800 до 1600 мм и диаметром 1 мм.
Структурной химической основой организмов являются природные высокомолекулярные биополимеры: белки, нуклеиновые кислоты, полисахариды, пектины, натуральный каучук, а также биополимеры смешанного типа: липопротеиды, гликопротеиды и липополисахариды. Природные ВМС характеризуются постоянным значением молекулярной массы.
Синтетические полимеры получаются в результате реакции полимеризации или поликонденсации. К ним относятся: полиэтилен, синтетический каучук, фенолформальдегидные пластмассы. Синтетические полимеры состоят из смеси макромолекул, различных по длине и массе. Таким образом, ВМС - это обычные органические вещества, молекулы которых имеют очень большой размер.
Практически все важные свойства ВМС тесно связаны с их строением. Различают три типа структуры цепей: линейную, разветвленную и пространственную (сетчатую) (рис. 14.1).
Линейные ВМС представляют собой открытую линейную цепь (натуральный каучук, целлюлоза).
Макромолекулы разветвленных ВМС имеют форму линейной цепи с ответвлениями (амилопектин, гликоген).
Пространственные (сетчатые) ВМС, макромолекулы которых представляют собой трехмерные сетки, образованы отрезками цепного строения (например, фенолформальдегидные смолы). Из пространственных полимеров в особую группу выделяют полимеры со сшитой структурой, цепи которых сшиты короткими мостиками.
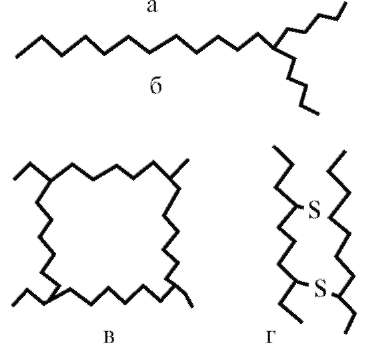
Рис. 1.Схемы строения макромолекул полимеров: а - линейного; б - разветвленного; в - пространственного; г - сшитого
Однако из всех структур именно линейной формой макромолекул определяются типичные свойства полимеров: каучукоподобная эластичность, способность образовывать прочные пленки и нити, набухать, давать при растворении вязкие растворы. Эти свойства цепных макромолекул и их растворов представляют наибольший интерес. Полимеры с пространственной структурой не способны растворяться, поэтому свойства сетчатых полимеров мы не рассматриваем.
Специфические свойства полимеров обусловлены гибкостью линейных макромолекул. Чтобы понять причину гибкости линейных макромолекул, рассмотрим строение молекулы этана, представляющую из себя две группы Н3С-, соединенные одинарной связью. Известно, что группы Н3С- способны вращаться вокруг одинарной связи С-С. Это хорошо согласуется с тем, что, например, ни сам этан,
ни бутан, ни симметричный дихлорэтан при комнатной температуре не имеют изомеров. Однако при низких температурах свободное вращение вокруг связи С-С затруднено, так как не все возможные положения группы -СН3 относительно друг друга равноценны в энергетическом отношении. Такая неравноценность обусловлена тем, что при повороте одной группы -СН3 по отношению к другой изменяется расстояние между С-Н-связями обеих групп. Это ведет к изменению энергии взаимодействия между группами -СН3. Поэтому при низких температурах -СН3 группы не вращаются вокруг оси С-С, а лишь вращательно колеблются на сравнительно небольшой угол. Только при достаточно высокой температуре благодаря увеличению кинетической энергии может быть преодолен энергетический барьер, и группы -СН3 будут свободно вращаться вокруг соединяющей их связи.
Высота потенциального барьера тем больше, чем больше разность максимального и минимального значения энергии взаимодействия атомов или групп атомов при их вращении относительно друг друга. В положении, когда связи находятся одна за другой, расстояние между ними минимально и взаимодействие друг с другом будет максимальным - энергия U1.
Когда связи или атомные группы находятся на максимальном расстоянии друг от друга, то энергия взаимодействия между ними будет минимальной (U2).
Очевидно, что поворот звеньев и переход молекул из одной конфор-мации в другую отвечает изменению потенциальной энергии:
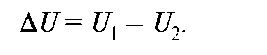
Эта величина носит название потенциального (энергетического) барьера вращения и служит мерой термодинамической гибкости полимерных цепей. Чем меньше величина ΔU, тем легче происходит вращение, и цепь является более гибкой. Полимеры с гибкими макромолекулами легко деформируются и вновь возвращаются в исходное состояние после снятия нагрузки, т.е. обладают свойством эластичности. Подобные тела проявляют одновременно свойства жидкостей и твердых тел. К таким системам относятся и гели.
Межклеточное вещество состоит из протеогликанов, находящихся в гелеобразном состоянии, белков коллагена, эластина и фибронек-тина. Эластин по сравнению с коллагеном содержит больше остатков гидрофобных аминокислот; резиноподобный характер этого полимера обусловливает достаточно большую его способность к упругому растяжению. В меньшей степени это характерно для коллагена.
Повышение энергетического барьера приводит к увеличению жесткости макромолекул. Наименьшим барьером вращения и наибольшей гибкостью характеризуются цепи неполярных незамещенных углеводородов (ΔU = 1-3 кДж/моль). Введение полярных заместителей (-CONH-, -СООН, -ОН, -С1) увеличивает высоту энергетического барьера и повышает жесткость цепей. Это объясняется тем, что введение полярных групп усиливает взаимодействие звеньев как внутри макромолекул (внутримолекулярное взаимодействие), так и между соседними молекулами (межмолекулярное взаимодействие).
Таким образом, гибкость цепей полимеров зависит от химического строения цепи, природы заместителей, их числа и распределения по длине цепи, от числа звеньев цепи.
Дата добавления: 2016-11-26; просмотров: 3729;











