Осмотическое давление растворов биополимеров
Растворы ВМС представляют собой истинные растворы, т.е. гомогенные, термодинамически устойчивые, не нуждающиеся в стабилизаторе, и образующиеся самопроизвольно системы. Однако растворы ВМС рассматривают в коллоидной химии, так как размеры их молекул приближаются, а в некоторых случаях даже превосходят размер коллоидных частиц. Кроме того, растворы ВМС в «плохих» растворителях содержат молекулы или агрегаты молекул с явно выраженной межфазной поверхностью. В концентрированных растворах ВМС обычно возникают достаточно большие ассоциаты молекул, которые можно рассматривать как вторую фазу. Наконец, растворы ВМС благодаря большим размерам их молекул обладают рядом свойств лиозолей: схожестью оптических свойств, малой скоростью диффузии, низким осмотическим давлением. Все это позволяет рассматривать многие проблемы одновременно и для коллоидных растворов, и для растворов ВМС.
В противоположность золям осмотическое давление растворов ВМС существенно и может быть измерено с достаточной точностью, что используется для определения их молекулярной массы.
С повышением концентрации ВМС их осмотическое давление перестает подчиняться закону Вант-Гоффа (π = cRT) и растет быстрее, причем экспериментально полученная кривая лежит выше теоретической прямой.
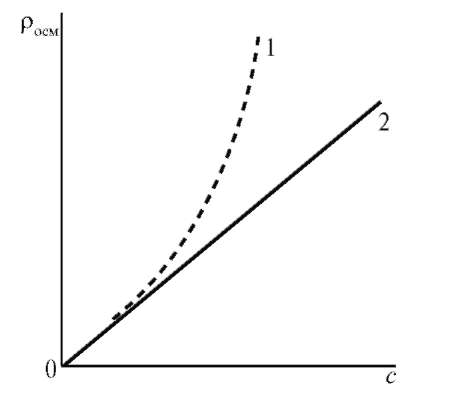
Рис. 14.6.Зависимость осмотического давления от концентрации раствора: 1 - раствор ВМС; 2 - раствор низкомолекулярного неэлектролита
Причиной отклонения от законов Вант-Гоффа является гибкость цепей ВМС, которые ведут себя, как несколько коротких молекул. Для расчета осмотического давления растворов ВМС предложено уравнение Галлера:

где c - концентрация раствора ВМС, г/л; М - молярная масса, г/моль; b - коээфициент, учитывающий гибкость и форму молекулы ВМС в растворе.
В сложных биологических системах суммарное осмотическое давление создается как низкомолекулярными электролитами и неэлектролитами, так и биополимерами. Составляющая суммарного осмотического давления, которая обусловлена наличием белков и других частиц коллоидного размера, называется онкотическим давлением. Доля онкотиче-ского давления относительно невелика: она составляет примерно 0,5% от суммарного осмотического давления (≈3,1кПа), однако отклонение этой величины от нормы приводит к серьезным нарушениям в функционировании организма.
Дата добавления: 2016-11-26; просмотров: 2399;











