Агрегативная устойчивость растворов ВМС и ее нарушение
Растворы ВМС агрегативно устойчивы, как и истинные растворы. Однако при введении больших количеств электролитов наблюдается выделение ВМС из раствора. Но это не следует отождествлять с коагуляцией типичных коллоидных систем. Коагуляция золей происходит при введении сравнительно небольших количеств электролита и представляет собой обычно необратимое явление. Выделение же из раствора ВМС происходит при добавлении относительно больших количеств электролита, не подчиняется правилу Шульце-Гарди и является обычно обратимым процессом. После удаления из осадка электролита промыванием или диализом ВМС снова способно к растворению.
Коагуляция золей происходит за счет сжатия двойного электрического слоя и исчезновения заряда на поверхности частицы. Выделение из раствора полимера при добавлении электролита объясняется уменьшением растворимости ВМС в концентрированном растворе электролита. Такое явление называется высаливанием.
Считается, что при высаливании молекулы растворенного вещества вытесняются из электрического поля введенных ионов, которые связываются с полярными молекулами растворителя. Таким образом, высаливание принципиально не отличается от выделения ВМС из раствора при добавлении нерастворителя. Как правило, высаливающее действие ионов изменяется соответственно тому порядку, в каком они стоят в лиотропном ряду. Так, катионы по мере уменьшения их высаливающей способности могут быть расположены в ряд:
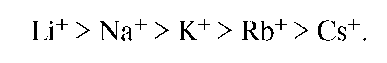
Подобный же ряд анионов имеет вид:
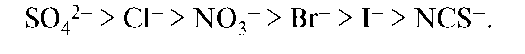
Взаимосвязь между высаливающим действием и местом иона в лио-тропном ряду вполне понятна: чем больше ион способен связывать растворитель, тем больше он будет уменьшать способность среды растворять ВМС.
Высаливание лежит в основе одного из методов фракционирования ВМС, поскольку способность этих соединений выделяться из раствора весьма сильно зависит от их химической природы и резко возрастает с увеличением молекулярной массы. Особенно широко применяется фракционирование с помощью высаливания при разделении белков. При этом высаливание часто сочетают с введением в систему нерастворителя (спирт) и охлаждением раствора. Высаливание белков целесообразно проводить при значении pH, близком к изоэлектрической точке, так как при значении pH, большем или меньшем изоэлектри-ческой точки, возрастают заряд и гидратация белковых молекул и увеличивается их растворимость.
В растворах ВМС при изменении температуры, pH или при введении низкомолекулярных веществ иногда наблюдается явление коацер-вации. Это явление заключается в разделении системы на две фазы, из которых одна представляет собой раствор ВМС в растворителе, а другая - раствор растворителя в ВМС. Раствор, более богатый ВМС, обычно выделяется в виде мельчайших капелек.
Практическая важность коацервации возросла в связи с развитием технологии микрокапсулирования. Микрокапсулирование в фармации используют с целью защиты лекарственного вещества от соприкосновения с окружающей средой. Микрокапсулы представляют заключенные в оболочку из полимера твердые, жидкие или газообразные лекарственные вещества. Оболочка их образуется из адсорбированных капель коацервата полимера, которые слипаются в сплошную пленку и специальной обработкой переводятся в твердое состояние.
Коацервация, используемая при микрокапсулировании, подразделяется на простую и сложную.
Простая коацервация наблюдается при обезвоживании гидрофильных коллоидных растворов, что приводит к снижению их растворимости. В простых коацерватах объединяются молекулы одного и того же химического соединения. В качестве материала для пленкообразования используют желатин и фибриноген.
Сложная коацервация обусловлена взаимодействием между положительными и отрицательными ионами различных молекул полиэлектролитов. Она происходит при изменении концентрации раствора полимера или изменении pH. Сложные коацерваты делят на три типа: однокомплексные, двухкомплексные и трехкомплексные.
В однокомплексных - молекулы одного и того же соединения притягиваются положительными и отрицательными зарядами друг к другу, что вызывает микроскопические изменения в системе. Пример - образование коацерватов из молекул белка в изоэлектри-ческой точке.
В основе двухкомплексной коацервации лежит взаимодействие двух соединений с противоположно заряженными ионами. Например, желатин и гуммиарабик.
Трехкомплексные коацерваты являются сложными системами, образованными из полиамфолита, поликислоты или полиоснования и низкомолекулярного иона.
Коллоидная защита
Белки плазмы оказывают защитное действие по отношению к коллоидно-дисперсным частицам крови, повышая агрегативную устойчивость системы в целом. Этот феномен известен под названием коллоидная защита. Количественно защитное действие ВМС оценивают в «золотых» числах. «Золотым» числом называют минимальную массу ВМС в миллиграммах, предотвращающую коагуляцию 10 мл коллоидного раствора золота [w(Au) = 0,0006%] при добавлении к нему 1 мл раствора хлорида натрия [w(NaCl) = 10%]. Чем меньше «золотое» число данного ВМС, тем сильнее выражено его стабилизирующее действие (табл. 14.2).
Таблица 2.«Золотые» числа некоторых биополимеров
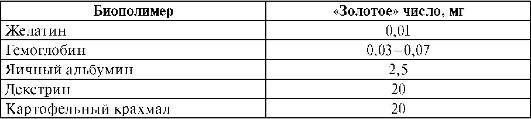
Белковый состав плазмы оказывает влияние на вязкость крови. При некоторых патологических состояниях изменяются белковый состав плазмы и как следствие вязкость крови. Причиной этих изменений чаще всего является образование крупных агрегатов: слипшихся эритроцитов, тромбоцитов, лейкоцитов. Глобулины, существующие в форме макрокатионов, адсорбируются на поверхности эритроцитов, снижая тем самым величину отрицательного заряда их поверхности. Это, в свою очередь, приводит к нарушению агрегативной устойчивости крови (можно оценить по величине СОЭ), увеличению ее вязкости и нарушению гемодинамики.
В современном фармакотерапевтическом арсенале имеются лекарственные средства, уменьшающие вязкость крови (например, пенто-ксифиллин, ксантинола никотинат, ницерголин).
ЛЕКЦИЯ № 11
Гели
План лекции:
1.Характеристика студней и гелей
2.Факторы студне- и гелеобразования
3.Свойства гелей и студней
4.Диффузия в гелях и студнях
5.Периодические реакции в гелях и студнях
Дата добавления: 2016-11-26; просмотров: 4378;











