Схема участия частиц среды в ОВР в зависимости от кислотности раствора
| Кислотность (рН) | Исходные частицы | Продукты |
| Кислая среда (рН<7) | Н+ и Н2О | Н2О и ОН- |
| Нейтральная среда (рН = 7) | Н2О | Н+ и (или) ОН- |
| Щелочная среда (рН>7) | Н2О и ОН- | Н2О и ОН- |
В качестве примера рассмотрим ту же реакцию.
2.1. Молекулярная схема реакции.
K2Cr2O7 + H2S + H2SO4 = Cr2(SO4)3 + S + K2SO4 + H2O
2.2. Ионно–молекулярная схема реакции. Для ее составления необходимо все сильные электролиты представить в виде ионов, а слабые электролиты оставить в виде молекул. К сильным электролитам относятся все соли, часть кислот (HCl, HNO3, H2SO4 и др.), щелочи (LiOH, NaOH, KOH и др.).
2K+ + Cr2O7-2 + H2S + 2H+ + SO4-2 = 2Cr+3+3SO4-2 + S0 + 2K+ +SO4-2 + H2O
2.3. Определяются частицы, изменившие свой заряд или состав.
Cr2O7-2 → 2Cr+3 и H2S → S0.
В данной реакции ионы водорода и молекулы воды выполняют роль среды, которая является кислой.
2.4. На основании этих превращений составляются полуреакции окисления и восстановления с участием частиц среды (см.табл.8.1). В первой реакции дихромат анион потерял 7 атомов кислорода, которые в кислой среде связываются ионами водорода и превращаются в воду. Во второй реакции молекула сероводорода потеряла 2 атома водорода.
Cr2O7-2 + 14Н+ → 2Cr+3 + 7Н2О
H2S → S0 + 2Н+
2.5. Полученные полуреакции необходимо уравнять по зарядам. В первом уравнении слева суммарный заряд равен (+12), а справа – (+6), значит, дихромат ион присоединил 6 электронов и восстановился. Во втором уравнении слева (0), а справа – (+2). Молекула сероводорода потеряла 2 электрона и окислилась.
Cr2O7-2 + 14Н+ +6  → 2Cr+3 + 7Н2О
→ 2Cr+3 + 7Н2О
H2S - 2  → S0 + 2Н+
→ S0 + 2Н+
2.6. Для соблюдения электронного баланса второе уравнение необходимо умножить на 3, после чего просуммировать уравнения.
Cr2O7-2 + 14Н+ +6  → 2Cr+3 + 7Н2О
→ 2Cr+3 + 7Н2О
3 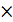 H2S - 2
H2S - 2  → S0 + 2Н+
→ S0 + 2Н+
Cr2O7-2 + 14Н+ + 3H2S = 2Cr+3 + 7Н2О + 3S0 + 6Н+
После сокращения подобных частиц в левой и правой частях уравнения получим суммарное ионно-молекулярное уравнение, которое отражает смысл произошедшей реакции.
Cr2O7-2 + 8Н+ + 3H2S = 2Cr+3 + 7Н2О + 3S0
Перенос полученных коэффициентов в молекулярную схему реакции позволяет получить ее полное уравнение.
K2Cr2O7 + 3H2S + 4H2SO4 = Cr2(SO4)3 + 3S + K2SO4 + 7H2O
Метод позволяет уравнивать не только атомы окислителя и восстановителя, но и атомы водорода и кислорода, что значительно упрощает подбор дополнительных коэффициентов.
Вопрос о принципиальной возможности или невозможности окислительно-восстановительных реакций решается так же, как и для всех других. Реакция термодинамически разрешена, если она протекает с уменьшением свободной энергии Гиббса, т.е. ΔGхр< 0. Однако этот вопрос для ОВР может быть решен и методом сравнения окислительно-восстановительных потенциалов сопряженных пар окислителя и восстановителя. Потенциал является мерой их окислительно-восстановительной способности. Подробно этот вопрос будет освещен в разделе «Основы электрохимических процессов».
Дата добавления: 2021-01-26; просмотров: 477;











