Зависимость скорости ферментативной реакции от концентрации фермента и концентрации субстрата
Зависимость скорости реакции от концентрации фермента и концентрации субстрата (кинетика ферментативных реакций) представлена соответственно на графиках.
График 1 График 2
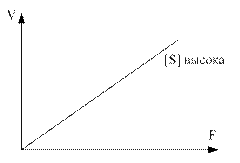
В ферментативной реакции выделяют скорости трёх составляющих этапов:
- образование фермент-субстратного комплекса FS;
- обратный распад фермент – субстратного комплекса;
- распад фермент-субстратного комплекса с образованием продуктов реакции.
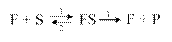
Скорость каждой из этих реакций подчиняется закону действующих масс:
V1 = К1 [F] ·[S]
V2 = K2 [FS]
V3 = K3 [FS]
В момент равновесия скорость реакции образования FS равна сумме скоростей его распада: V1=V2+V3. Из трёх этапов ферментативной реакции наиболее важным и медленным является третий, так как он связан с образованием продуктов реакции. По приведенной выше формуле найти скорость V3 невозможно, так как фермент- субстратный комплекс очень неустойчив и измерение его концентрации затруднено. В связи с этим, Л. Михаэлис, М.Ментен ввели константу Михаэлиса - Кm и преобразовали уравнение для измерения V3 в новое уравнение, в котором присутствуют реально измеримые величины. Ниже представлены два варианта данного уравнения
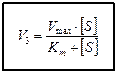
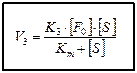
[F0] – исходная концентрация фермента;
Кm – константа Михаэлиса.
Физический смысл Кm: Кm = (К2+К3) /К1, т.е. она показывает соотношение констант скоростей распада фермент-субстратного комплекса и константы скорости его образования.
Уравнение Михаэлиса-Ментен является универсальным. Оно иллюстрирует зависимость скорости реакции от [F0] от [S].
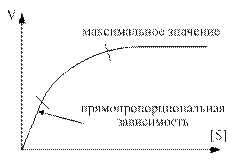
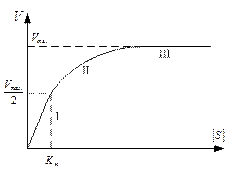
1. Зависимость скорости реакции от концентрации субстрата. Эта зависимость выявляется при малых концентрациях субстрата [S]<Km. В этом случае концентрацией субстрата в уравнении можно пренебречь и уравнение приобретает вид: 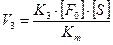 . В данном уравнении K3, [F0], Km – константы и могут быть заменены новой константой К*. Таким образом, при малой концентрации субстрата скорость реакции прямо пропорциональна этой концентрации V3 = K* · [S]. Эта зависимость соответствует первому участку графика 2.
. В данном уравнении K3, [F0], Km – константы и могут быть заменены новой константой К*. Таким образом, при малой концентрации субстрата скорость реакции прямо пропорциональна этой концентрации V3 = K* · [S]. Эта зависимость соответствует первому участку графика 2.
2. Зависимость скорости от концентрации фермента проявляется при высокой концентрации субстрата. S > Km. В этом случае можно пренебречь Km и уравнение преобразуется в следующее: 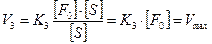 . Таким образом, при высокой концентрации субстрата скорость реакции определяется концентрацией фермента и достигает максимального значения V3 = K3[F0]=Vmax. (третий участок графика 2).
. Таким образом, при высокой концентрации субстрата скорость реакции определяется концентрацией фермента и достигает максимального значения V3 = K3[F0]=Vmax. (третий участок графика 2).
3. Уравнение позволяет определить численное значение Km при условии 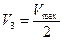 . В этом случае оно приобретает вид:
. В этом случае оно приобретает вид: 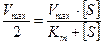 , откуда следует, что Km=[S]
, откуда следует, что Km=[S]
Таким образом, Кm численно равна концентрации субстрата при скорости реакции, равной половине максимальной. Кm является очень важной характеристикой фермента, она измеряется в молях (10-2 – 10-6 моль) и характеризуют специфичность фермента: чем ниже Km, тем выше специфичность фермента.
Графическое определение константы Михаэлиса возможно на графике зависимости скорости ферментативной реакции от концентрации фермента (слева).
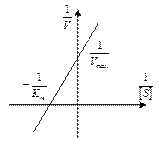
Удобнее использовать график, представляющий прямую линию. Такой график предложен Лайнуивером – Берком (график двойных обратных величин), который соответствует обратному уравнению Михаэлиса – Ментен (справа)
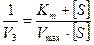 .
.
Дата добавления: 2016-09-26; просмотров: 1880;











