Глава III. 2. ОСНОВЫ ТЕРМОДИНАМИКИ
§III.2.1 ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
1. Что понимают под: энергией тела; внутренней энергией тела?
2. Как изменится внутренняя энергия идеального газа, если его молекулы будут состоять из нескольких атомов? Почему?
3. Как изменится внутренняя энергия идеального газа при изотермическом сжатии?
A. увеличивается;
B. уменьшается;
C. не изменяется.
4. Сравните значения внутренней энергии водорода и кислорода при одинаковых их массах и температурах?
A. внутренняя энергия водорода в 16 раз больше;
B. внутренняя энергия кислорода в 16 раз больше;
C. внутренняя энергия водорода и кислорода одинакова.
5. Как изменится внутренняя энергия идеального газа при увеличении его давления и объема в 3 раза?
A. увеличивается в 3 раза;
B. увеличивается в 9 раз;
C. увеличивается в 6 раз;
D. не изменяется.
6. Что такое число степеней свободы молекул газа? Чему равно число степеней одно-, двух-, трехатомных и многоатомных молекул?
7. В чем состоит закон равномерного распределения энергии по степеням свободы и всегда ли он выполняется?
8. Что называется теплоемкостью?
9. От чего зависит теплоемкость газов, и в каких пределах она может изменяться?
10. Получите выражение для разности молярных теплоемкостей: 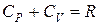 . Почему
. Почему 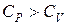 ? Каков физический смысл универсальной газовой постоянной R?
? Каков физический смысл универсальной газовой постоянной R?
11. Выведите уравнение Пуассона.
12. Изобразите в зависимости р от V изотерму и адиабату. Объясните, почему адиабата с ростом V спадает круче, чем изотерма.
13. Выведите формулы для расчета работы различных изопроцессов и покажите, как изображается эта работа на графиках в зависимости р от V.
14. Начальное состояние газа характеризуется параметрами р1 и V1. При каком расширении, изотермическом или изобарном, газ совершит большую работу? Ответ обоснуйте графически в системе координат (р,V).
15. Что такое количество теплоты? В каких единицах она измеряется?
16. При передаче телу некоторого количества теплоты…
A. температура тела всегда повышается;
B. температура тела не всегда повышается.
17. При изотермическом расширении идеального газа температура и внутренняя энергия его не изменяются. Куда же идет подводимая теплота?
18. Проанализируйте различные формулировки первого закона термодинамики.
19. Один моль идеального газа изобарно нагревают от температуры Т до 3Т. Какое количество теплоты необходимо для этого?
A. 3RT;
B. 2RT;
C. 5RT.
20. Внешние силы совершили работу 300 Дж по адиабатному сжатию газа. Как изменилась при этом внутренняя энергия газа?
A. увеличилась на 300 Дж;
B. уменьшилась на 300 Дж;
C. не изменилась.
21. В результате изотермического расширения газ совершил работу 500 Дж. Какое количество теплоты было сообщено газу в этом процессе?
A. 500 Дж;
B. 250 Дж;
C. при изотермическом расширении газа теплота не потребляется.
22. Один моль одноатомного идеального газа, находящегося при температуре Т, нагревают. Определите количество теплоты, которое надо подвести к газу, чтобы изобарно увеличить его объем вдвое?
A. 1,5 RT;
B. 2,5 RT;
C. 2RT;
D. 3RT.
23. Кислород массой 0,32 кг нагрели на 100 К, сообщив ему количество теплоты 30 кДж. Найти приращение внутренней энергии кислорода и совершённую им работу.
§III.2.2 ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ
1. Какие состояния называются равновесными и неравновесными?
2. Какие процессы называются равновесными, и какие неравновесными?
3. Какие процессы называются обратимыми, какие – необратимыми? Может ли равновесный процесс быть обратимым?
4. Какие процессы называют круговыми? Обязательно ли круговой процесс должен быть и обратимым?
5. Запишите общее выражение для к.п.д. любого кругового процесса.
6. Сформулируйте второй закон термодинамики.
7. Какие следствия вытекают из второго начала термодинамики, касающиеся работы теплового двигателя?
8. Из каких процессов состоит цикл Карно? Покажите на диаграмме цикла те его участки, которые соответствуют контакту рабочего вещества с нагревателем и холодильником. На каких участках рабочее вещество не имеет теплообмена с окружающей средой?
9. Как, пользуясь диаграммой цикла Карно, подсчитать работу, совершенную газом при расширении?
10. Выведите из общего выражения для к.п.д. любого кругового процесса формулу к.п.д. для цикла Карно. Почему к.п.д. цикла Карно определяется только температурами нагревателя и холодильника?
11. Приведите примеры реально осуществимых круговых замкнутых процессов (циклов).
12. Приведите различные формулировки второго закона термодинамики.
13. Что такое приведенное количество теплоты? Что такое энтропия?
14. Чему равно изменение энтропии обратимого и необратимого цикла?
15. Как связана термодинамическая вероятность состояния с энтропией (уравнение Больцмана)?
16. Что такое флуктуация? Является ли броуновское движение проявлением флуктуации?
17. Найти коэффициент полезного действия цикла, состоящего из двух изобар и двух изотерм.
18. Газ совершает цикл Карно. Абсолютная температура нагревателя в 4 раза выше абсолютной температуры холодильника. Какую долю теплоты, получаемой за один цикл от нагревателя, газ отдает холодильнику?
19. Найти изменение энтропии при превращении 10 г льда, взятого при -200С, в пар при 1000С.
20. В результате изохорического нагревания одного грамма водорода давление газа увеличилось в 2 раза. Определить изменение энтропии.
21. 10 г водорода расширяется изобарически до удвоенного объема. Найти изменение энтропии.
§III.2.3 РЕАЛЬНЫЕ ГАЗЫ
1. В чем состоят основные отличия модели реального газа от модели идеального газа?
2. Используя уравнение состояния идеального газа получите уравнение состояния реального газа (уравнение Ван – дер– Ваальса)?
3. Какие имеются основания считать, что уравнение Ван – дер – Ваальса в большей мере отвечает свойствам газа, чем уравнение Менделеева – Клапейрона?
4. Запишите уравнение Ван –дер–Ваальса для одного моля газа, для массы m. Объясните все параметры, входящие в него.
5. Найти выражение для работы А, совершаемой киломолем газа при изотермическом расширении. Считать, что газ подчиняется уравнению Ван – дер – Ваальса.
6. Изобразите систему изотерм Ван–дер–Ваальса. Что означает точка перегиба? На какой изотерме имеется эта точка?
7. Изобразите систему опытных изотерм для реального газа. Что означают участки кривых, параллельные оси абсцисс? На плоскости р,V укажите области газа, пара, жидкости и двойной фазы. Покажите на диаграмме точку, соответствующую критическому состоянию.
8. Что называется критическим состоянием вещества? У всех ли веществ имеется критическое состояние?
9. Что такое критическая температура, давление, объем?
10. Вычислить критическую температуру Ткр и критическую плотность ρкр углекислого газа (СО2).
11. Можно ли газ обратить в жидкость при температуре выше критической? При давлении выше критического? При объеме больше критического?
12. Какой пар принято считать насыщенным? Укажите на диаграмме опытных изотерм в осях (р,V) области с насыщенным и ненасыщенным паром.
13. Какому давлению соответствуют горизонтальные участки опытных изотерм?
14. Зависит ли внутренняя энергия реальных газов от объема?
15. В чем состоит эффект Джоуля – Томсона? Каковы его причины?
16. Объясните отрицательный эффект Джоуля – Томсона (нагревание газа при расширении без подвода теплоты). Какую роль при этом выполняет потенциальная энергия взаимодействия молекул? Зависит ли эта энергия от температуры?
17. Как изменилось бы давление внутри газа, если бы силы притяжения между молекулами исчезли?
18. Найти внутреннее давление воды.
19. Один киломоль идеального газа и один киломоль реального газа занимают один и тот же объем и имеют одинаковую температуру. Какой газ будет оказывать большее давление на стенки сосуда и насколько?
20. Найти значения критических параметров для воды и ее критическую плотность.
§III.2.4 ЖИДКОСТИ
1. Каковы отличительные особенности молекулярного строения жидкости?
2. Что такое «ближний порядок» в расположении молекул?
3. Чем объясняется свойство текучести жидкости?
4. Какими свойствами обладает поверхностный слой жидкости?
5. Объясните особенности поверхностного слоя с двух точек зрения: энергетической и динамической.
6. Какие силы обусловливают сокращение поверхности жидкости?
7. Будет ли изменяться поверхностное натяжение с ростом температуры?
8. Какую величину называют коэффициентом поверхностного натяжения? Чему он равен при критической температуре?
9. Что такое лапласовское давление? Как оно возникает?
10. Объясните растекание жидкости по твердому телу с точки зрения действия сил поверхностного натяжения. Что такое краевой угол?
11. В чем состоит явление абсорбции? Почему поверхностно активные вещества всегда уменьшают поверхностное натяжение жидкости?
12. Внутри пузыря из мыльной воды добавочное давление 0,32 мм.рт.ст. Каков радиус этого пузыря, какую работу надо совершить для выдувания пузыря и какова свободная энергия поверхностной пленки пузыря?
13. Сообщающиеся сосуды наполнены жидкостью. Температура жидкости в одном из них повышается, а в другом остается неизменной. Меняется ли при этом уровень жидкости во втором сосуде?
14. В сосуде с водой плавает кусок льда. Изменится ли уровень воды после того, как лед растает, если температура воды останется равной 00С?
15. В каком сосуде быстрее закипит смачивающая (несмачивающая) его жидкость – в широком или капиллярном?
16. Почему из мыльной воды легко выдуть пузырь, а из чистой нельзя?
17. На дне водоема выделяются пузырьки газа радиусом 0,02 мм. Чему будет равен их радиус, если пузырьки поднимутся на половину глубины к поверхности? Глубина водоема 5 м.
§III.2.5 ТВЁРДЫЕ ТЕЛА
1. Что такое кристалл? Какие тела называют монокристаллическими, какие – поликристаллическими? Почему поликристаллические тела относятся к изотропным?
2. Перечислите основные физические свойства кристаллических и аморфных тел.
3. По какому принципу осуществляется укладка атомов и молекул в кристаллах?
4. Из чего образована идеальная кристаллическая решетка? Какие типы кристаллических решеток вам известны?
5. Какие дефекты встречаются в структуре кристалла?
6. Что такое дислокация?
7. Какими способами повышают прочность твердых тел?
8. Какова роль кристаллов в живых организмах?
9. В чем состоит классическая теория теплоемкостей твердых тел? Каковы ее трудности?
10. Кем была создана теория теплоемкости кристаллических тел, учитывающая квантование колебательной энергии и кто ее в последствии усовершенствовал?
11. Какую величину принято называть характеристической температурой Дебая? Что она указывает?
12. Что означает тройная точка? Как зависит температура плавления от давления?
13. Может ли твердое тело превратиться в газ без плавления?
14. Как изменяется температура плавления твердых тел от примесей?
15. Стальную масштабную линейку при 00С требуется отградуировать так, чтобы миллиметровые интервалы при определенной температуре гарантировали измерение с точностью до 0,001 мм. Определить максимальную температуру, допустимую при градуировке.
16. Часы с металлическим маятником спешат на 8 сек в сутки при температуре 30 С и отстают на 7 сек при температуре 230 С. Найти коэффициент линейного расширения материала маятника.
17. Какой длины стальной трос постоянного сечения разорвется под влиянием собственной тяжести? Какие в связи с этим предложения можно сделать о конструировании тросов для подъемников глубоких шахт, если в этих конструкциях должен быть десятикратный запас прочности?
18. Для того чтобы колеса вагонов не стучали на стыках рельсов, рельсы сваривают. Найти напряжение в поперечном сечении такого рельса при изменении температуры на 300 С. Найти силу, действующую на поперечное сечение рельса площадью 1 дм2. При каком изменении температуры может произойти разрыв рельса?
19. Найти количество теплоты, теряемой за 1с с площади 1м2 кирпичной стены толщиной 51см, а также температуру внутренней и внешней поверхностей стены, если температура в помещении 200С, а температура наружного воздуха –200С. Коэффициент теплоотдачи со стороны помещения 12 Вт/(м2·К), а с наружной стороны 6 Вт/(м2·К).
20. Для уменьшения тепловых потерь стеной здания, рассмотренной в предыдущей задаче, и повышения температуры внутренней поверхности стены применена изоляция слоем пробки толщиной 5см в двух вариантах:
A. слой пробки покрывает стену с внутренней стороны здания;
B. слой пробки покрывает стену с наружной стороны здания.
Определить температуру кирпичной стены с внутренней стороны здания в обоих вариантах. Указать, какой из вариантов, является наиболее выгодным и какой процент теплоты с его помощью можно сберечь.
ЗАКЛЮЧЕНИЕ
Уважаемые студенты, предложенное Вашему вниманию учебное пособие «Основы молекулярной физики и термодинамики» было написано в соответствии с действующей программой курса общей физики для инженерно-технических специальностей вузов. Хотелось бы отметить, что среди всех дисциплин, изучаемых в вузе нет таких, которые могли бы сравниться с курсом физики по богатству и многообразию идей, методов исследования и фундаментальности изучаемых в нём явлений и законов.
Мы старались путём тщательного отбора и лаконичного изложения материала, достигнуть того, чтобы предложенный материал был доступен Вам и понятен, невзирая на степень Вашей подготовки.
Изложение материала велось без громоздких математических выкладок, должное внимание уделялось физической сути явлений.
Дорогие студенты, очень надеемся, что данное пособие стало для Вас неоценимым помощником при овладении одним из важных разделов общего курса физики.
Авторы выражают глубокую признательность профессору А.М. Баранову, профессору М.В. Гореву, профессору И.Н. Флёрову, доценту Т.Г. Зингель, за доброжелательные замечания и пожелания, которые способствовали улучшению учебного пособия: «Основы молекулярной физики и термодинамики».
Основная литература
1. Савельев, И.В. Курс общей физики: в 5 кн. Кн. 1 / И.В. Савельев. – М.: Наука; Физматлит, 1989. – 350 с.
2. Трофимова, Т.И. Курс физики: Учебное пособие для инженерно-технических специальностей вузов / Т.И. Трофимова. – 9–е изд., перераб. и доп. – М,: Academia, 2004. – 558 с.
3. Трофимова, Т.И. Курс физики. / Т.И. Трофимова. – М.: Высшая школа, 2003. – 543 с.
4. Детлаф, А.А. Курс физики / А.А. Детлаф, Б.М. Яворский. – М.: Высшая школа, 2001. – 718 с.
5. Волькенштейн, В.С. Сборник задач по общему курсу физики / В.С. Волькенштейн. – М.: Наука, 1999. – 327 с.
6. Чертов, А.Г. Задачник по физике / Чертов А.Г., Воробьев А.А. – М.: Интеграл-пресс, 1997. – 544 с.
7. Трофимова, Т.И. Сборник задач по курсу физики / Т.И.Трофимова. – М.: Высшая школа, 1996. – 303 с.
8. Трофимова, Т.И. Сборник задач по курсу физики с решениями / Т.И. Трофимова, З.Г. Павлова. – М.: Высшая школа, 2004. – 591 с.
Дата добавления: 2016-09-06; просмотров: 2469;











