Электрические свойства нейронов: мембранный потенциал, ионные каналы и распространение сигнала
Представленный ниже материал служит наглядной иллюстрацией общего принципа, согласно которому физиологические процессы подчиняются законам химии и физики — в частности, тем, что управляют направленным движением заряженных молекул. Как уже обсуждалось в главе 4, основными растворёнными веществами во внеклеточной жидкости являются ионы натрия (Na⁺) и хлорид-ионы (Cl⁻). Напротив, внутриклеточная жидкость содержит высокие концентрации ионов калия (K⁺) наряду с ионизированными непроницаемыми молекулами, прежде всего фосфатными соединениями и белками с отрицательно заряженными боковыми цепями. Электрические явления, возникающие вследствие такого распределения заряженных частиц, развёртываются на плазматической мембране клетки и играют критическую роль в интеграции сигналов и межклеточной коммуникации — двух основных функциях нейронов.
Фундаментальный физический принцип гласит, что одноимённые заряды отталкиваются, а разноимённые — притягиваются. Разделённые барьером противоположные заряды обладают способностью совершать работу при их соединении; эта способность называется электрическим потенциалом, или, поскольку определяется разностью зарядов между двумя точками, разностью потенциалов (часто сокращением «потенциал»). Единица измерения — вольт (В), однако в биологических системах общий разделяемый заряд очень мал, поэтому потенциалы измеряют в милливольтах (1 мВ = 0,001 В). Движение электрического заряда именуют током: потенциал стремится вызвать ток, притягивая противоположные заряды или отталкивая одноимённые.
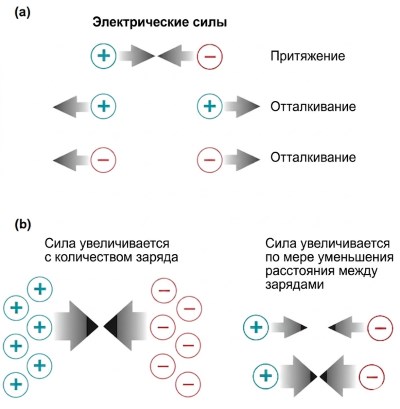
Рисунок 6.7. (а) Типы электрических взаимодействий. (б) Влияние количества и расстояния между зарядами на электрические силы
Величина тока зависит от разности потенциалов между зарядами и от сопротивления материала или структуры, через которые они движутся. Сопротивление является мерой препятствия перемещению заряда: высокое сопротивление даёт слабый ток. Соотношение между напряжением (V), сопротивлением (R) и током (I) выражается законом Ома: I = V / R. Материалы с высоким электрическим сопротивлением называют изоляторами, а с низким — проводниками. Вода с растворёнными ионами — относительно хороший проводник, и поскольку внутриклеточная и внеклеточная жидкости богаты ионами, они легко проводят ток. Липиды же содержат крайне мало заряженных групп, поэтому липидный бислой плазматической мембраны представляет собой область высокого сопротивления, отделяющую два низкоомных водных отсека. Именно такое устройство лежит в основе генерации мембранного потенциала покоя, который у разных нейронов варьирует от –40 мВ до –90 мВ.
Происхождение и поддержание мембранного потенциала покоя. Мембранный потенциал покоя возникает из-за неравномерного распределения ионов по разные стороны плазматической мембраны и её селективной проницаемости. В состоянии покоя мембрана нейрона гораздо более проницаема для K⁺, чем для Na⁺, благодаря наличию протекающих калиевых каналов (leak channels). Поскольку внутри клетки концентрация калия высока, а снаружи — низка, ионы калия диффундируют наружу по своему концентрационному градиенту. Это перемещение положительного заряда из клетки создаёт отрицательный заряд внутри относительно внешней среды, формируя потенциал покоя.
Натрий-калиевый насос (Na⁺/K⁺-АТФаза) активно поддерживает ионные градиенты, транспортируя три иона Na⁺ из клетки и два иона K⁺ внутрь клетки на каждую гидролизованную молекулу АТФ. Этот электрогенный насос прямо (примерно на –5…–10 мВ) влияет на потенциал покоя и косвенно — поддерживая концентрационные градиенты, которые управляют пассивными ионными потоками. Без работы насоса градиенты постепенно рассеялись бы, и нейрон утратил бы способность генерировать электрические сигналы.
Электрохимические градиенты и движущие силы. Суммарное перемещение иона через мембрану определяется как его концентрационным (химическим) градиентом, так и мембранным потенциалом (электрическим взаимодействием). Совокупное влияние называют электрохимическим градиентом. Для каждого иона равновесный потенциал, рассчитываемый по уравнению Нернста, представляет собой значение мембранного потенциала, при котором электрическая сила в точности уравновешивает химическую, и чистого потока иона не возникает. В покое мембранный потенциал близок к равновесному потенциалу для K⁺ (около –90 мВ), но далёк от такового для Na⁺ (около +60 мВ), что отражает высокую покоящуюся проницаемость мембраны именно для калия.
Локальные потенциалы, потенциалы действия и распространение сигнала. Когда нейрон получает синаптический сигнал, нейротрансмиттеры открывают лиганд-управляемые ионные каналы, вызывая кратковременные локальные изменения мембранного потенциала — градуированные (локальные) потенциалы. Если мембрана деполяризуется до критического порога (приблизительно –55 мВ), открываются потенциал-зависимые натриевые каналы: быстрый входящий ток Na⁺ генерирует потенциал действия, следующий принципу «всё или ничего». После этого открываются потенциал-зависимые калиевые каналы, и выходящий ток K⁺ реполяризует мембрану, возвращая её к исходному уровню.
Закон Ома управляет пассивным распространением электрических сигналов внутри нейронов. Постоянная длины (λ) описывает расстояние, на котором градуированный потенциал затухает в e раз; она пропорциональна квадратному корню из сопротивления мембраны и обратно пропорциональна квадратному корню из внутреннего сопротивления аксона. Миелинизация увеличивает сопротивление мембраны и снижает её электрическую ёмкость, тем самым увеличивая постоянную длины и скорость проведения. В миелинизированных аксонах потенциалы действия «перескакивают» между перехватами Ранвье — это явление называют сальтаторной проводимостью.
Клиническое значение и экспериментальные подходы. Нарушения в работе ионных каналов — каналопатии — могут вызывать неврологические расстройства, включая эпилепсию, мигрень и периодические параличи. Местные анестетики (например, лидокаин) блокируют потенциал-зависимые натриевые каналы, предотвращая распространение потенциалов действия и тем самым устраняя болевые сигналы. Понимание электрических свойств нейронов лежит в основе таких методов, как пэтч-кламп (patch-clamp) — запись тока через одиночные каналы, и электроэнцефалография (ЭЭГ), регистрирующая суммарные постсинаптические потенциалы больших популяций кортикальных нейронов.
Таким образом, физические принципы взаимодействия зарядов, разности потенциалов, сопротивления и электрического тока, объединённые законом Ома, полностью применимы к нейрональной сигнализации. Липидный бислой плазматической мембраны действует как изолятор, разделяющий два проводящих водных отсека, что обеспечивает быстрое и контролируемое перемещение ионов. Именно эти процессы лежат в основе всех функций нервной системы — от сенсорной трансдукции до сложных когнитивных способностей.
Сведения об авторах и источниках:
Авторы: Эрик П. Видмайер, Бостонский университет, Хершел Рафф, Медицинский колледж Висконсина, Медицинский центр Авроры Сент-Люк, Кевин Т. Странг, Университет Висконсин-Мэдисон
Источник: Физиология человека: механизмы функционирования организма
Данные публикации будут полезны студентам биологических и медицинских специальностей, начинающим специалистам в области клеточной биологии, биофизики и физиологии, а также всем, кто интересуется основами мембранного транспорта и регуляции клеточного гомеостаза.
Дата добавления: 2026-04-29; просмотров: 154;











